
分析 (1)亚硫酸氢钠溶液中存在水的电离、亚硫酸氢根离子的电离和水解平衡;c(SO32-)>c(H2SO3),说明HSO3-的电离程度大于水解程度;
(2)二者恰好反应生成NaA,根据酸的强弱判断溶液酸碱性;
(3)通常认为残留在溶液中的离子浓度小于1.0×10-5mol.L-1时,沉淀就达到完全,结合氢氧化铁溶度积计算氢氧根离子浓度得到氢离子浓度来计算溶液PH,Mg2+的浓度为1.0×10-2mo1.L-1,镁离子不沉淀的溶液PH依据溶度积计算;要除去混在氯化镁溶液中氯化铁杂质加入试剂能和酸反应调节溶液PH,但不能引入新的杂质.
解答 解:(1)亚硫酸氢钠溶液中存在水的电离、亚硫酸氢根离子的电离和水解平衡,方程式为:H2O?H++OH-、HSO3-?H++SO32-、HSO3-+H2O?H2SO3+OH-,c(SO32-)>c(H2SO3),说明HSO3-的电离程度大于水解程度,溶液呈酸性,则c(H+)大于c(OH-),
故答案为:大于;在NaHSO3溶液中存在HSO3-的电离(HSO3-?H++SO32-)和水解(HSO3-+H2O?H2SO3+OH-),由题给信息c(SO32-)>c(H2SO3)知电离比水解程度大,所以c(H+)>c(OH-);
(2)如果酸是强酸,二者恰好反应生成强酸强碱盐,溶液呈中性,则PH=7,如果酸是弱酸,二者恰好反应生成强碱弱酸盐,溶液呈碱性,则pH>7,
故答案为:大于或等于;若HA是强酸,pH=7,若HA是弱酸,pH>7.
(3)通常认为残留在溶液中的离子浓度小于1.0×10-5mol.L-1时,沉淀就达到完全,结合氢氧化铁溶度积计算,Fe(OH)3的KSP=1.0×10-38mol4•L-4=c(Fe3+)c3(OH-),c3(OH-)=$\frac{Ksp(Fe(OH)_{3})}{c(F{e}^{3+})}$=$\frac{1.0×1{0}^{-38}}{1.0×1{0}^{-5}}$=1.0×10-33,c(OH-)=$\root{3}{1.0×1{0}^{-33}}$=10-11mol/L,c(H+)=$\frac{1{0}^{-14}}{1{0}^{-11}}$=10-3mol/L,溶液PH=3,Mg2+的浓度为1.0×10-2mo1.L-1,镁离子不沉淀的溶液PH,依据溶度积计算,Mg(OH)2的KSP=c(Mg2+)c2(OH-)=1.0×10-11mol3•L-3,c2(OH-)=$\frac{Ksp(Mg(OH)_{2})}{c(M{g}^{2+})}$=$\frac{1.0×1{0}^{-11}}{1.0×1{0}^{-2}}$=1.0×10-9mol/L,c(OH-)=1.0×10-4.5mol?L,c(H+)=$\frac{1{0}^{-14}}{1{0}^{-4.5}}$=10-9.5mol/L,现要除去溶液中的Fe3+,而Mg2+不沉淀,应将溶液的pH控制在3≤pH<9.5,要除去混在氯化镁溶液中氯化铁杂质加入试剂能和酸反应调节溶液PH,但不能引入新的杂质,A.氨水会引入铵根离子杂质离子,D.氧化铜和酸反应会引入铜离子杂质,B.碳酸氢镁 C.氢氧化镁可以调节溶液PH且不引入新的杂质,故选BC,
故答案为:3≤pH<9.5;BC.
点评 本题考查了盐类水解、沉淀溶解平衡的分析计算应用,侧重于学生的分析能力和计算能力的考查,根据溶液酸碱性确定酸式酸根离子电离和水解程度,注意任何溶液中都存在水的电离平衡,为易错点,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径 (10-10m) | 0.73 | 1.02 | 1.34 | 1.06 | 0.99 | .5 4 | 0.75 | 1.18 |
| 最高或最 低化合价 | +6 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -2 | -3 | -1 | -3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯和己烷(溴水) | B. | 矿物油和植物油(NaOH溶液) | ||
| C. | 乙醛和丙烯酸(KMnO4溶液) | D. | 硝基苯和CCl4(水) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 哈伯法合成氨是吸热反应,新法合成氨是放热反应 | |
| B. | 新法合成和哈伯法相比不需要在高温条件下,可节约大量能源,具有发展前景 | |
| C. | 新法合成能在常温下进行是因为不需要断裂化学键 | |
| D. | 新的催化剂升高了反应所需要的能量,提高了活化分子百分数 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
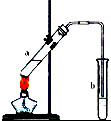 ①生成液体W的化学方程式为CH3CH2OH+CH3COOH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;
①生成液体W的化学方程式为CH3CH2OH+CH3COOH$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com