
| | NaOH起始读数 | NaOH终点读数 |
| 第一次 | 0.10mL | 18.50mL |
| 第二次 | 0.20mL | 18.80mL |
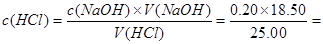 0.148mol/L。
0.148mol/L。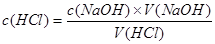 来分析结果是否变高,主要是看氢氧化钠的体积,A项混有Na2CO3杂质,消耗氢氧化钠的体积偏大,结果偏高;B项滴定终点读数时,俯视滴定管的刻度,氢氧化钠的体积偏小,结果偏低;C项无影响;D项滴定管尖嘴处悬挂一滴溶液,说明氢氧化钠的体积偏大,导致待测液浓度偏大;E项未用标准液润洗碱式滴定管,导致标准液浓度偏小,需要的体积变大,使待测液浓度变大。
来分析结果是否变高,主要是看氢氧化钠的体积,A项混有Na2CO3杂质,消耗氢氧化钠的体积偏大,结果偏高;B项滴定终点读数时,俯视滴定管的刻度,氢氧化钠的体积偏小,结果偏低;C项无影响;D项滴定管尖嘴处悬挂一滴溶液,说明氢氧化钠的体积偏大,导致待测液浓度偏大;E项未用标准液润洗碱式滴定管,导致标准液浓度偏小,需要的体积变大,使待测液浓度变大。

 考前必练系列答案
考前必练系列答案科目:高中化学 来源:不详 题型:单选题
| A.SO2、O2、N2 | B.HCl、Cl2、CO2 | C.CH4、H2、CO | D.SO2、Cl2、O2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

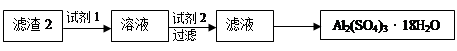
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
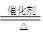 4NO+6H2O。请从下图中选用所需的仪器(可重复使用)组成一套进行该反应的简单装置。现提供试剂:过氧化钠、碱石灰、铂粉、氯化钙、浓硫酸、浓氨水和氢氧化钠溶液。
4NO+6H2O。请从下图中选用所需的仪器(可重复使用)组成一套进行该反应的简单装置。现提供试剂:过氧化钠、碱石灰、铂粉、氯化钙、浓硫酸、浓氨水和氢氧化钠溶液。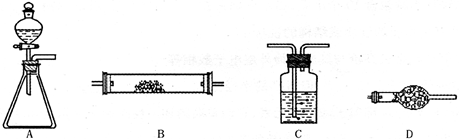
| 选用的仪器(填字母) | 加入的试剂 | 作用 |
| | | |
| | | |
| | | |
| | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
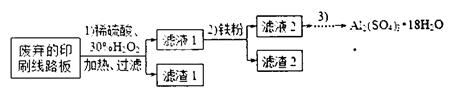
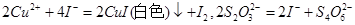
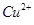 含量将会 (填“偏高”、“偏
含量将会 (填“偏高”、“偏
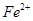 除去。下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mo1.L-1计算)。
除去。下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为1.0mo1.L-1计算)。| | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| A13+ | 3.8 | 5.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com