
| A.SO2、O2、N2 | B.HCl、Cl2、CO2 | C.CH4、H2、CO | D.SO2、Cl2、O2 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
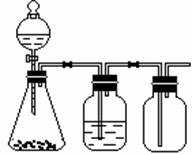
| 选项 | 制气装置 | 洗气瓶中试剂 | 瓶中气体 |
| A | 氯酸钾 MnO2 | 浓硫酸 | O2 |
| B | 石灰石 稀盐酸 | NaHCO3溶液 | CO2 |
| C | Zn 稀硫酸 | 浓硫酸 | H2 |
| D | MnO2 浓盐酸 | 浓硫酸 | Cl2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
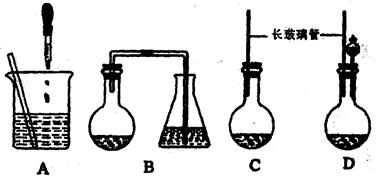
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.称取该晶体28.6 g溶于1 L水中 |
| B.称取10.6 g该晶体,溶于水制成1 L溶液 |
| C.将该晶体加热除去结晶水,称取10.6 g溶于水中制成1 L溶液 |
| D.称取该晶体28.6 g溶于水中制成1 L溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):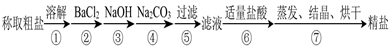
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| | NaOH起始读数 | NaOH终点读数 |
| 第一次 | 0.10mL | 18.50mL |
| 第二次 | 0.20mL | 18.80mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com