
【题目】某晶体 M·nH2O溶于水后,溶液温度降低。而 M(s)溶于水后,溶液温度升高,可将变化过程表示为图。下列说法中错误的是( )
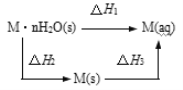
A.△H1=△H2+△H3
B.M(s)溶于水形成溶液△S>0
C.△H2>△H3
D.△H1+△H3>△H2
【答案】D
【解析】
A.根据盖斯定律可知,总反应的热效应等于各分步反应的热效应之和,因此△H1=△H2+△H3,故A正确;
B.M(s)溶于水形成溶液,混乱度增大,熵变增大,△S>0,故B正确;
C.M(s)溶于水后,溶液温度升高,△H3<0,晶体 MnH2O 溶于水后,溶液温度降低,△H1>0,根据盖斯定律可知,△H1=△H2+△H3,△H2=△H1△H3>0,所以△H2>△H3,故C正确;
D.根据盖斯定律可知,总反应的热效应等于各分步反应的热效应之和,因此△H1=△H2+△H3,故△H1+△H3=△H2+2△H3;M(s)溶于水后,溶液温度升高,△H3<0,故△H1+△H3<△H2,故D错误;
故答案选D。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】SO2是有用的化工原料,回收利用SO2既能减少大气污染,又能充分利用资源。有学者提出利用Fe3+、Fe2+等离子的作用,在常温下将SO2氧化成SO42-而实现SO2的回收利用。某研究性学习小组设计如下方案,在实验室条件下测定转化器的脱硫效率:
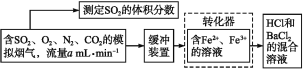
(1)写出Fe3+将SO2反应的离子方程式:__。
(2)若上述实验是在标准状况下进行的,欲测定转化器中的脱硫效率,现已测得气体流量和模拟烟气中SO2的体积分数,还需要测定的数据是___。
(3)向滴有紫色石蕊溶液的试管中通入SO2气体,现象是__;若再向其中滴入足量的氯水,现象是__,涉及反应的化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于放热反应Zn+H2SO4===ZnSO4+H2↑,下列叙述正确的是( )
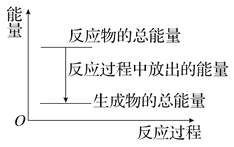
A. 反应过程中的能量关系可用上图表示
B. 1 mol Zn的能量大于1 mol H2的能量
C. 若将其设计为原电池,则锌作正极
D. 若将其设计为原电池,当有32.5 g Zn溶解时,正极放出的气体一定为11.2 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液可能含有Al3+、NH4+、Fe2+、Na+、CO32-、SO42-、Cl-、NO3-中的若干种,若在该溶液中逐滴加入稀盐酸至过量,无明显现象,并得到X溶液,对X溶液进行如下实验,下列结论正确的是( )(忽略水的电离,且原溶液中各离子浓度均为0.5mol/L)
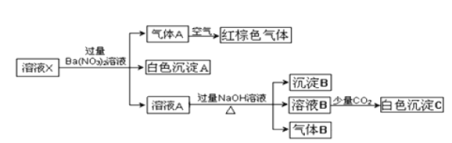
A.原溶液中一定存在NH4+、Fe2+、SO42-B.原溶液中可能合有NO3-和Al3+
C.白色沉淀C可能是![]() D.沉淀B可能是Fe(OH)2和Fe(OH)3的混合物
D.沉淀B可能是Fe(OH)2和Fe(OH)3的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以稀硫酸为电解质溶液,利用太阳能将CO2转化为低碳烯烃,工作原理图如下。下列说法正确的是
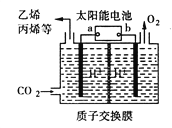
A. a电极为太阳能电池的正极
B. 产生丙烯的电极反应式为:3CO2+18H++18e-===CH3CH=CH2+6H2O
C. 装置中每转移2e-,理论上有2molH+通过质子交换膜从左向右扩散
D. 太阳能电池的原理与原电池的原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石墨电极完成下列电解实验。
实验装置 | 实验现象 |
| a处试纸变蓝; b处变红,局部褪色; c处无明显变化; d处试纸变蓝 |
下列对实验现象的解释或推测不合理的是
A. a为电解池的阴极
B. b处有氯气生成,且与水反应生成了盐酸和次氯酸
C. c处发生了反应:Fe-3e- = Fe3+
D. d处:2H2O+2e-=H2↑+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铵明矾[NH4Al(SO4)2·12H2O]是分析化学常用的基准试剂,其制备过程如图所示。下列分析不正确的是( )
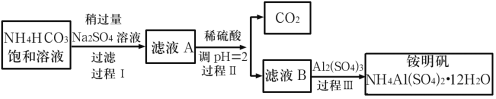
A.过程Ⅰ发生的反应:2NH4HCO3+Na2SO4=2NaHCO3↓+(NH4)2SO4
B.向铵明矾溶液中逐滴加入NaOH溶液,先后观察到:刺激性气体逸出→白色沉淀生成→白色沉淀消失
C.检验溶液B中阴离子的试剂仅需BaCl2溶液
D.若省略过程Ⅱ,则铵明矾的产率明显降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】叠氮化钠(NaN3)是易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,常用作汽车安全气囊中的药剂。实验室制取叠氮化钠的原理、实验装置及实验步骤如下:
①关闭止水夹K2,打开止水夹K1,开始制取氨气。
②加热装置A中的金属钠,使其熔化并充分反应后,停止通入氨气并关闭止水夹K1。
③向装置A中的b容器内充入加热介质,并加热到210~220℃,然后打开止水夹K2,制取并通入N2O。
请回答下列问题:
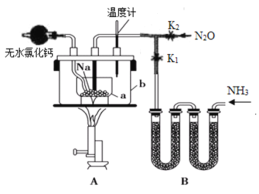
(1)制取氨气可选择的装置是__(填序号,下同),N2O可由NH4NO3在240~245℃分解制得(硝酸铵的熔点为169.6℃),则可选择的气体发生装置是__。
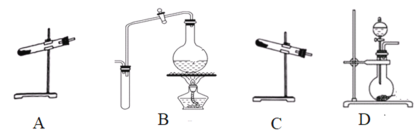
(2)步骤①中先通氨气的目的是__,步骤②氨气与熔化的钠反应生成NaNH2的化学方程式为__,步骤③中最适宜的加热方式为___。
(3)生成NaN3的化学方程式为___。
(4)反应完全结束后,进行以下操作,得到NaN3固体:
a中混合物![]() NaN3固体
NaN3固体
已知NaNH2能与水反应生成NaOH和氨气。操作Ⅱ的目的是___,操作Ⅳ最好选用的试剂是___。
(5)实验室用滴定法测定叠氮化钠样品中NaN3的质量分数:①将2.500g试样配成500.00mL溶液。②取50.00mL溶液置于锥形瓶中,加入50.00mL0.1010mol·L-1(NH4)2Ce(NO3)6溶液。③充分反应后,将溶液稍稀释,向溶液中加入8mL浓硫酸,滴入3滴邻菲啰啉指示剂,用0.0500mol·L-1(NH4)2Fe(SO4)2标准溶液滴定过量的Ce4+,消耗溶液体积为29.00mL。测定过程的反应方程式为:2(NH4)2Ce(NO3)6+2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑、Ce4++Fe2+=Ce3++Fe3+,试样中NaN3的质量分数为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第ⅤA族元素的原子R与Cl原子结合形成RCl3气态分子,其立体结构呈三角锥形。RCl5在气态和液态时,分子结构如图所示,下列关于RCl5分子的说法中不正确的是( )
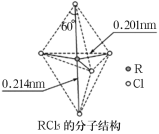
A.每个原子都达到8电子稳定结构
B.键角(Cl—R—Cl)有90°、120°、180°三种
C.RCl5受热后会分解生成分子立体结构呈三角锥形的RCl3
D.分子中5个R—Cl键键能不都相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com