解答:解:(1)①氯气和水反应生成盐酸和次氯酸,该反应为可逆反应,离子反应方程式为:Cl
2+H
2O?H
++Cl
-+HClO,故答案为:Cl
2+H
2O?H
++Cl
-+HClO;
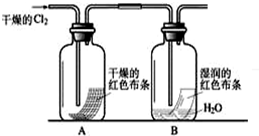
②干燥的氯气不能使干燥的有色布条褪色,干燥的氯气能使湿润的有色褪色,氯气溶于水得到氯水,说明氯水能使有色布条褪色,则起漂白作用的物质是氯水;
氯气有毒,不能直接排空,所以为防止氯气污染空气,最后要有尾气处理装置,
故答案为:干燥的氯气没有漂白性,氯水有漂白性;尾气吸收装置;
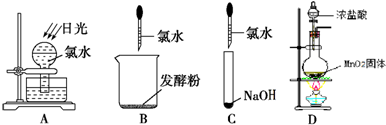
(2)①A.次氯酸不稳定,光照条件下,次氯酸易分解生成盐酸和氧气,所以有气体生成,故不选;
B.发酵粉的主要成分是碳酸氢钠,碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,所以有气体生成,故不选;
C.氢氧化钠和盐酸或次氯酸都生成可溶性的盐和水,所以没有气体生成,故选;
D.浓盐酸和二氧化锰在加热条件下能反应生成黄绿色气体氯气,所以有气体生成,故不选;
故选C;
②在加热条件下,浓盐酸和二氧化锰反应生成氯化锰、氯气和水,反应方程式为:MnO
2+4HCl(浓)
MnCl
2+Cl
2↑+2H
2O,故答案为:MnO
2+4HCl(浓)
MnCl
2+Cl
2↑+2H
2O;
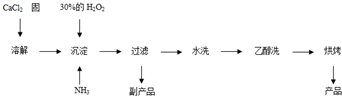
(3)①碘化钾中碘离子不稳定,易被空气中氧气氧化生成碘单质,碘单质易升华导致碘化钾中碘的损失率高,故答案为:碘化钾容易在空气中被氧化成单质碘,单质碘易升华;
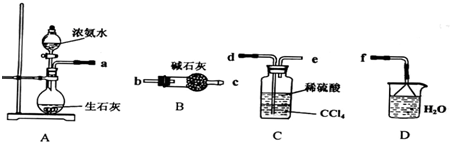
②A.酒精和水互溶,所以不能用酒精作萃取剂,故错误;
B.四氯化碳和水不互溶,和碘不反应,且碘在四氯化碳中的溶解度大于在水中的溶解度,所以四氯化碳能作萃取剂,故正确;
C.醋酸和水互溶,所以不能用醋酸作萃取剂,故错误;
D.硝酸银溶液和碘离子反应,且水和硝酸银溶液互溶,所以不能用硝酸银溶液作萃取剂,故错误;
故选B;
③酸性条件下,碘化钾和碘酸钾反应生成单质碘,碘遇淀粉试液变蓝色,所以反应现象为:溶液由无色变蓝色,故答案为:溶液变蓝色.