
【题目】在容积为2L的密闭容器中进行如下反应:A(g)+2B(g)![]() 3C(g)+nD(g),开始时A为4mol,B为6mol,5min末达到平衡,此时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol·L-1·min-1。
3C(g)+nD(g),开始时A为4mol,B为6mol,5min末达到平衡,此时测得C的物质的量为3mol,用D表示的化学反应速率v(D)为0.2mol·L-1·min-1。
计算:
(1)平衡时A的物质的量浓度为___。
(2)前5min内用B表示的化学反应速率v(B)为___。
(3)化学方程式中n值为__。
(4)此反应在四种不同情况下的反应速率分别为:
①v(A)=5mol·L-1·min-1
②v(B)=6mol·L-1·min-1
③v(C)=4.5mol·L-1·min-1
④v(D)=8mol·L-1·min-1
其中反应速率最快的是__(填编号)。
【答案】1.5mol·L-1 0.2mol·L-1·min-1 2 ①
【解析】
5min末时测得C的物质的量为3mol,v(C)=![]() =0.3mol/(Lmin),用D表示的化学反应速率v(D)为0.2mol/(Lmin),由速率之比等于化学计量数之比可知,
=0.3mol/(Lmin),用D表示的化学反应速率v(D)为0.2mol/(Lmin),由速率之比等于化学计量数之比可知,![]() =3n,解得n=2,则
=3n,解得n=2,则
A(g)+2B(g)3C(g)+2D(g),
开始(mol)4600
转化(mol)1232
5min(mol)3432
(1)根据以上分析,平衡时A的物质的量浓度为![]() =1.5 mol/L,
=1.5 mol/L,
答案为:1.5 mol/L;
(2)前5min内用B表示的化学反应速率v(B)为![]() =0.2mol/(Lmin),
=0.2mol/(Lmin),
故答案为:0.2mol/(Lmin);
(3)由上述分析可知,化学方程式中n值为2,
故答案为:2;
(4)反应速率与化学计量数的比值越大,反应速率越快,则
①由v(A)=5mol/(Lmin),![]() =5;
=5;
②由v(B)=6mol/(Lmin),![]() =3;
=3;
③由v(C)=4.5mol/(Lmin),![]() =1.5;
=1.5;
④由v(D)=8mol/(Lmin),![]() =4;
=4;
显然只有①中比值最大,反应速率最快,
故答案为:①。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
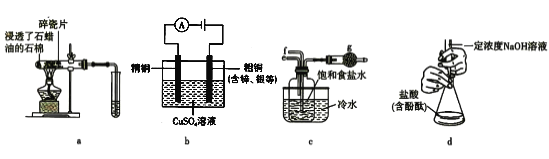
A.图a所示实验中,石蜡油发生分解反应,碎瓷片作催化剂
B.用图b所示装置精炼铜,电解过程中CuSO4溶液的浓度保持不变
C.用图c所示装置制备碳酸氢钠固体时,从e口通入NH3,再从f口通入CO2,g中盛放蘸有稀硫酸的脱脂棉
D.测定某盐酸的物质的量浓度所用图d所示装置中滴定管选择错误
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全球碳计划组织(GCP,The Global Carbon Project)报告称,2018年全球碳排放量约371亿吨,达到历史新高。
(1)中科院设计了一种新型的多功能复合催化剂,实现了CO2直接加氢制取高辛烷值汽油,其过程如图1所示。
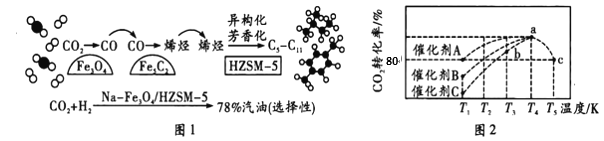
①已知:CO2(g)+H2(g)=CO(g)+H2O(g) △H= + 41 kJ·mol-1
2CO2(g)+6H2(g)=4H2O(g)+CH2=CH2(g) △H= -128 kJ·mol-1
则上述过程中CO和H2转化为CH2=CH2的热化学方程式是_________。
②下列有关CO2转化为汽油的说法,正确的是___________________(填标号)。
A. 该过程中,CO2转化为汽油的转化率高达78%
B. 中间产物Fe5C2的生成是实现CO2转化为汽油的关键
C. 在Na-Fe3O4上发生的反应为CO2+H2=CO+H2O
D. 催化剂HZSM-5可以提高汽油中芳香烃的平衡产率
③若在一容器中充入一定量的CO2和H2,加入催化剂恰好完全反应,且产物只生成C5以上的烷烃类物质和水。则起始时CO2和H2的物质的量之比不低于_________。
(2)研究表明,CO2和H2在一定条件下可以合成甲醇。反应方程式为CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H<0。一定条件下,往2L恒容密闭容器中充入1.0molCO2和3.0molH2,在不同催化剂作用下合成甲醇,相同时间内CO2的转化率随温度变化关系如图2所示。
CH3OH(g)+H2O(g) △H<0。一定条件下,往2L恒容密闭容器中充入1.0molCO2和3.0molH2,在不同催化剂作用下合成甲醇,相同时间内CO2的转化率随温度变化关系如图2所示。
①该反应自发进行的条件是__________(填“高温”“低温”或“任意温度”)
②催化效果最佳的催化剂是__________(填“A”“B”或“C”);b点时,![]() ________
________![]() (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
③若容器容积保持不变,则不能说明该反应达到化学平衡状态的是________。
a.c(CO2)与c(H2)的比值保持不变
b.v(CO2)正=v(H2O)逆
c.体系的压强不再发生变化
d.混合气体的密度不变
e.有lmolCO2生成的同时有断开3mol的H-H键
f.气体的平均相对分子质量不变
④已知容器内的起始压强为100 kPa,若图2中c点已达到平衡状态,则该温度下反应的平衡常数Kp =____________________(只列出计算式,不要求化简,Kp为以分压表示的平衡常数,分压=总压×物质的量分数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】混合物A含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下发生如图所示的物质之间的变化:
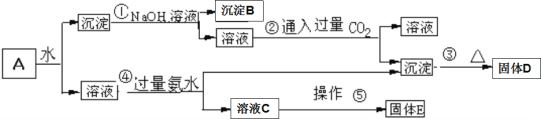
(1)固体D的化学式为___________
(2)写出反应①、④的离子方程式________________、_____________
(3)溶液C中含有的主要离子是______________________
(4)操作⑤是__________、______________________
(5)如图表示AlCl3与NaOH溶液相互滴加的两组实验过程中,微粒数量的关系曲线。判断下列说法不正确的是_____________
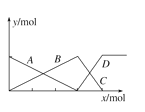
A.A线可表示Al3+或OH—的物质的量的变化
B.B C D线均可表示AlO2—的物质的量的变化
C.B C D线均可表示Al(OH)3的物质的量的变化
D.同一组实验中A、B、C、D线不可能全部出现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国某知名企业开发了具有多项专利的锂钒氧化物二次电池,其成本较低,对环境无污染,能量密度远远高于其他电池,电池总反应为V2O5+xLi![]() LixV2O5。下列说法中正确的是( )
LixV2O5。下列说法中正确的是( )
A.电池在放电时,Li+向负极移动
B.锂在放电时做正极,充电时做阳极
C.该电池充电时阳极的反应为LixV2O5-xe-=V2O5+xLi+
D.V2O5只是锂发生反应的载体,不参与电池反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 的a、b两种酸溶液各1mL,分别加水稀释到1000mL,其中pH与溶液体积V的关系如图所示。下列说法正确的是
的a、b两种酸溶液各1mL,分别加水稀释到1000mL,其中pH与溶液体积V的关系如图所示。下列说法正确的是![]()
![]()
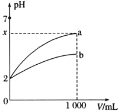
A.a、b两酸溶液的物质的量浓度一定相等
B.稀释后,a酸溶液的酸性比b酸溶液强
C.![]() 时,a是强酸,b是弱酸
时,a是强酸,b是弱酸
D.若a、b都是弱酸,则![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,在三个干燥的烧瓶内分别装有纯净的NH3,含一半空气的HCl气体, NO2 和O2的混合气体[V(NO2)∶V(O2) = 4∶1 ],然后分别作喷泉实验,三个烧瓶内所得溶液的物质的量浓度之比为
A. 2∶1∶2 B. 5∶5∶4 C. 1∶1∶1 D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3制取七水合硫酸亚铁(FeSO4·7H2O),设计流程如图:

(1)溶解烧渣选用的足量的酸的名称是___。
(2)固体1的主要成分是___。
(3)加入药品X后,溶液1中主要反应的离子方程式为___。
(4)从溶液2得到FeSO4·7H2O产品的过程中,须控制条件防止其氧化和分解,经过、___、___过滤等步骤得到晶体。
(5)有同学认为在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4·7H2O,你认为这一方案___(填写“可行”或“不可行”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物Y 能用于高性能光学树脂的合成,可由化合物X与2 甲基丙烯酰氯在一定条件下反应制得:

下列有关化合物X、Y 的说法正确的是
A. X 分子中所有原子一定在同一平面上 B. Y与Br2的加成产物分子中含有手性碳原子
C. X、Y均不能使酸性KMnO4溶液褪色 D. X→Y的反应为加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com