
【题目】把Na2O2投入FeCl2溶液中,可观察到的现象是( )
A.生成白色沉淀
B.生成红褐色沉淀
C.无气泡产生
D.无变化
科目:高中化学 来源: 题型:
【题目】下图中A是现代社会中用量最多的金属,F为红褐色沉淀。根据下图的转化关系回答下列问题:
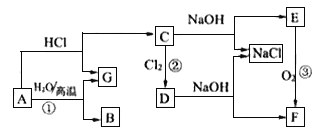
(1)写出下列物质的化学式:
C_________,E____________。
(2)分别写出反应①、反应③的化学方程式:________;________。
(3)写出反应②的离子方程式:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮元素可以形成多种物质,根据已学的知识,回答下列问题:
(1)氮原子的核外电子排布式是___________,其最外层电子有_____种不同的运动状态。
(2)氮气在常温常压下是很稳定的,对此的合理解释是____________________。
(3)N元素处于同一主族的P、As元素,这三种元素形成的气态氢化物的稳定性由大到小的顺序是________________________。
(4)工业上常用氮气与氢气来合成氨气,温度控制在400~500 ℃,采用铁触媒做催化剂,压强控制在2 ⅹ 105 ~ 5 ⅹ 105 Pa。
①该反应的化学方程式为_____________________。
它的平衡常数表达式为_______________________。
②在一体积为10 L的密闭容器中充入了280 g N2,100 g H2,反应半小时后,测得有34 g NH3生成,则用H2表示该反应的速率为_________mol/(Lmin)。此时,氮气的转化率为__________。
③下列判断可以作为该反应达到平衡的标志的是(_______)
A.单位时间内每消耗1摩尔氮气的同时消耗3摩尔氢气
B.混合气体的平均分子量不再发生变化
C.混合气体的密度保持不变
D.体系的温度不再变化
④当反应达到平衡后的t2时刻,将混合气体通过“分子筛”,可以及时将产物NH3分理出平衡体系,这会使得平衡正向移动,请根据平衡移动原理,在下图中画出t2时刻后平衡移动的示意图:_____________

⑤当及时分离出氨气后,工业上常常将氮气、氢气再次转移到反应器,这样做的原因是________________。
⑥氨气常用来生产化肥NH4Cl,NH4Cl溶于水会使得溶液显__________性,在该盐的水溶液中存在多种微粒:NH4+、NH3H2O、H+、Ci-,这些离子浓度由大到小的顺序为_________;该盐溶液中还存在多种守恒,请任意写出一种合理的守恒关系式___________________。
⑦工业上常用氨气来制备硝酸,其中第1步是用氨气与纯氧在Cr2O3的催化作用下制得NO和水。请写出这个反应的化学方程式并配平______________________。该反应中,还原剂是_________________,若反应中转移了1.204 ⅹ 1024 个电子,则生成的 NO在标准状况下的体积是________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上可利用右图所示电解装置吸收和转化SO2 (A,B均为惰性电极)。下列说法正确的是

A. B电极为电解池的阴极
B. B极区吸收5mo1 SO2,则A极区生成2.5 mo1 S2O42-
C. B极区电解液为稀硫酸,电解一段时间后硫酸浓度增大
D. A电极的电极反应为:2SO32--2e-+4H+=S2O42- + 2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于容量瓶及其使用方法的叙述正确的是
①是配制一定物质的量浓度的溶液的专用仪器 ②使用前要先检查容量瓶是否漏液 ③容量瓶可用来加热 ④不能用容量瓶长期贮存配制好的溶液 ⑤可以用500 mL容量瓶配制250 mL溶液
A. ①B. ①②④C. 除了③D. 除了⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4g NaOH溶解在10 mL水中,稀释至1 L后,再取出10 mL,这时的物质的量浓度为 ( )
A. 0.01 mol/LB. 0.1 mol/LC. 1 mol/LD. 无法精确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用纯净的碳酸钙跟稀盐酸反应制取二氧化碳气体,请回答:
(1)实验过程如右图所示,分析判断: 段化学反应速率最快, 段收集的二氧化碳最多。

(2)为了减缓上述化学反应的速率,欲向溶液中加入下列物质,你认为可行的是( )
A、蒸馏水B、NaCl固体C、NaCl溶液D、浓盐酸
(3)除了上述方法外,你认为还可以采取哪些措施来减缓化学反应速率?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于糖类的说法正确的是( )
A. 所有糖类物质都有甜味,但不一定都溶于水
B. 葡萄糖和果糖性质不同,但分子式相同
C. 摄入人体的纤维素在酶的作用下能水解为葡萄糖
D. 用浓硫酸与蛋白质的颜色反应鉴别部分蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增加。m、p、r是由这些元素组成的二元化合物。n是元素Z的单质。通常为黄绿色气体,q的水溶液具有漂白性。0.01mol/Lr溶液的![]() 为2,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是
为2,s通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是

A. 原子半径的大小W<X<Y
B. 元素的非金属性Z>X>Y
C. ![]() 的氢化物常温常压下为液态
的氢化物常温常压下为液态
D. ![]() 的最高价氧化物的水化物为强酸
的最高价氧化物的水化物为强酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com