
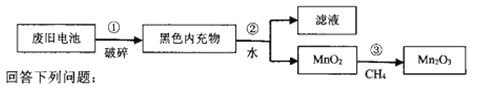
����Ŀ�����������̣�Mn2O3����������֯��ҵ��ӡȾ����Ϊ���������Դ��̽���Ͼɸɵ�صı��Ϊ������ʵ�������÷Ͼɸɵ���е�MnO2�Ʊ�Mn2O3��������ͼ��
��l������ڼ�ˮ��IJ�������Ҫ�IJ����������ձ����__�����ţ���
A�������� B����Һ©�� C����ͨ©�� D���ƾ���
��2���������ͼ�еļ�װ����������CH4����ԭMnO2�Ʊ�Mn2O3��
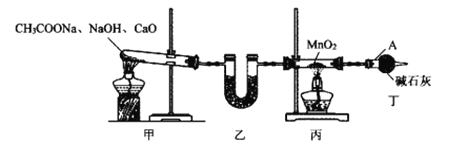
������A������Ϊ__��װ������ʢ�е��Լ�������__�����ţ���
a��Ũ���� b����ʯ�� c������ d������������
��ʵ��������ȵ�ȼ__�����������������������ľƾ��ƣ���ȼ�����ƾ���ǰ����еIJ�����___��
�۲ⶨװ�ñ�����������CO��CO2���ʵ���Ϊ1��1����÷�Ӧ�Ļ�ѧ����ʽΪ__��
�ܸ�װ�ô��ڵ�ȱ��Ϊ__��
��3��ʵ�������������ȴ��ȡװ�ñ��ڴֲ�ƷΪ7.19g��ʹ֮�����������ữ��KI��Һ��Ӧ���ֲ�Ʒ�е�Mn2O3��MnO2����Ԫ�ؾ�ת��ΪMn2+�������û��Һϡ����500mL��Ȼ��ȡ25.00mLϡ�ͺ����Һ����0.200molL-1��Na2S2O3������Һ�ζ����ﵽ�ζ��յ�ʱ������Na2S2O3����ҺΪ25.00mL������֪��I2+2Na2S2O3�TNa2S4O6+2NaI��
�ٸõζ������п���ѡ��__��ָʾ����
�����ζ�ǰ�ζ����������ݣ��ﵽ�ζ��յ�ʱ�����촦�����ݣ���ⶨ�ı�Һ�����__������ƫ��������ƫС��������Ӱ��������
�۴ֲ�Ʒ��Mn2O3�Ĵ���Ϊ__%��������С�����1λ��
���𰸡�C ���θ���� bd �� �������Ĵ��� 2CH4+14MnO2![]() 7Mn2O3+CO+CO2+4H2O ȱ��CO��β������ ���� ƫС 87.9
7Mn2O3+CO+CO2+4H2O ȱ��CO��β������ ���� ƫС 87.9
��������
�÷Ͼɸɵ���е�MnO2�Ʊ�Mn2O3�������̿�֪���ٷ�������ܽ���˷����MnO2������CH4��ԭMnO2�Ʊ�Mn2O3����ӦΪ2CH4+14MnO2![]() 7Mn2O3+CO+CO2+4H2O���Դ˽��1������2����
7Mn2O3+CO+CO2+4H2O���Դ˽��1������2����
(3)����Mn2O3+2I-+6H+=2Mn2++I2+3H2O��MnO2+2I-+4H+=Mn2++I2+2H2O��I2+2Na2S2O3�TNa2S4O6+2NaI���ҵ�������������Դ������
(l)����ڼ�ˮ��IJ���Ϊ���ˣ���Ҫ�IJ����������ձ������ͨ©����
(2)������A������Ϊ���θ���ܣ�װ������ʢ�е��Լ������Ǽ�ʯ�һ����������ף��ɸ���������壻
�����鲻������������ը����ʵ��������ȵ�ȼ�״��ľƾ��ƣ���ȼ�����ƾ���ǰ����еIJ����Ǽ������Ĵ��ȣ�
���ⶨװ�ñ�����������CO��CO2���ʵ���Ϊ1��1����÷�Ӧ�Ļ�ѧ����ʽΪ2CH4+14MnO2![]() 7Mn2O3+CO+CO2+4H2O��
7Mn2O3+CO+CO2+4H2O��
����װ�ô��ڵ�ȱ��Ϊȱ��CO��β��������
(3)�ٸõζ������п���ѡ�õ�����ָʾ����
�����ζ�ǰ�ζ����������ݣ��ﵽ�ζ��յ�ʱ�����촦�����ݣ����ı���Һ�����ȡƫС������I2+2Na2S2O3�TNa2S4O6+2NaI��֪���ɵ�Ϊ0.025L��0.2mol/L��![]() =0.05mol����7.19g������Mn2O3���ʵ���Ϊx��MnO2���ʵ���Ϊy����Mn2O3+2I-+6H+=2Mn2++I2+3H2O��MnO2+2I-+4H+=Mn2++I2+2H2O����֪
=0.05mol����7.19g������Mn2O3���ʵ���Ϊx��MnO2���ʵ���Ϊy����Mn2O3+2I-+6H+=2Mn2++I2+3H2O��MnO2+2I-+4H+=Mn2++I2+2H2O����֪![]() �����x=0.04mol��y=0.01mol����ֲ�Ʒ��Mn2O3�Ĵ���Ϊ
�����x=0.04mol��y=0.01mol����ֲ�Ʒ��Mn2O3�Ĵ���Ϊ![]() ��100%=87.9%��
��100%=87.9%��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����![]() ��ȡ
��ȡ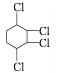 ,��ϳ�·����ͼ��ʾ:
,��ϳ�·����ͼ��ʾ:
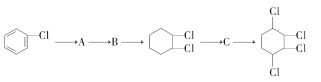
��ش���������:
(1)��������������дÿ�������ķ�Ӧ����:_________(����ĸ)��
a.ȡ����Ӧ b.�ӳɷ�Ӧ c.��ȥ��Ӧ
(2)д��A��B������Լ��ͷ�Ӧ����:_______��
(3)� C![]()
 �Ļ�ѧ����ʽ:_____________��
�Ļ�ѧ����ʽ:_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ѥ����ʵ������ϵ�Ӧ���������˹Ŵ��滭�Ͳ��յĻԻ͡�����(CdS)��һ��������ˮ�Ļ�ɫ���ϣ���ˮ�д��ڳ����ܽ�ƽ�⣺CdS(s)![]() Cd2+(aq)+S2-(aq)�����ܶȻ�Ksp=c(Cd2+)��c(S2-)������ˮ�еij����ܽ�ƽ��������ͼ��ʾ��T2��T1��������˵��������ǣ� ��
Cd2+(aq)+S2-(aq)�����ܶȻ�Ksp=c(Cd2+)��c(S2-)������ˮ�еij����ܽ�ƽ��������ͼ��ʾ��T2��T1��������˵��������ǣ� ��

A.ͼ��a��b�ֱ�ΪT1��T2�¶���CdS��ˮ�е��ܽ��
B.ͼ�и����Ӧ��Ksp�Ĺ�ϵΪ��Ksp(m)=Ksp(n)<Ksp(p)<Ksp(q)
C.��m�����Һ�м�������Na2S���壬��Һ�����m��mpn����p�����ƶ�
D.�¶Ƚ���ʱ��q��ı�����Һ�������q��qp����p�����ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��HCHO��O2���ǻ���ʯ��HAP�����淴Ӧͨ��������Ӧ����CO2��H2O�Ļ�����ͼ��ʾ��ͼ��ֻ������HAP�IJ��ֽṹ��������˵��������ǣ� ��
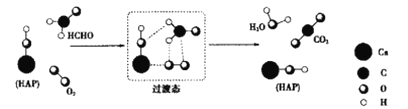
A.HCHO�ڷ�Ӧ�����У�����C-H������������
B.��Ӧ��һ�������ȹ���
C.����H2O�е�Oȫ��������O2
D.HAP�Ǹ÷�Ӧ�Ĵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Zn��OH��2��ZnS�ֱ�Ϊ��ɫ������ɫ����������ܽ�Ⱦ����¶����߶�����ij�¶��£�Ksp[Zn��OH��2]=1.0��10-18�������ʵ���Ũ����ͬ��NaOH��Na2S�Ļ����Һ�еμ�ZnSO4��Һ����Һ�������ӡ�������Ũ�ȹ�ϵ��ͼ��ʾ��ͼ��p��Zn��=-lgc��Zn2+����p��B��=-lgc��OH-����-1gc��S2-��������˵��������ǣ� ��
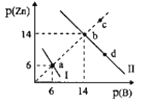
A.����l��ʾ����Zn2+��OH-Ũ�ȹ�ϵ������
B.���¶��£�Ksp��ZnS��=1.0��10-28
C.�����¶�ʱ��b��һ������c���ƶ�
D.��֪���¶���Ka2��H2S���T4.0��10-16����0.01molL-lNaHS��Һ�еμӵ����0.2molL-1ZnSO4��Һ���ܲ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(2017������)��ѹ���ʻ�������������ԭ��Ϊ��Ni(s)+4CO(g)![]() Ni(CO)4(g)��230��ʱ���÷�Ӧ��ƽ�ⳣ��K=2��105����֪��Ni(CO)4�ķе�Ϊ42.2�����������ʲ����뷴Ӧ��
Ni(CO)4(g)��230��ʱ���÷�Ӧ��ƽ�ⳣ��K=2��105����֪��Ni(CO)4�ķе�Ϊ42.2�����������ʲ����뷴Ӧ��
��һ�Σ���������CO��Ӧת������̬Ni(CO)4��
�ڶ��Σ�����һ�η�Ӧ���������������������230���Ƶøߴ�����
�����ж���ȷ����
A. ����c(CO)��ƽ���������ƶ�����Ӧ��ƽ�ⳣ������
B. �ڶ��Σ�Ni(CO)4�ֽ��ʽϵ�
C. ��һ�Σ���30����50������֮��ѡ��Ӧ�¶ȣ�ѡ50��
D. �÷�Ӧ�ﵽƽ��ʱ��v����[Ni(CO)4]=4v����(CO)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ 25����ʱ��NH3��H2O kb=1.77��10-5��H2CO3 ka1=4.30��10-7��ka2=5.61��10-11�� 25��ʱ�й�NH4HCO3��Һ��˵������ȷ����
A. ��������
B. c(OH-)+c(NH3��H2O)=c(H+)+c(H2CO3)
C. ����NaOH ��Һ������Ӧ:NH4++OH-=NH3��H2O��HCO3-+OH-=H2O+CO32-
D. ����NaOH��Һ����![]() ����
����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E��F��G Ϊ����������Ԫ�أ���ԭ�Ӱ뾶�������������Ĺ�ϵ��ͼ������˵����ȷ����
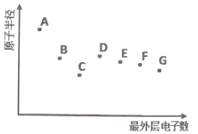
A.����Ԫ��B ��Ԫ�����ڱ��е�λ���Ʋ⣬������������Ӧ��ˮ������ܾ�������
B.Ԫ��D����Ȼ������Ҫ������̬���ڣ��䵥�ʿ������뵼�����
C.Ԫ��A�����Ӱ뾶����Ԫ��G�����Ӱ뾶
D.Ԫ��F ����̬�⻯���Ԫ��G����̬�⻯����ȶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����4 mol A�����2 mol B������2 L�������л�ϲ���һ�������·������·�Ӧ��2A������+B������![]() 2C������������2 s���룩����C��Ũ��Ϊ0.6 mol��L��1���������м���˵����
2C������������2 s���룩����C��Ũ��Ϊ0.6 mol��L��1���������м���˵����
��������A��ʾ�ķ�Ӧƽ������Ϊ0.3 mol��L��1��s��1
��������B��ʾ�ķ�Ӧ��ƽ������Ϊ0.6 mol��L��1��s��1
��2sʱ����A��ת����Ϊ70%
��2sʱ����B��Ũ��Ϊ0.7 mol��L��1
������ȷ���ǣ�
A.�٢�B.�٢�C.�ڢ�D.�ۢ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com