
【题目】Zn(OH)2、ZnS分别为白色、淡黄色难溶物,二者溶解度均随温度升高而增大。某温度下,Ksp[Zn(OH)2]=1.0×10-18。向物质的量浓度相同的NaOH和Na2S的混合溶液中滴加ZnSO4溶液,溶液中阳离子、阴离子浓度关系如图所示。图中p(Zn)=-lgc(Zn2+),p(B)=-lgc(OH-)或-1gc(S2-)。下列说法错误的是( )
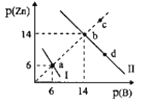
A.曲线l表示的是Zn2+与OH-浓度关系的曲线
B.该温度下,Ksp(ZnS)=1.0×10-28
C.升高温度时,b点一定会向c点移动
D.已知此温度下Ka2(H2S)═4.0×10-16,向0.01molL-lNaHS溶液中滴加等体积0.2molL-1ZnSO4溶液不能产生沉淀
【答案】CD
【解析】
A. 若曲线I表示的是Zn2+与OH-浓度关系的曲线,则a点时c(Zn2+)=c(OH-)=10-6mol/L,Ksp[Zn(OH)2]=10-6×(10-6)2=1.0×10-18,所以假设成立,即曲线表示的是Zn2+与OH-浓度关系的曲线,故A正确;
B.曲线I表示的是Zn2+与OH-浓度关系的曲线,则曲线II表示的是Zn2+与S2-浓度关系的曲线,b点时c(Zn2+)=c(S2-)=10-14mol/L,Ksp(ZnS)=c(Zn2+)c(S2-)=10-14×10-14=1.0×10-28,故B正确;
C.曲线II表示的是Zn2+与S2-浓度关系的曲线,ZnS溶解吸热,升高温度时溶液中c(Zn2+)、c(S2-)增大,则p(Zn)、p(B)减小,即升高温度时,b点一定会沿着ba方向向a点移动,故C错误;
D.等体积混合瞬间,NaHS浓度为0.005molL-l、ZnSO4浓度为0.1molL-1,c(S2-)=![]() mol/L=1.4×10-9mol/L,浓度熵Qc=c(Zn2+)c(S2-)=1.4×10-9×0.1=1.4×10-10mol>1.0×10-28=Ksp(ZnS),所以产生ZnS沉淀,故D错误;
mol/L=1.4×10-9mol/L,浓度熵Qc=c(Zn2+)c(S2-)=1.4×10-9×0.1=1.4×10-10mol>1.0×10-28=Ksp(ZnS),所以产生ZnS沉淀,故D错误;
答案选CD。


科目:高中化学 来源: 题型:
【题目】工业上由乙苯生产苯乙烯的反应如下,下列有关说法正确的是 ( )
 +H2
+H2
A.该反应的类型为取代反应
B.苯乙烯分子中所有原子一定在同一平面上
C.乙苯和苯乙烯都能发生氧化反应
D.比乙苯多一个碳原子的同系物R的同分异构体(包含R,不含立体异构)共有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的某磁黄铁矿(主要成分FexS,S为-2价)与100mL盐酸恰好完全反应(矿石中其他成分不与盐酸反应),生成3.2g硫单质、0.4molFeCl2和一定量H2S气体,且溶液中无Fe3+。则下列说法正确的是( )
A.该盐酸的物质的量浓度为4.0mol·L-1
B.该磁黄铁矿FexS中,Fe2+与Fe3+的物质的量之比为2:1
C.生成的H2S气体在标准状况下的体积为8.96L
D.该磁黄铁矿中FexS的x=0.85
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:焦性没食子酸的碱性溶液可吸收O2。碘化亚铁(FeI2)在常温下为灰黑色固体,易升华,可溶于水,具有潮解性。实验室用如图装置制备FeI2。下列说法错误的是( )
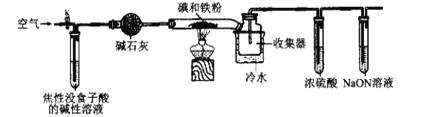
A.空气的主要作用是将产生的FeI2吹入收集器中
B.冷水的作用是将升华的FeI2凝华便于收集,使用粗玻璃管可以防止堵塞
C.浓硫酸的作用是防止水蒸气进入收集器而引起FeI2潮解
D.向FeI2溶液中通入等物质的量的Cl2,反应的离子方程式为:2Fe2++2Cl2=2Fe3++4Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解法利用 CO2制备甲酸盐可实现 CO2资源化利用, 其装置如图所示:

下列说法错误的是
A.a 极为正极,K+由左向右通过交换膜
B.乙池中的反应为 CO2+HCO3-+2e-= HCOO-+ CO32-
C.电解过程中,Pt 电极产生的气体可以用作燃料电池的负极反应
D.两池的溶液 KHCO3浓度均降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氧化二锰(Mn2O3)可用作纺织行业的印染剂。为充分利用资源,探究废旧干电池的变废为宝,在实验室中用废旧干电池中的MnO2制备Mn2O3,流程如图:
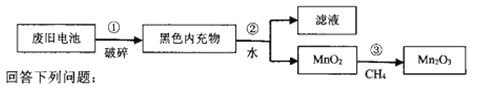
(l)步骤②加水后的操作,需要的玻璃仪器除烧杯外还需__(填标号)。
A.玻璃棒 B.分液漏斗 C.普通漏斗 D.酒精灯
(2)步骤③用图中的甲装置所产生的CH4,还原MnO2制备Mn2O3。
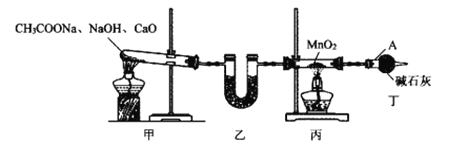
①仪器A的名称为__,装置乙内盛有的试剂可以是__(填标号)。
a.浓硫酸 b.碱石灰 c.胆矾 d.五氧化二磷
②实验过程中先点燃__(填“甲”或“丙”)处的酒精灯,点燃丙处酒精灯前需进行的操作是___。
③测定装置丙内生成物中CO、CO2物质的量为1:1,则该反应的化学方程式为__。
④该装置存在的缺陷为__。
(3)实验结束,仪器冷却后,称取装置丙内粗产品为7.19g,使之与足量硫酸酸化的KI溶液反应(粗产品中的Mn2O3和MnO2的锰元素均转化为Mn2+),将该混合液稀释至500mL,然后取25.00mL稀释后的溶液,用0.200molL-1的Na2S2O3;标准溶液滴定,达到滴定终点时,消耗Na2S2O3标准溶液为25.00mL。(已知:I2+2Na2S2O3═Na2S4O6+2NaI)
①该滴定过程中可以选用__作指示剂。
②若滴定前滴定管内无气泡,达到滴定终点时,尖嘴处有气泡,则测定的标准液的体积__(填“偏大”、“偏小”或“无影响”)。
③粗产品中Mn2O3的纯度为__%。(保留小数点后1位)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】示意图甲为锌铜原电池装置,乙为电解熔融氯化钠制备金属钠的装置。 下列说法正确的是
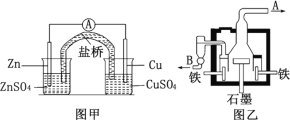
A.甲装置中锌为负极,发生还原反应;铜为正极,发生氧化反应
B.甲装置盐桥可以使反应过程中溶液保持电中性
C.乙装置中铁极的电极反应式为:2Na-2e- = 2Na+
D.乙装置中 B 是氯气出口,A 是钠出口
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美托洛尔是一种能降低血压,治疗心律不齐的药物,其一种合成路线如图所示:
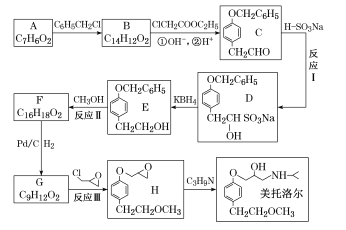
回答下列问题:
(I)A官能团的名称是____,B的结构简式为___________。
(2)反应I的反应类型是____,反应Ⅱ的反应条件是__________。
(3)反应Ⅲ的化学方程式为__________。
(4)化合物H的芳香族类同分异构体K,其性质如下:
①能发生水解反应
②核磁共振氢谱有4组峰.峰面积之比为9:3:2:2
写出一种符合要求的K的结构简式:_________________。
(5)已知:
设计由对氯苯甲醛![]() 为原料制备
为原料制备![]() 的合成路线____。(无机试剂和反应条件所需有机试剂任选,标清反应条件)
的合成路线____。(无机试剂和反应条件所需有机试剂任选,标清反应条件)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知①2C(s)+O2(g)=2CO(g) ΔH=-221.0 kJ·mol-1
②2H2(g)+O2(g) =2H2O(g) ΔH=-483.6 kJ·mol-1
则制备水煤气的反应C(s)+H2O(g) =CO(g)+H2(g) ΔH为( )
A.+262.6 kJ·mol-1B.-131.3 kJ·mol-1
C.-352.3 kJ·mol-1D.+131.3 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com