
【题目】工业上由乙苯生产苯乙烯的反应如下,下列有关说法正确的是 ( )
 +H2
+H2
A.该反应的类型为取代反应
B.苯乙烯分子中所有原子一定在同一平面上
C.乙苯和苯乙烯都能发生氧化反应
D.比乙苯多一个碳原子的同系物R的同分异构体(包含R,不含立体异构)共有4种
【答案】C
【解析】
A. 该反应的类型为消去反应,故A错误;
B.苯是一个平面,乙烯是一个平面,碳碳单键可以旋转,因此苯乙烯分子中所有原子不一定在同一平面上,故B错误;
C. 乙苯和苯乙烯都能燃烧且都能使酸性高锰酸钾溶液褪色,即能发生氧化反应,故C正确;
D. 比乙苯多一个碳原子的同系物R,即苯环外还有3个碳原子,第一种情况三个碳在一起有两种同分异构,第二种情况三个碳分为一个甲基,一个乙基,有邻、间、对三种,第三种情况三个碳分为三个甲基,两个甲基在邻、间、对三种位置,另一个甲基分别放入分别有两种、三种、一种,因此同分异构体(包含R,不含立体异构)共有11种,故D错误。
综上所述,答案为C。


科目:高中化学 来源: 题型:
【题目】化合物 YX2、ZX2 中,X、Y、Z 的核电荷数小于 18;X 原子最外能层的 p 能级中有一个轨道充填了 2 个电子,Y 原子的最外层中 p 能级的电子数等于前一能层电子总数,且X 和 Y 具有相同的电子层数;Z 与 X 在周期表中位于同一主族。回答下列问题:
(1)X 的电子排布式为______________,Y 的价电子轨道表示式为_______。
(2)ZX2 的分子式是_______,YX2 电子式是_______ 。
(3)Z 形成的简单阴离子的结构示意图是___________。
(4) Y 和 Z 一定条件下形成简单分子的结构式是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明,大气中氮氧化物和碳氢化合物受紫外线作用可产生二次污染物——光化学烟雾,其中某些反应过程如图所示。下列说法不正确的是

A. 整个过程中O3作催化剂
B. 反应III的方程式为O2+O===O3
C. 光化学烟雾中含甲醛、乙醛等刺激性物质
D. 反应I、反应Ⅱ均属于氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种胃药的止酸剂为碳酸钙,测定每片中碳酸钙含量的方法有以下几步操作(设药片中的其它成分不与盐酸反应,也不与氢氧化钠反应),实验步骤如下:
①配制![]() 稀盐酸和
稀盐酸和![]() 溶液各
溶液各![]()
②取一粒药片(![]() )研碎后加入
)研碎后加入![]() 蒸馏水
蒸馏水
③加入![]() 稀盐酸
稀盐酸
④用![]() 溶液中和过量盐酸,用去体积为
溶液中和过量盐酸,用去体积为![]() 。
。
请回答下列问题:
(1)测定过程中发生反应的离子方程式_________。
(2)配制上述![]() 稀盐酸所用玻璃仪器有量筒、烧杯、________。
稀盐酸所用玻璃仪器有量筒、烧杯、________。
(3)如果选用酚酞作指示剂,滴定达到终点的现象为____。
(4)某同学四次测定的![]() 数据如下:
数据如下:
测定次序 | 第一次 | 第二次 | 第三次 | 第四次 |
| 13.40 | 11.90 | 12.10 | 12.00 |
请根据这位同学的实验数据,计算药片中碳酸钙的质量分数为_____。
(5)若在实验过程中存在下列操作,会使所测碳酸钙的质量分数偏高的是_________。
a 用没有润洗的碱式滴定管装![]() 溶液进行滴定
溶液进行滴定
b 用没有润洗的酸式滴定管量取![]() 稀盐酸溶解样品
稀盐酸溶解样品
c 用![]() 溶液滴定时,开始读数平视,终点俯视
溶液滴定时,开始读数平视,终点俯视
d 装![]() 溶液的滴定管,滴定前尖嘴有气泡,滴定结束后无气泡。
溶液的滴定管,滴定前尖嘴有气泡,滴定结束后无气泡。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由![]() 制取
制取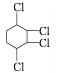 ,其合成路线如图所示:
,其合成路线如图所示:
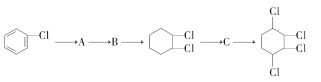
请回答下列问题:
(1)从左向右依次填写每步所属的反应类型:_________(填字母)。
a.取代反应 b.加成反应 c.消去反应
(2)写出A→B所需的试剂和反应条件:_______。
(3)写出 C![]()
 的化学方程式:_____________。
的化学方程式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
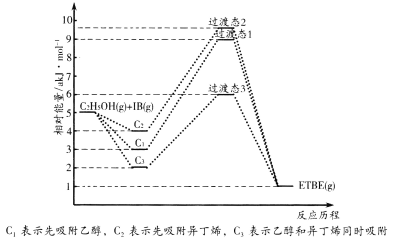
【题目】(1)乙基叔丁基醚(以ETBE表示)是一种性能优良的高辛烷值汽油调和剂。用乙醇与异丁烯(以IB表示)在催化剂HZSM-5催化下合成ETBE,反应的化学方程式为:C2H5OH(g)+IB(g)![]() ETBE(g) △H。回答下列问题:
ETBE(g) △H。回答下列问题:
反应物被催化剂HZSM-5吸附的顺序与反应历程的关系如图所示,该反应的△H=__kJ·mol-1。反应历程的最优途径是__(填C1、C2或C3)。
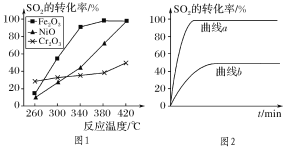
(2)一定条件下,用Fe2O3、NiO或Cr2O3作催化剂对燃煤烟气回收。反应为2CO(g)+SO2(g)![]() 2CO2(g)+S(l) ΔH=-270kJ·mol-1
2CO2(g)+S(l) ΔH=-270kJ·mol-1
①其他条件相同、催化剂不同,SO2的转化率随反应温度的变化如图1,Fe2O3和NiO作催化剂均能使SO2的转化率达到最高,不考虑催化剂价格因素,选择Fe2O3的主要优点是:__。
②某科研小组用Fe2O3作催化剂。在380℃时,分别研究了[n(CO)∶n(SO2)]为1∶1、3∶1时SO2转化率的变化情况(图2)。则图2中表示n(CO)∶n(SO2)=3∶1的变化曲线为__。
(3)已知NO2存在如下平衡:2NO2(g)![]() N2O4(g) △H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系:v(NO2)=k1·p2(NO2),v(N2O4)=k2·p(N2O4),相应的速率与其分压关系如图所示。
N2O4(g) △H<0,在一定条件下NO2与N2O4的消耗速率与各自的分压(分压=总压×物质的量分数)有如下关系:v(NO2)=k1·p2(NO2),v(N2O4)=k2·p(N2O4),相应的速率与其分压关系如图所示。

一定温度下,k1、k2与平衡常数Kp(压力平衡常数,用平衡分压代替平衡浓度计算)间的关系是k1=__;在图标出点中,指出能表示反应达到平衡状态的点是__,理由是__。
(4)二氧化硫的催化氧化是工业上生产硫酸的主要反应O2(g)+2SO2(g)![]() 2SO3(g)。
2SO3(g)。
已知:标准平衡常数Kθ=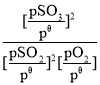 ,其中pθ为标准压强(1×105Pa),p(SO3)、p(O2)和p(SO2)为各组分的平衡分压,如p(SO3)=x(SO3)p,p为平衡总压,x(SO3)为平衡系统中SO3的物质的量分数。
,其中pθ为标准压强(1×105Pa),p(SO3)、p(O2)和p(SO2)为各组分的平衡分压,如p(SO3)=x(SO3)p,p为平衡总压,x(SO3)为平衡系统中SO3的物质的量分数。
SO2和O2起始物质的量之比为2:1,反应在恒定温度和标准压强下进行,SO3的平衡产率为ω,则Kθ=___(用含ω的最简式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定体积的密闭容器中,进行如下化学反应:2X(g)+Y(s)![]() Z(g)+W(g),若其化学平衡常数K和温度t的关系如下表
Z(g)+W(g),若其化学平衡常数K和温度t的关系如下表
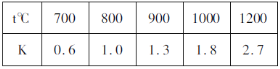
下列叙述不正确的是
A.上述反应的正反应是吸热反应
B.该反应的化学平衡常数表达式为K=![]()
C.若在1L的密闭容器中通入X和Y各0.3mol,5min后温度升高到800℃,此时测得X为0.1mol,该反应达到平衡状态
D.混合气体的密度保持不变可作为该反应达到平衡的标志之一
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Zn(OH)2、ZnS分别为白色、淡黄色难溶物,二者溶解度均随温度升高而增大。某温度下,Ksp[Zn(OH)2]=1.0×10-18。向物质的量浓度相同的NaOH和Na2S的混合溶液中滴加ZnSO4溶液,溶液中阳离子、阴离子浓度关系如图所示。图中p(Zn)=-lgc(Zn2+),p(B)=-lgc(OH-)或-1gc(S2-)。下列说法错误的是( )
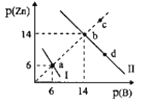
A.曲线l表示的是Zn2+与OH-浓度关系的曲线
B.该温度下,Ksp(ZnS)=1.0×10-28
C.升高温度时,b点一定会向c点移动
D.已知此温度下Ka2(H2S)═4.0×10-16,向0.01molL-lNaHS溶液中滴加等体积0.2molL-1ZnSO4溶液不能产生沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com