
(1)已知:C3H8(g)+5O2(g) ===3CO2(g)+4H2O(1) △H=-2220.0kJ/mol
H2O(1) ===H2O(g);△H=+44.0kJ/mol
写出丙烷燃烧生成CO2和气态水的热化学方程式 。
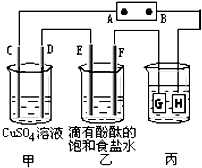
(2)在如图所示的实验装置中,E为一张用淀粉碘化钾溶液润湿的滤纸,C、D为夹在滤纸两端的铂夹,X、Y分别为直流电源的两极。在A、B中充满AgNO3溶液后倒立于盛有AgNO3溶液的水槽中,再分别插入铂电极。切断电源开关S1,闭合开关S2,通直流电一段时间后,B电极质量增重,A极产生无色气体。请回答下列问题:
① 写出D电极反应式: ;
②写出水槽中电解AgNO3溶液总反应的离子方程式: ,阴极增重2.16 g,则阳极上放出的气体在标准状况下的体积是____ _L。

(1)C3H8(g)+5O2(g)=3CO2(g)+4H2O(g) △H=-2044kJ/mol(3分)
(2)2I--2e-=I2(2分);4Ag++2H2O 4Ag+4H++O2↑(2分);0.112(2分)
4Ag+4H++O2↑(2分);0.112(2分)
【解析】
试题分析:(1)已知:①C3H8(g)+5O2(g) ===3CO2(g)+4H2O(1) △H=-2220.0kJ/mol、②H2O(1) ===H2O(g);△H=+44.0kJ/mol,则根据盖斯定律可知①+②×4即得到丙烷燃烧生成CO2和气态水的热化学方程式C3H8(g)+5O2(g)=3CO2(g)+4H2O(g),所以该反应的反应热△H=-2220.0kJ/mol+44.0kJ/mol×4=-2044kJ/mol。
(2)①切断电源开关S1,闭合开关S2,则构成电解池。通直流电一段时间后,B电极质量增重,这说明B电极是阴极,溶液中的金属阳离子放电析出金属。A极是阳极,溶液中的OH-放电产生无色气体氧气。所以Y电极是电源的负极,X是正极。则D电极是阴极,溶液中的碘离子放电生成单质碘,电极反应式为2I--2e-=I2。
②惰性电极电解硝酸银溶液生成硝酸、氧气和银,离子方程式为4Ag++2H2O 4Ag+4H++O2↑。阴极增重2.16 g,即银的质量是2.16g,物质的量是2.16g÷108g/mol=0.02mol。所以根据方程式可知,生成氧气的物质的量=0.02mol÷4=0.005mol。因此在标准状况下的体积=0.005mol×22.4L/mol=0.112L。
4Ag+4H++O2↑。阴极增重2.16 g,即银的质量是2.16g,物质的量是2.16g÷108g/mol=0.02mol。所以根据方程式可知,生成氧气的物质的量=0.02mol÷4=0.005mol。因此在标准状况下的体积=0.005mol×22.4L/mol=0.112L。
考点:考查盖斯定律的应用、电化学原理的应用、判断与计算


科目:高中化学 来源: 题型:
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 (Ⅰ)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).
(Ⅰ)北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com