
 ��֪T��X��Y��Z��Q����ѧ��ѧ����������Ԫ�أ�����T��X��Y��Z����Ϣ�����
��֪T��X��Y��Z��Q����ѧ��ѧ����������Ԫ�أ�����T��X��Y��Z����Ϣ�����| Ԫ�� | �ṹ��������Ϣ |
| T | ԭ�ӵ�L����s����������p�������� |
| X | Ԫ�ص�ԭ�Ӱ뾶�ǵ�����������Ԫ�������ģ� |
| Y | �����к��䵥�ʣ�ԭ�ӵ������δ�ɶԵ������Ǹ�Ԫ���������������ģ� |
| Z | ���ʳ��¡���ѹ�������壮ԭ�ӵ�M������1��δ�ɶԵ�p���ӣ� |
���� T��X��Y��Z����ѧ��ѧ����������Ԫ�أ�Tԭ�ӵ�L����s����������p����������Tԭ����Χ�����Ų�Ϊ2s22p2����TΪ̼Ԫ�أ�XԪ�ص�ԭ�Ӱ뾶�ǵ�����������Ԫ���������XΪNaԪ�أ������к�Y���ʣ�ԭ�ӵ������δ�ɶԵ������Ǹ�Ԫ���������������ģ���YΪ��Ԫ�أ�Zԭ�ӵ�M������1��δ�ɶԵ�p���ӣ���Χ�����Ų�Ϊ3s23p1��3s23p5���䵥�ʳ��¡���ѹ�������壬��ZΪClԪ�أ��ݴ˽��
��� �⣺T��X��Y��Z����ѧ��ѧ����������Ԫ�أ�Tԭ�ӵ�L����s����������p����������Tԭ����Χ�����Ų�Ϊ2s22p2����TΪ̼Ԫ�أ�XԪ�ص�ԭ�Ӱ뾶�ǵ�����������Ԫ���������XΪNaԪ�أ������к�Y���ʣ�ԭ�ӵ������δ�ɶԵ������Ǹ�Ԫ���������������ģ���YΪ��Ԫ�أ�Zԭ�ӵ�M������1��δ�ɶԵ�p���ӣ���Χ�����Ų�Ϊ3s23p1��3s23p5���䵥�ʳ��¡���ѹ�������壬��ZΪClԪ�أ�
��1����N2��Ϊ�ȵ����������ΪCO���ʴ�Ϊ��CO��
��2��NH3���Ӽ����γ��������HCl���Ӽ�û���������NH3�ķе��HCl�ķе㣬�ʴ�Ϊ��NH3���Ӽ����γ��������HCl���Ӽ�û�������
��3���ǽ�����Խǿ���縺��Խ�ʵ縺��N��C��Na���ʴ�Ϊ��N��C��Na��
��4��Ԫ��Q��ԭ��������Na��Cl��ԭ������֮�ͣ���Q��ԭ������Ϊ11+17=28����QΪNiԪ�أ�
��NiԪ��ԭ�ӵĺ�������Ų�ʽΪ1s22s22p63s23p63d84s2�������������Ų�Ϊ3d84s2���ʴ�Ϊ��3d84s2��
��ƽ���͵�[Ni��CN��4]2-���������[NiCl4]2-��CN-��Cԭ�Ӽ۲������Ϊ1+$\frac{4+1-3}{2}$=2��Nԭ�Ӳ�ȡsp�ӻ���[NiCl4]2-��������ṹ��Niԭ�Ӳ�ȡsp3�ӻ���
�ʴ�Ϊ��sp��sp3��
��[Ni4]2-�Ŀռ乹�ͣ������߱�ʾ�ռ乹�͵�����������ʾ��������������ԭ��֮��Ļ�ѧ��Ϊ��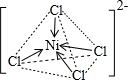 ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼��ṹ����λ�ù�ϵӦ�á�Ԫ�������ɡ���������Ų����ɡ��ӻ����ۡ������ȣ�ע����λ���ı�ʾ��������������ʵ�Ӱ�죬�Ѷ��еȣ�


 �����ҵ��ٿ���������������ϵ�д�
�����ҵ��ٿ���������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��4 | B�� | 1��3 | C�� | 1��2 | D�� | 1��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
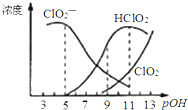 �������ƣ�NaClO2������Ư��֯���ά��ֽ�������ж���ά����С���ص㣮������Һ�п�����ClO2��HClO2��ClO2-��Cl-�ȣ�����HClO2��ClO2������Ư�����ã���֪pOH=-lgc��OH-�������ⶨ25��ʱ����ֺ�����pOH�仯�����ͼ��ʾ��Cl-û�л����������¶��£����з���������ǣ�������
�������ƣ�NaClO2������Ư��֯���ά��ֽ�������ж���ά����С���ص㣮������Һ�п�����ClO2��HClO2��ClO2-��Cl-�ȣ�����HClO2��ClO2������Ư�����ã���֪pOH=-lgc��OH-�������ⶨ25��ʱ����ֺ�����pOH�仯�����ͼ��ʾ��Cl-û�л����������¶��£����з���������ǣ�������| A�� | HClO2�ĵ���ƽ�ⳣ������ֵKa=10-6 | |
| B�� | ���������ڼ��������½��ȶ� | |
| C�� | pH=7ʱ����Һ�к�������Ũ�ȴ�СΪ��c��HClO2����c��ClO2-����c�� ClO2����c�� Cl-�� | |
| D�� | ͬŨ�ȵ�HClO2��Һ��NaClO2��Һ�������ϣ�������Һ����c��HClO2��+2c��H+��=c��ClO2-��+2c��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �μ�����ʱ���Ȳ����������ܽ� | |
| B�� | ��������Ĥ | |
| C�� | ���ȡ����ɡ����գ����ն���Fe2O3���� | |
| D�� | ���ж����ЧӦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3�� | B�� | 4�� | C�� | 5�� | D�� | 6�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1.0mol•L-1KNO3��Һ��H+��Fe2+��Cl-��SO42- | |
| B�� | pH=1����Һ��NH4+��Al3+��SO42-��Br- | |
| C�� | 0.1 mol•L-1FeCl3��Һ��NH4+��H+��I-��SCN- | |
| D�� | �����£���c��H+��ˮ•c��OH-��ˮ=10-26����Һ�У�K+��Fe2+��Cl-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ba��OH��2��Һ�еμ�NaHSO4��Һ��ǡ��Ϊ���ԣ�Ba2++OH-+H++SO42-�TBaSO4��+H2O | |
| B�� | NH4HCO3��Һ�����KOHŨ��Һ���ȣ�NH4++OH-$\frac{\underline{\;\;��\;\;}}{\;}$NH3��+H2O | |
| C�� | ����������Һ��̼����þ��Һ��Ӧ��Ca2++OH-+HCO3-�TCaCO3��+H2O | |
| D�� | KI��Һ��H2SO4�ữ��H2O2��Һ��ϣ�2 I-+H2O2+2 H+�T2 H2O+I2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֪2H2��g��+O2��g���T2H2O��g����H=-483.6kJ•mol-1����������ȼ����Ϊ241.8kJ•mol-1 | |
| B�� | ��֪NaOH��aq��+HCl��aq���TNaCl��aq��+H2O��l����H=-57.4kJ•mol-1��40.0gNaOH��ϡ��Һ��ϡ������ȫ�кͣ��ų�С��57.3kJ������ | |
| C�� | ��֪2C��s��+2O2��g���T2CO2��g����H=akJ•mol-1��2C��s��+O2��g��=2CO��g����H=bkJ•mol-1����a��b | |
| D�� | ��֪P�����ף�s���Tp�����ף�s����H��0������ױȺ����ȶ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com