
 全氮型超高能材料是指能量比常规炸药至少高一个数量级的新型高能物质,它最突出的特性是分子中蕴含有巨大的能量.
全氮型超高能材料是指能量比常规炸药至少高一个数量级的新型高能物质,它最突出的特性是分子中蕴含有巨大的能量.

科目:高中化学 来源: 题型:
| A、Cu(OH)2的溶解度增大 |
| B、Cu(OH)2的溶解度、Ksp均增大 |
| C、KspCu(OH)2增大 |
| D、Cu(OH)2的溶解度、Ksp均不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加NaOH |
| B、加盐酸 |
| C、加NH4Cl |
| D、加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:

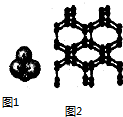
| A、C50Cl10摩尔质量为955g |
| B、C50Cl10晶体是原子晶体 |
| C、C50Cl10分子中含有25个碳碳双键 |
| D、C50Cl10分子共用电子对数目为105对 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com