
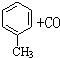
 $→_{加热}^{AlCl_{3},HCl}$
$→_{加热}^{AlCl_{3},HCl}$ 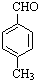 $→_{OH-,△}^{CH_{3}CHO}$B$→_{②H+}^{①C}$
$→_{OH-,△}^{CH_{3}CHO}$B$→_{②H+}^{①C}$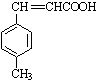 $→_{H_{2}SO_{4},加热}^{CH_{3}OH}$E
$→_{H_{2}SO_{4},加热}^{CH_{3}OH}$E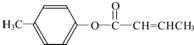 是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为
是E的一种同分异构体,该物质与足量NaOH溶液共热的化学方程式为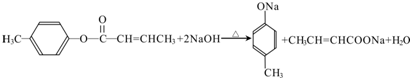 .
. .
. 分析 由合成路线可知,甲苯发生取代反应生成对甲基苯甲醛,再与CH3CHO在碱性条件下反应生成B,B为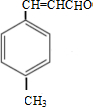 ,①中-CHO被弱氧化剂氧化为-COOH,而C=C不能被氧化,再酸化得到D
,①中-CHO被弱氧化剂氧化为-COOH,而C=C不能被氧化,再酸化得到D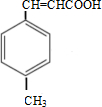 ,D与甲醇发生酯化反应生成E为
,D与甲醇发生酯化反应生成E为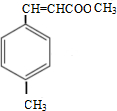 ,据此分析解答.
,据此分析解答.
解答 解:由合成路线可知,甲苯发生取代反应生成对甲基苯甲醛,再与CH3CHO在碱性条件下反应生成B,B为 ,①中-CHO被弱氧化剂氧化为-COOH,而C=C不能被氧化,再酸化得到D
,①中-CHO被弱氧化剂氧化为-COOH,而C=C不能被氧化,再酸化得到D ,D与甲醇发生酯化反应生成E为
,D与甲醇发生酯化反应生成E为 ,
,
(1)遇FeCl3溶液显紫色,则含酚-OH,且苯环上有两个取代基,另一取代基为-CH=CH2,则符合条件的A的同分异构体为邻、间、对乙烯基苯酚3种,B中含氧官能团的名称为醛基,
故答案为:3;醛基;
(2)试剂C不能与C=C反应,只氧化-CHO,则C为b或d,
故答案为:b、d;
(3)E同分异构体中含-COOC-,与足量NaOH溶液共热的化学方程式为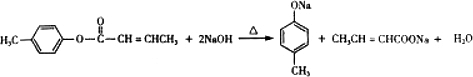 ,
,
故答案为: ;
;
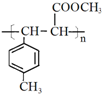
(4)E中含C=C,在一定条件下可以生成高聚物F,发生加聚反应,则F的结构简式为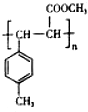 ,
,
故答案为: .
.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,根据反应前后结构简式差异性确定反应类型,再结合官能团推断,难点是同分异构体种类判断.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
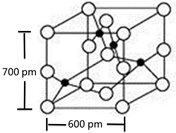 X、Y、M、Z、R为前四周期元素,且原子序数依次增大.XY2是红棕色气体;X与氢元素可形成XH3;M是周期表中电负性最大的元素;Z基态原子的M层是K层电子数的3倍;R2+离子的3d轨道中有9个电子.请回答下列问题:
X、Y、M、Z、R为前四周期元素,且原子序数依次增大.XY2是红棕色气体;X与氢元素可形成XH3;M是周期表中电负性最大的元素;Z基态原子的M层是K层电子数的3倍;R2+离子的3d轨道中有9个电子.请回答下列问题: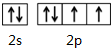 ;Z所在周期中第一电离能最大的主族元素是氯(元素名称)
;Z所在周期中第一电离能最大的主族元素是氯(元素名称)
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
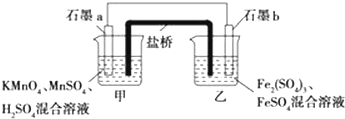
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
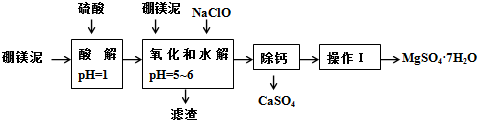
| 氢氧化物 | 开始沉淀时的pH | 完全沉淀时的pH |
| Mg(OH)2 | 9.3 | 10.8 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Al(OH)3 | 3.7 | 4.7 |
| 温度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 35g | B. | 30g | C. | 20g | D. | 15g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 阳离子 | Na+、Ba2+、NH4+ |
| 阴离子 | CH3COO-、OH-、Cl-、SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com