
| 元素 | A | B | C | D | E |
| 相关 信息 | 最高正价与最低负价代数和为2 | 与元素C可形成离子个数比为2:1和1:1的化合物 | 单质质软,通常保存在煤油中 | D元素可形成两种氧化物,其中一种是形成酸雨的主要成分 | 其单质是用途最广泛的金属,人体缺少该元素易患贫血症 |

 =297.2kJ,因此此反应的热化学方程式为SO2(g)+2CO(g)=S(s)+2CO2(g) △H=-297.2kJ/mol。
=297.2kJ,因此此反应的热化学方程式为SO2(g)+2CO(g)=S(s)+2CO2(g) △H=-297.2kJ/mol。

科目:高中化学 来源:不详 题型:单选题
| A.工业上电解YW饱和溶液冶炼金属Y |
| B.气态氢化物的稳定性:W > X |
| C.简单离子半径的大小顺序:r(Y+)>r(X—) |
| D.Y、W的最高价氧化物的水化物均能溶解金属Z |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

A.Q的一种核素中 的质子数和中子数相等 的质子数和中子数相等 |
| B.X的最高正化合价与最低负化合价的绝对值之差为6 |
| C.Y是常见的半导体材料 |
| D.Z的氧化物的水化物是强酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| R | | |
| X | Y | Z |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
 的空间构型是 ,其中D原子的杂化轨道类型是 。
的空间构型是 ,其中D原子的杂化轨道类型是 。
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| | 类比对象 | 结论 |
| A | Cl2+H2O HCl+HClO HCl+HClO | I2+H2O HI+HIO HI+HIO |
| B | C+2CuO ="==" 2Cu+CO2↑(条件:加热) | C+SiO2 ="==" Si+ CO2↑(条件:加热) |
| C | Na2O+H2O ="=" 2NaOH | CuO+H2O ="=" Cu(OH)2 |
| D | Ca(ClO)2+CO2+H2O="=" CaCO3↓+2HClO | Ca(ClO)2+SO2+H2O="=" CaSO3↓+2HClO |
| 元素 | 8O | 16S | 34Se | 52Te |
| 单质熔点(℃) | -218.4 | 113 | | 450 |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1390 |
| 主要化合价 | -2 | -2,+4,+6 | -2,+4,+6 | |
| 原子半径 | 逐渐增大 | |||
| 单质与H2反应情况 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
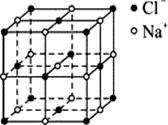
 X+2WZ
X+2WZ| A.离子晶体 | B.分子晶体 | C.原子晶体 | D.金属晶体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| X | 动植物生长不可缺少的元素,是蛋白质的重要成分 |
| Y | 最外层电子数是次外层的3倍 |
| Z | 短周期中,其原子半径最大 |
| Q | 生活中大量使用其合金制品,工业上可用电解其氧化物的方法制备 |
| M | 海水中大量富集的元素之一,其最高正化合价与负价的代数和为6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.M层才开始出现d轨道 |
| B.d轨道最早出现在第4周期元素 |
| C.电子排布时,3d轨道能量高于4s轨道 |
| D.d轨道有10种空间伸展方向 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com