
 2NO2 (g) ��H�� 0����Ӧ�����и����ʵ����ʵ���Ũ�ȣ�c����ʱ�䣨t���ı仯��ϵ����ͼ��ʾ��
2NO2 (g) ��H�� 0����Ӧ�����и����ʵ����ʵ���Ũ�ȣ�c����ʱ�䣨t���ı仯��ϵ����ͼ��ʾ��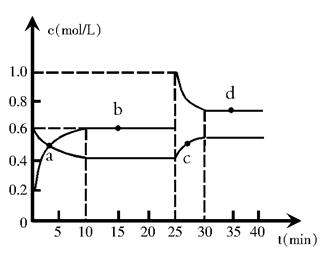
 ֱͨ������У�ܲ��¿�ֱͨ��Уϵ�д�
ֱͨ������У�ܲ��¿�ֱͨ��Уϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
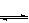 2SO3�����ﵽƽ�⡣��������У�����������������䣬����������ѹǿ���䣬����������SO2��ת����Ϊp%������������SO2��ת����
2SO3�����ﵽƽ�⡣��������У�����������������䣬����������ѹǿ���䣬����������SO2��ת����Ϊp%������������SO2��ת����| A������p% | B������p% | C��С��p% | D�����ж� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2H2(g)��O2(g)��2CO(g)��O2(g)
2H2(g)��O2(g)��2CO(g)��O2(g) 2CO2(g)
2CO2(g)�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 bZ(g)
bZ(g) 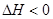 ����ͼ��������X��Z�����ʵ���Ũ����ʱ��仯�����ߡ�
����ͼ��������X��Z�����ʵ���Ũ����ʱ��仯�����ߡ�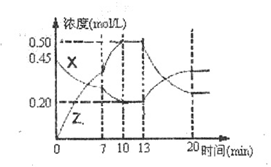
| A����X��ʾ0~10 min�ڸ÷�Ӧ��ƽ������Ϊv(x)=0.045mol/(L��min) |
| B����ѧ����ʽ��a:b=1:3 |
| C���Ʋ��ڵ�7minʱ���߱仯��ԭ����������� |
| D���Ʋ��ڵ�13minʱ�÷�Ӧ�պôﵽ��ѧƽ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
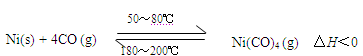
| A��50��80��ʱ���ʵ�����ѹǿ��������Ni(CO)4������ |
| B��180��200��ʱ����̬��Ni(CO)4 ��ֽ����Ni |
| C���ᴿ�����У�CO(g)�������ϼ��� |
| D���¶�Խ�ߣ�Ni(CO)4 (g)��ת����Խ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 pC(g)���ﵽƽ��������¶�ʱ��B��ת���ʱ����Сѹǿʱ�������ϵ��C����������Ҳ��С����:
pC(g)���ﵽƽ��������¶�ʱ��B��ת���ʱ����Сѹǿʱ�������ϵ��C����������Ҳ��С����:�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
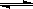 ��2SO3(g)
��2SO3(g) 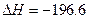 kJ��mol
kJ��mol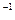 ��
��| ���� | �� | �� | �� |
| ��Ӧ��Ͷ���� | 2mol SO2��1mol O2 | 2mol SO3 | 4mol SO3 |
SO3��Ũ�ȣ�mol�� L L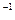 �� �� | c1 | c2 | c3 |
| ��Ӧ�������仯 | �ų�akJ | ����bkJ | ����ckJ |
| ��ϵѹǿ��Pa�� | p1 | p2 | p3 |
| ��Ӧ��ת���� |  | 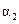 | 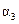 |
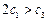 B��
B��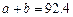 C��
C��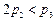 D��
D��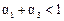
 ��2SO3(g)����˵����ȷ����
��2SO3(g)����˵����ȷ���� SO2��ת����Ϊ12. 5%��O2��ת����Ϊ25%�� ��ʼ���������е�SO2��O2���ʵ���֮��Ϊ4��1
SO2��ת����Ϊ12. 5%��O2��ת����Ϊ25%�� ��ʼ���������е�SO2��O2���ʵ���֮��Ϊ4��1�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2NH3�Ѵ�ƽ��״̬����___ _____
2NH3�Ѵ�ƽ��״̬����___ _____ һ��ʱ������ѹǿ���ٱ仯
һ��ʱ������ѹǿ���ٱ仯�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

 mol A��ͬʱ����2n mol C
mol A��ͬʱ����2n mol C�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com