
(16分)
甲同学进行Fe2+还原性的实验,针对异常现象进行探究。
步骤一:制取FeCl2溶液。向0.1 molL-1 FeCl3溶液中加足量铁粉振荡,静置后取上层清液,测得pH<1。
步骤二:向2 mL FeCl2溶液中滴加2滴0.1 molL-1 KSCN溶液,无现象;再滴加5滴5% H2O2溶液(物质的量浓度约为1.5 molL-1、pH约为5),观察到溶液变红,大约10秒左右红色褪去,有气体生成(经检验为O2)。
(1)用离子方程式表示步骤二中溶液变红的原因: 、 。
(2)甲探究步骤二中溶液褪色的原因:
I.取褪色后溶液两份,一份滴加FeCl3溶液无现象;另一份滴加KSCN溶液出现红色;
II.取褪色后溶液,滴加盐酸和BaCl2溶液,产生白色沉淀。
III.向2 mL 0.1 molL-1 FeCl3溶液中滴加2滴0.1 molL-1 KSCN溶液,变红,通入O2,无明显变化。
实验I的说明 ;②实验III的目的是 。
得出结论:溶液退色的原因是酸性条件下H2O2将SCN-氧化成SO42-。
(3)甲直接用FeCl2·4H2O配制 ① molL-1 的FeCl2溶液,重复步骤二中的操作,发现液体红色并未褪去。进一步探究其原因:
I.用激光笔分别照射红色液体和滴加了KSCN溶液的FeCl3溶液,前者有丁达尔效应,后者无。测所配FeCl2溶液的pH,约为3。由此,乙认为红色不褪去的可能原因是 ② 。
II.查阅资料后推测,红色不褪去的原因还可能是pH较大时H2O2不能氧化SCN-。乙利用上述部分试剂,通过实验排除了这一可能。乙的实验操作及现象是:
步骤 | 试剂及操作 | 现 象 |
i | ③ | 生成白色沉淀 |
ii | 向i所得溶液中滴加0.1 molL-1 FeCl3溶液 | ④ |
(1)2Fe2++H2O2+2H+=2Fe3++2H2O Fe3++3SCN-=Fe(SCN)3(2)①溶液红色褪色是因为SCN-发生了反应而不是三价铁离子。②排除双氧水分解产生的氧气氧化SCN-的可能。(3)①0.15,②双氧水将二价铁氧化为三价铁,PH增大促进三价铁离子水解形成红色氢氧化铁胶体。③取2mlBaCl2溶液,滴加0.1mol/L-1r KSCN溶液和5滴HNOOH溶液(多答盐酸或答酸化的BaCl2溶液0分),无明显现象。
【解析】
试题分析:
(1)Fe2+被H2O2氧化生成Fe3+,再与SCN-形成血红色的Fe(SCN)3;(2)Ⅰ、①取褪色后溶液两份,一份滴加FeCl3溶液无现象,说明溶液中SCN-离子不存在;另一份滴加KSCN溶液出现红色说明溶液中存在Fe3+;②实验Ⅲ的目的是排除H2O2分解产生的O2氧化SCN-的可能,如果氧气氧化SCN-,红色应褪去,但现通入氧气无现象说明氧气没有氧化SCN-;(3)由2Fe3++Fe=3Fe2+可知配制的FeCl2的浓度应为原FeCl3浓度的1.5倍;Ⅰ.用激光笔分别照射红色液体和滴加了KSCN溶液的FeCl3溶液,前者有丁达尔效应,说明H2O2氧化Fe2+使溶液pH增大,促进Fe3+水解生成Fe(OH)3胶体;后者无丁达尔效应,说明硫氰化铁溶液不能产生丁达尔效应; Ⅱ.如果SCN-被双氧水氧化,生成硫酸根离子,再加入Fe3+无明显现象,说明硫氰化钾已被氧化.
考点:了解Fe2+、Fe3+的性质及检验方法。设计、评:价或改进实验方案。


 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源:2014-2015学年四川省高三上学期期中考试化学试卷(解析版) 题型:选择题
以下是常见的五种中草药,下列说法正确的是
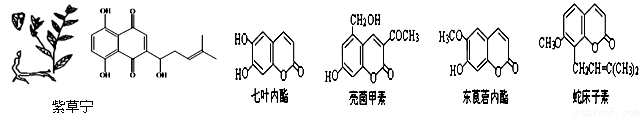
A.等量的紫草宁消耗NaOH溶液、溴水的物质的量比为3∶4
B.1mol上述五种物质与足量氢氧化钠溶液反应,消耗氢氧化钠最多的是亮菌甲素
C.七叶内酯与东莨菪内酯互为同系物。
D.一定条件下,等物质的量的五种中药消耗氢气:七叶内酯与东莨菪内酯一样多。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市静安区高三上学期期末教学质量检测化学试卷(解析版) 题型:选择题
硝基苯中溶有少量CaCl2,适宜的提纯方法是
A.过滤 B.蒸馏 C.分液 D.纸上层析
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省益阳市高三上学期期中考试化学试卷(解析版) 题型:选择题
下表中叙述Ⅰ和叙述Ⅱ均正确并且互为因果关系的是
选项 | 叙述Ⅰ | 叙述Ⅱ |
A | NH4Cl是强酸弱碱盐 | 将NH4Cl溶液蒸干可制备NH4Cl固体 |
B | Fe3+有强氧化性 | 用KSCN溶液可以鉴别Fe3+ |
C | SO2有还原性 | 用SO2可使溴水褪色 |
D | Cl2有漂白性 | 用Cl2可与石灰乳反应制备含氯消毒剂 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省益阳市高三上学期期中考试化学试卷(解析版) 题型:选择题
在MgCl2、KCl、K2SO4三种盐的混合溶液中,若K+、Cl-各1.5mol,Mg2+为0.5mol,则SO42-的物质的量是
A.0.25 mol B.0.5mol C.0.75mol D.0.75mol
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省高三12月月考化学试卷(解析版) 题型:选择题
下列离子方程式正确的是
A.用氢氧化钠溶液吸收二氧化氮:2OH-+2NO2===NO3-+NO↑+H2O
B.碳酸氢钠溶液与过量的澄清石灰水反应:2HCO3-+Ca2++2OH-===CaCO3↓+CO32-+2H2O
C.用浓盐酸酸化的KMnO4溶液与H2O2反应:2MnO4-+6H++5H2O2===2Mn2++5O2↑+8H2O
D.硫酸氢钠溶液与足量氢氧化钡溶液混合:H++SO42-+Ba2++OH-===BaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河南省高三12月月考化学试卷(解析版) 题型:选择题
下列有关化学用语正确的是
①乙烯的最简式C2H4 ②乙醇的结构简式C2H6O
③四氯化碳的电子式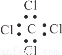 ④乙炔的结构简式CHCH
④乙炔的结构简式CHCH
⑤乙烷的结构式CH3CH3 ⑥乙醛的结构简式CH3COH
A.全对 B.全错 C.③④⑤ D.③④⑥
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三1月练习理综化学试卷(解析版) 题型:选择题
下列实验操作、现象和结论均正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 向某溶液中先滴加硝酸酸化,再滴加BaCl2溶液 | 有白色沉淀生成 | 该溶液中一定含有Ag+ |
B | 向AgNO3溶液中滴加过量氨水 | 溶液澄清 | Ag+与NH3H2O能大量共存 |
C | 用石墨作电极电解MgSO4溶液 | 某电极附近有白色沉淀生成 | 该电极为阳极 |
D | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置 | 下层溶液显紫红色 | 氧化性:Fe3+>I2 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省惠州市高三第三次调研考试化学试卷(解析版) 题型:选择题
用NA表示阿伏伽德罗常数的值。下列叙述正确的是:
A.常温常压下,22.4L CH4中含有4NA个C-H键
B.48g O3气体含有3NA个氧原子
C.在1L0 .5mol·L-lFeCl3溶液中含有0.5NA个Fe3+
D.标准状况下,2.24LCCl4含有的分子数为0.1NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com