
下列解释实验事实的方程式中,不准确的是
A.在CH3COONa 溶液中滴入无色酚酞,溶液变红:CH3COO- + H2O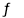 CH3COOH + OH-
CH3COOH + OH-
B.在Mg(OH)2白色悬浊液中滴入饱和FeCl3溶液,悬浊液变红褐:3Mg(OH)2 + 2Fe3+  2Fe(OH)3↓ + 3Mg2+
2Fe(OH)3↓ + 3Mg2+
C.在NaHSO3溶液中滴加紫色石蕊溶液,溶液变红:NaHSO3  Na+ + H+ + SO32-
Na+ + H+ + SO32-
D.在稀H2SO4酸化的KMnO4溶液中滴入双氧水,溶液褪色:2MnO4- + 5H2O2 + 6H+  2Mn2+ + 5O2↑ + 8H2O
2Mn2+ + 5O2↑ + 8H2O
科目:高中化学 来源:2014-2015学年新疆乌鲁木齐地区高三第二次诊断性测试化学试卷(解析版) 题型:填空题
(8分)元素周期表中第ⅦA族元素的单质及其化合物的用途广泛。
(1)Cl2的电子式是 。新制的氯水可用于漂白,工业上将氯气制成漂白粉的目的是 ,漂白粉是一种 (填“混合物”或“纯净物”)。
(2)碘元素在元素周期表中的位置是 ;为防缺碘,食盐中常添加碘酸钾,该物质内存在 键(填化学键类型)。
(3)溴单质是唯一常温下呈液态的非金属单质,液溴的保存通常采取的方法是 。
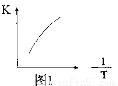
(4)已知:X2(g)+H2(g)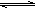 2HX(g) (X2表示Cl2、Br2和I2)。下图表示平衡常数K与温度T的关系。
2HX(g) (X2表示Cl2、Br2和I2)。下图表示平衡常数K与温度T的关系。
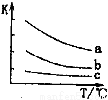
① H表示X2与H2反应的晗变,H 0。(填“>”、“<”或“=”)
H表示X2与H2反应的晗变,H 0。(填“>”、“<”或“=”)
②曲线a表示的是 (填“Cl2”、“Br2”或“I2”)与H2反应时K与T的关系。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市延庆县高三3月模拟理综化学试卷(解析版) 题型:实验题
(15分)焦亚硫酸钠(Na2S2O5)是一种常用的抗氧化剂。
某研究小组对焦亚硫酸钠进行如下研究:
(1)采用下图装置(实验前已除尽装置内的空气)制取Na2S2O5。
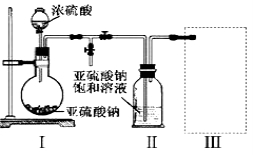
装置Ⅱ中有Na2S2O5析出,发生的化学反应方程式为:Na2SO3 + SO2 = Na2S2O5。
①装置Ⅰ中产生气体的化学方程式为 。
②要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是 。
③装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为 (填序号)。
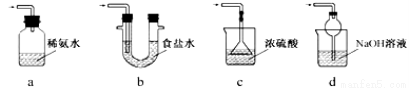
(2)【查阅资料】Na2S2O5溶于水即生成NaHSO3。
①NaHSO3溶液显酸性。请用化学用语和必要的文字解释原因________________________________;
证明该结论可采用的实验方法是 (填序号)。
a.测定溶液的pH
b.加入Ba(OH)2溶液
c.加入盐酸
d.加入品红溶液
e.用蓝色石蕊试纸检测
②检验Na2S2O5晶体在空气中已被氧化的实验方案是__________________。
(3)焦亚硫酸钠(Na2S2O5)在酸性条件下可将工业废水中的Cr2O72—还原为Cr3+。
①写出该反应的离子方程式_______________________。
②若处理Cr2O72—浓度为1×10-3mol/L的工业废水1L,需用Na2S2O5固体_________mg。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市门头沟区高三3月综合练习理综化学试卷(解析版) 题型:选择题
短周期元素X、T、Y、Z、R原子序数依次增大,T最内层电子数为最外层的2倍,部分元素的化合价关系如下表。则下列判断正确的是
X | Y | Z | R | |
主要化合价 | -4,+4 | -4,+4 | -2,+6 | -1,+7 |
A.非金属性:Z < R < Y
B.T与R可以形成化合物: TR2
C.X与R的单质均能使品红溶液褪色,且褪色原理相同
D.T的最高价氧化物的水化物分别能与X、Y、Z的最高价氧化物反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市房山区高三一模理综化学试卷(解析版) 题型:填空题
(14分)碳和氮的化合物与人类生产、生活密切相关。
(1)C、CO、CO2在实际生产中有如下应用:
a.2C + SiO2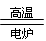 Si + 2CO b.3CO + Fe2O3
Si + 2CO b.3CO + Fe2O3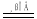 2Fe + 3CO2
2Fe + 3CO2
c.C + H2O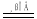 CO + H2 d.CO2 + CH4
CO + H2 d.CO2 + CH4 CH3COOH
CH3COOH
上述反应中,理论原子利用率最高的是 。
(2)有机物加氢反应中镍是常用的催化剂。但H2中一般含有微量CO会使催化剂镍中毒,在反应过程中消除CO的理想做法是投入少量SO2,为搞清该方法对催化剂的影响,查得资料:
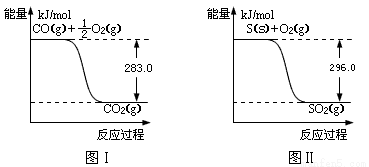
则:① 不用通入O2氧化的方法除去CO的原因是 。
② SO2(g) + 2CO(g) = S(s) + 2CO2(g) △H = 。
(3)汽车尾气中含大量CO和氮氧化物(NO )等有毒气体。
)等有毒气体。
①活性炭处理NO的反应:C(s)+2NO(g) N2(g)+CO2 (g) H=-a kJ·mol-1(a>0)
N2(g)+CO2 (g) H=-a kJ·mol-1(a>0)
若使NO更加有效的转化为无毒尾气排放,以下措施理论上可行的是: 。

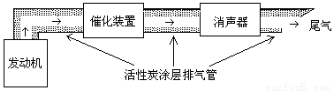
a.增加排气管长度 b.增大尾气排放口
c.添加合适的催化剂 d.升高排气管温度
②在排气管上添加三元催化转化装置,CO能与氮氧化物(NO )反应生成无毒尾气,其化学方程式是 。
)反应生成无毒尾气,其化学方程式是 。
(4)利用CO2与H2反应可合成二甲醚(CH3OCH3)。以KOH为电解质溶液,组成二甲醚 空气燃料电池,该电池工作时其负极反应式是 。
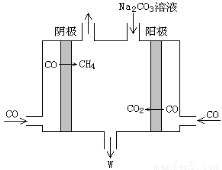
(5)电解CO制备CH4和W,工作原理如图所示,生成物W是 ,其原理用电解总离子方程式解释是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省台州市高三3月调研考试理综化学试卷(解析版) 题型:填空题
(15分)二氧化碳的过度排放会引发气候问题,而进行有效利用则会造福人类,如以CO2和 NH3 为原料合成尿素。经研究发现该反应过程为:
① CO2(g) + 2NH3(g)  NH2COONH4(s) △H1
NH2COONH4(s) △H1
② NH2COONH4(s) CO(NH2)2(s) + H2O(g) △H2>0
CO(NH2)2(s) + H2O(g) △H2>0
请回答下列问题:
(1)研究反应①的平衡常数(K)与温度(T)的关系,如图1所示,则△H1____0。(选填“>”、“<”或“=”)。
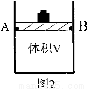
(2)有体积可变(活塞与容器之间的摩擦力忽略不计)的密闭容器如图2所示,现将3molNH3和2molCO2放入容器中,移动活塞至体积V为3L,用铆钉固定在A、B点,发生合成尿素的总反应如下:
CO2(g) + 2NH3(g) CO(NH2)2(s) + H2O(g)
CO(NH2)2(s) + H2O(g)
测定不同条件、不同时间段内的CO2的转化率,得到如下数据:
CO2的转化率T(℃) | 10min | 20min | 30min | 40min |
T1 | 30% | 65% | 75% | 75% |
T2 | 45% | 50% | a1 | a2 |
①T1℃下,l0min内NH3的平均反应速率为__________。
②根据上表数据,请比较T1_________T2(选填“>”、“<”或“=”);T2℃下,第30min 时,a1=________,该温度下的化学平衡常数为_________。
③T2℃下,第40min时,拔去铆钉(容器密封性良好)后,活塞没有发生移动,再向容器中通人3molCO2,此时v(正)_____ v (逆)(选填“>”、“<”或“=”),判断的理由是______。
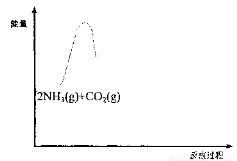
(3)请在下图中补画出合成氨总反应2NH3(g) + CO2(g) CO(NH2)2(s) + H2O(g)过程中能量变化图,并标明中间产物〔NH2COONH4(s)〕、 生成物CO(NH2)2(s) + H2O(g)〕。
CO(NH2)2(s) + H2O(g)过程中能量变化图,并标明中间产物〔NH2COONH4(s)〕、 生成物CO(NH2)2(s) + H2O(g)〕。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省台州市高三3月调研考试理综化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z、W、M的原子序数依次增大,X、Z同主族,Z、W、M同周期,其中X 与Y能形成两种物质,且常温下均为液体。W的氧化物既能溶于强碱溶液,又能溶于X、M形成的水溶液。已知W与M形成的物质在178°C时升华。下列说法不正确的是
A.Z、W、M的原子半径由大到小的顺序为Z>W>M
B.M分别与Z、W所形成的物质的晶体类型相同
C.X2Y2易溶于X2Y中,是由于X2Y2与X2Y能形成分子间氢键
D.将Z2Y在空气中加热可得到Z2Y2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省韶关市高三调研考试理综化学试卷(解析版) 题型:填空题
(15分)镁橄榄石主要成分是Mg2SiO4,电解法促进镁橄榄石固定CO2的工艺流程如下图所示:
已知:Mg2SiO4(s)+4HCl(aq) 2MgCl2(aq)+SiO2(s)+2H2O(l) △H =-49.04 kJ·mol-1
2MgCl2(aq)+SiO2(s)+2H2O(l) △H =-49.04 kJ·mol-1
固碳时主要反应的方程式为NaOH(aq)+CO2(g)=NaHCO3(aq)。
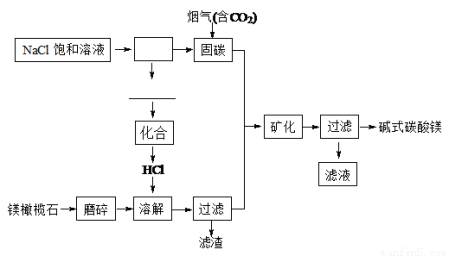
(1)上图方框里的操作名称是 ,横线上的物质有(填化学式) 。
(2)下列物质中也可用作“固碳”的是(填字母序号) 。
A.CaCl2 B.NH3·H2O
C.Na2CO3 D.H2O
(3)由下图可知,90 ℃后曲线A溶解效率下降,分析其原因 。
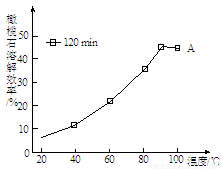
(4)经分析,所得碱式碳酸镁沉淀中含有少量NaCl。为提纯,可采取的方法是 。本流程中可循环利用的物质是(填化学式) 。
(5)另一种橄榄石的组成是Mg9FeSi5O20,用氧化物的形式可表示为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省八校高三二次联考理综化学试卷(解析版) 题型:选择题
氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强。25℃时氯气-氯水体系中存在以下平衡关系:
Cl2(g)  Cl2(aq) K1=10-1.2
Cl2(aq) K1=10-1.2
Cl2(aq)+ H2O  HClO + H+ +Cl- K2=10-3.4
HClO + H+ +Cl- K2=10-3.4
HClO  H+ + ClO- Ka=?
H+ + ClO- Ka=?
其中,Cl2(aq)、HClO和ClO-分别在三者中所占的物质的量分数(α)随pH变化的关系如图所示。下列表述正确的是
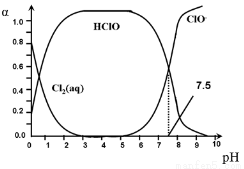
A.Cl2(g)+ H2O  2H+ + ClO- + Cl- K=10-10.9
2H+ + ClO- + Cl- K=10-10.9
B.pH=7.5时,用氯处理饮用水体系中,c(Cl-) + c(HClO) =c(H+)-c(OH-)
C.用氯处理饮用水时,pH=6.5时杀菌效果比pH=4.5时好
D.氯处理饮用水时,在夏季的杀菌效果比在冬季好
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com