
| A. | X能与某些非金属元素化合 | |
| B. | X可能为金属元素 | |
| C. | X原子的最外层电子数和核电荷数肯定为奇数 | |
| D. | X可能形成化学式为KXO3的盐 |
分析 原子的核电荷数小于18的某元素X,其原子的电子层数为n,1<n<4,最外层电子数为2n+1,则最外层电子数为5或7,原子核内质子数为2n2-1,如果n=2,N元素,如果n=3,为Cl元素,
A.N、Cl都能与某些非金属元素化合;
B.N、Cl都是非金属元素;
C.2n+1、2n2-1都为奇数;
D.X可能形成化学式为KXO3的盐,如KNO3、KClO3.
解答 解:原子的核电荷数小于18的某元素X,其原子的电子层数为n,1<n<4,最外层电子数为2n+1,则最外层电子数为5或7,原子核内质子数为2n2-1,如果n=2,N元素,如果n=3,为Cl元素,
A.N、Cl都能与某些非金属元素化合,如:与氢气发生反应,故A正确;
B.N、Cl都是非金属元素,则X不可能是金属元素,故B错误;
C.2n+1、2n2-1都为奇数,所以X原子的最外层电子数和核电荷数肯定为奇数,故C正确;
D.X可能形成化学式为KXO3的盐,如KNO3、KClO3,故D正确;
故选B.
点评 本题考查原子结构和性质,为高频考点,正确判断元素是解本题关键,熟悉常见元素原子核外电子排布,掌握原子结构和元素性质关系,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖注射液不能产生丁达尔效应,不属于胶体 | |
| B. | 油脂是高分子化台物,水解可生成甘油和高级脂肪酸 | |
| C. | 煤中含有的煤焦油,可由煤干馏获得 | |
| D. | 聚乙烯塑料的老化是因为发生了加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 在实验室里制取乙烯的反应为:
在实验室里制取乙烯的反应为: $→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O
$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
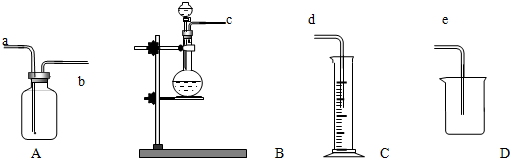
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②①③ | C. | ③②① | D. | ①③② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
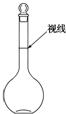 实验室配制500mL 0.2mol•L-1的Na2SO4溶液,实验操作步骤有:
实验室配制500mL 0.2mol•L-1的Na2SO4溶液,实验操作步骤有:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Be(OH)2可能具有两性 | |
| B. | 氯化铍中铍原子的最外层电子数是8个 | |
| C. | 氢氧化铍的碱性比氢氧化钙强 | |
| D. | 单质铍可和冷水剧烈反应产生氢气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com