
【题目】熟悉和使用中学化学实验中常见仪器及用品,是化学学习的基本要求。试回答以下问题:
(1) 在仪器: a.分液漏斗 b.试剂瓶 c.集气瓶 d.滴定管 e.容量瓶 f.量筒 g.托盘天平 h.玻璃棒 i.胶头滴管中,标有“0”刻度的是(填序号)___________________;若配制一定物质的量浓度H2SO4溶液所用的主要仪器有(填序号)________________。
(2)蒸发皿的使用:把滤液倒入蒸发皿中,再把蒸发皿放到铁架台的铁圈上。用酒精灯加热,同时用玻璃棒不断搅拌,其目的是__________________________。
(3) 用装置甲、乙、丙和乳胶管组成一套装置(气密性已检查),可用于制取并收集NH3或HCl气体。可供选择的液体试剂有:浓硫酸、浓盐酸、浓氨水,丙中试剂为紫色石蕊溶液。请回答下列问题:

① 若制取某气体的过程中,丙中的石蕊溶液变红,且烧瓶中的试剂A与分液漏斗中的试剂B均为无色液体,则试剂A为_____________________________,制取该气体利用了B的性质有________________ 、__________________。通过丙中紫色石蕊溶液变红或变蓝,说明乙中气体已集满。若石蕊溶液变蓝,则烧瓶甲中应加入的固体试剂A为____________;
② 若在乙中收集氨气,气体流经装置的顺序是:a→___→___→d(填接口代号)。
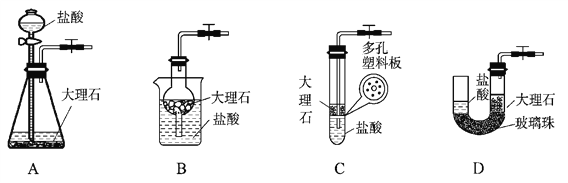
(4)下图中的装置D是实验室制备CO2的简易装置图,用该装置制备CO2可起到随时使反应发生,也可以随时使反应停止的效果。 在下图中的装置A、B、C也可起到相同效果的有_________________(填写编号)。
【答案】 d、g efhi 防止液体飞溅 浓盐酸 吸水性 溶于水放出大量热 NaOH或CaO或碱石灰 c b B
【解析】(1)标有“0”刻度的是滴定管和托盘天平,注意:量筒是没有零刻度的。配制一定物质的量浓度H2SO4溶液:首先用量筒量取一定体积的浓硫酸,在烧杯中稀释,用玻璃棒引流,转移至容量瓶中,洗涤,用胶头滴管定容。所以主要仪器为efhi。
(2)加热水溶液至沸腾后,液体容易飞溅,所以要不断搅拌。
(3)① 若制取某气体的过程中,丙中的石蕊溶液变红,说明制取的是HCl。所以A为浓盐酸,B为浓硫酸。浓硫酸加入浓盐酸中,会吸水,同时放热,都有利于HCl的从水中挥发。若石蕊溶液变蓝,则制取的是氨气,所以应该是将浓氨水滴加至固体氢氧化钠、氧化钙或碱石灰上。②氨气的密度小于空气,所以收集时应该短进长出。
(4)B中大理石和盐酸反应生成二氧化碳,需要停止反应时,将止水夹关闭,二氧化碳气体在干燥管内聚集,压强增大,将盐酸从干燥管内压至烧杯内,当盐酸液面低于大理石的时候,反应自动停止,所以选择B正确。选项A中,盐酸不可能都被压至分液漏斗中,没有固液分离的时候,所以反应不会停止,选项A错误。选项C中,没有加长颈漏斗,所以没有压入的空间,选项C错误。


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,下列叙述是可逆反应A(g)+3B(g)![]() 2C(g)在定容密闭容器中达到平衡的标志的是:( )
2C(g)在定容密闭容器中达到平衡的标志的是:( )
①C的生成速率与C的分解速率相等;
②单位时间内amol A生成,同时生成3amolB;
③A、B、C的浓度不再变化;
④混合气体的总压强不再变化;
⑤混合气体的平均摩尔质量不再变化;
⑥用A、B、C的物质的量浓度变化表示的反应速率之比为1:3:2;
⑦A、B、C的分子数目比为1:3:2;
⑧混合气体的密度不再变化
A. ②⑤ B. ①③④⑤ C. ②⑥⑦⑧ D. ⑤⑥⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】青蒿素,是烃的含氧衍生物,为无色针状晶体,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156~157℃,热稳定性差,青蒿素是高效的抗疟药.已知:乙醚沸点为35℃.从青蒿中提取青蒿素的方法之一是以萃取原理为基础的,主要有乙醚浸取法和汽油浸取法.乙醚浸取法的主要工艺为:

请回答下列问题:
(1)对青蒿进行干燥破碎的目的是_____________________。
(2)操作I需要的玻璃仪器主要有:烧杯、_______________,操作Ⅱ的名称是___________________。
(3)操作Ⅲ的主要过程可能是___________________________(填字母)。
A.加水溶解,蒸发浓缩、冷却结晶
B.加95%的乙醇,浓缩、结晶、过滤
C.加入乙醚进行萃取分液
(4)用下列实验装置测定青蒿素分子式的方法如下:将28.2g青蒿素样品放在硬质玻璃管C中,缓缓通入空气数分钟后,再充分燃烧,精确测定装置E和F实验前后的质量,根据所测数据计算。
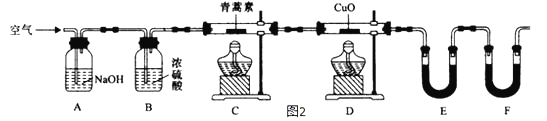
①装置E中盛放的物质是__________________,装置F中盛放的物质是____________________。
②该实验装置可能会产生误差,造成测定含氧量偏低,改进方法是______________________。
③用合理改进后的装置进行试验,称得:
装置 | 实验前/g | 实验后/g |
E | 22.6 | 42.4 |
F | 80.2 | 146.2 |
则测得青蒿素的最简式是_____________________________。
(5)某学生对青蒿素的性质进行探究。将青蒿素加入含有NaOH、酚酞的水溶液中,青蒿素的溶解量较小,加热并搅拌,青蒿素的溶解量增大,且溶液红色变浅,说明青蒿素与_________(填字母)具有相同的性质。
A.乙醇B.乙酸C.乙酸乙酯D.葡萄糖
(6)某科研小组经多次提取青蒿素实验认为用石油醚做溶剂较为适宜,实验中通过控制其他实验条件不变,来研究原料的粒度、提取时间和提取温度对青蒿素提取速率的影响,其结果如图所示:由下图可知控制其他实验条件不变,采用的最佳粒度、时间和温度为__________________。

A.80目、100分钟、50℃ B.60目、120分钟、50℃ C.60目、120分钟、55℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是某兴趣小组通过实验获得的相同体积足量稀硫酸与铁反应的实验数据:
实验 序号 | 金属 质量/g | 金属 状态 | c(H2SO4) mol/L | 实验 温度/℃ | 金属消失 的时间/s |
1 | 0.10 | 丝 | 0.7 | 20 | 250 |
2 | 0.10 | 丝 | 1.0 | 20 | 200 |
3 | 0.10 | 粉末 | 1.0 | 20 | 125 |
4 | 0.10 | 粉末 | 1.0 | 30 | 50 |
分析上述数据,回答下列问题:
(1)①实验1、2可得出的结论是,硫酸浓度越_____,反应速率越慢;
②实验3、4可得出的结论是温度越_____,反应速率越快.
(2)①用铁粉和稀硫酸反应制取H2,实验过程中绘制出生成H2的体积(V)与时间(t)的关系如图所示. 试分析判断OE段、EF段、FG段、GH段反应速率(分别用v (OE)、v (EF)、v (FG)、v (GH)表示)最快时段是______.
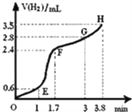
A.v (OE) B.v (EF)C.v (FG) D.v (GH)
②1min内反应较慢的原因是:_________;一段时间后反应明显加快的原因是_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】摄入过多的反式脂肪酸,容易堵塞血管而导致心脑血管疾病。顺式脂肪酸、反式脂肪酸的结构如下图所示。

试回答下列问题:
(1)顺、反式脂肪酸中所含相同官能团名称是____________。
(2)上述顺式脂肪酸的分子式为________。
(3)上述顺、反式脂肪酸不可能具备的下列化学性质是________(填序号)。
A.能使酸性高锰酸钾溶液褪色
B.1 mol顺式脂肪酸最多与2 mol氢气发生加成反应
C.能与乙醇发生酯化反应
D.能与溴发生加成且生成物相同
(4)顺式脂肪酸多为液态,空间呈弯曲状,反式脂肪酸多为固态,空间呈线型。油脂长时间高温加热,会产生反式脂肪酸,人类长期食用油炸食品,血液中反式脂肪酸过高容易堵塞血管而导致心脑血管疾病。这说明反式脂肪酸比顺式脂肪酸的硬度________(填“大”或“小”),熔点________(填“高”或“低”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,氯化亚硝酰(NOCl)足一种红黄色气体,其熔点- 64.5℃,沸点-5.5℃,可被水分解,其一种制备原理为Cl2+2NO =2NOC1。实验装置如下图所示,回答下列问题:

(1)实验前须排尽装置I、Ⅱ、Ⅲ中的空气,其原因是__________________________。
(2)NO是用铜与稀硝酸反应制得,其离子方程式为__________________________。
(3)图中各装置连接顺序为a→________________(按气流自左向右方向,用小写字母表示)。
(4)装置I、Ⅱ的作用是观察气泡调节气体的流速和________________________________。
(5)装置V是为了吸收尾气,防止污染环境,其中吸收NOC1时反应的化学方程式为____________(非氧化还原反应)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子方程式CO32﹣+2H+═H2O+CO2↑中CO32﹣的代表的物质可以是( )
A.CaCO3
B.NaHCO3
C.Na2CO3
D.BaCO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com