


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源:不详 题型:实验题
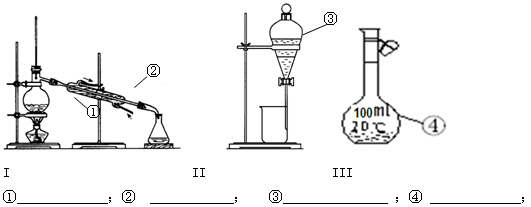


查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1.5mol石墨含有C-C键数为4.5NA |
| B.常温常压下,46g的NO2和N2O4混合气体含有的原子数为3 NA |
| C.常温常压下,22.4L的NO2和CO2合气体含有2 NA 个O 原子 |
| D.标准状况下,44.8L氟化氢中含有氟原子的数目为2NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1:1 | B.1:4 | C.4:1 | D.1:2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.12.4g白磷含有的P—P键数目为0.4NA |
| B.15.6gNa2O2与过量的CO2反应时,转移的电子数为0.4NA |
| C.标准状况下,a L甲烷和乙烷混合气体中的分子数为a NA /22.4 |
| D.5.6 g铁粉与硝酸完全反应失去的电子数一定为0.3NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.标况下,11.2L的CHCl3含有分子数为0.5NA |
| B.1mol苯乙烯中含有的碳碳双键数为4NA |
| C.常温下,14g乙烯和丙烯的混合物中总原子数为3NA |
| D.0.1mol CnH2n+2中含有的碳碳单键数为0.1nNA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.22.2% | B.30% | C.75.5% | D.80.6% |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com