
| A. | 2种 | B. | 4种 | C. | 6种 | D. | 8种 |
分析 相对分子质量为106.5的一氯代烃分子式为C5H11Cl,然后根据烷烃的异构体和氯原子的位置不同来解答.
解答 解:相对分子质量为106.5的一氯代烃分子式为C5H11Cl,分子式为C5H11Cl的同分异构体有
主链有5个碳原子的:CH3CH2CH2CH2CH2Cl;CH3CH2CH2CHClCH3;CH3CH2CHClCH2CH3;
主链有4个碳原子的:CH3CH(CH3)CH2CH2Cl;CH3CH(CH3)CHClCH3;CH3CCl(CH3)CH2CH3;CH2ClCH(CH3)CH2CH3;
主链有3个碳原子的:CH2C(CH3)2CH2Cl;
共有8种情况.
故选:D.
点评 本题考查以氯代物的同分异构体的判断,难度不大,做题时要抓住判断角度,找出等效氢原子种类.


科目:高中化学 来源: 题型:解答题
 二甲醚(CH3OCH3)是无色气体,可作为一种新型能源.由合成气(组成为H2、CO和少量的CO2)直接制备二甲醚,其中的主要过程包括以下四个反应:甲醇合成反应:
二甲醚(CH3OCH3)是无色气体,可作为一种新型能源.由合成气(组成为H2、CO和少量的CO2)直接制备二甲醚,其中的主要过程包括以下四个反应:甲醇合成反应:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 雪白、漂亮的“白木耳”,可能是在用硫黄熏制的过程中产生的SO2所致 | |
| B. | 钢铁在潮湿的空气中放置,易发生化学腐蚀而生锈 | |
| C. | 绿色化学的核心是从源头上消除工业生产对环境的污染 | |
| D. | 硅胶可用作食品干燥剂和催化剂载体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
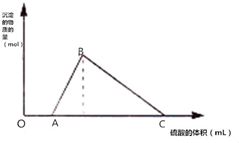 将M克钠和铝的混合物投入到一定量的水中,金属全部溶解,并收集到标准状况下体积为N升的气体,在所得溶液中逐滴加入1mol/L H2SO4,所得沉淀的物质的量随滴入硫酸溶液的体积变化如图所示;已知:A、C点对应的横坐标数据分别是500mL和2500mL,则
将M克钠和铝的混合物投入到一定量的水中,金属全部溶解,并收集到标准状况下体积为N升的气体,在所得溶液中逐滴加入1mol/L H2SO4,所得沉淀的物质的量随滴入硫酸溶液的体积变化如图所示;已知:A、C点对应的横坐标数据分别是500mL和2500mL,则查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 L 0.1 mol L-1NaHCO3溶液含有0.1NA个HCO3- | |
| B. | 1L0.1mol•L-1乙酸溶液电离的H+数为0.1NA | |
| C. | 2.8 g乙烯与丙烯的混合物中含碳原子的数目为0.2 NA | |
| D. | 标准状况下,22.4L溴苯的分子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化碳通过Na2O2粉末 | B. | 铝与Fe2O3发生铝热反应 | ||
| C. | 碳与SiO2电炉中抽取粗硅 | D. | 将锌片投入CuSO4溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 将含有少量CO2的CO通入足量Na2O2的试管中并不断用电火花引燃 | |
| B. | 向等物质的量的干冰和CaO的混合物中加几滴水 | |
| C. | 将1molCu置于含2molH2SO4的浓溶液中加热 | |
| D. | 在强光持续照射下,向过量的Ca(ClO)2浊液中通入少量的CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 温度(℃) | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H+ Na+ S2- CO32- | B. | H+ Ca2+ MnO4- NO3- | ||
| C. | K+ Ca2+ Cl- HCO3- | D. | Cl- Mg2+ Al3+ SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com