
【题目】均为0.1 mol/L、体积均为V0的HX、HY,分别加水稀释至体积V,pH随lg![]() 的变化关系如图所示。下列叙述正确的是
的变化关系如图所示。下列叙述正确的是
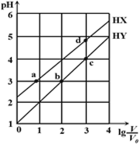
A.a、b两点的溶液中:c(X-)=c(Y-)
B.相同温度下,电离常数K(HX):d>a
C.溶液中水的的电离程度:d>c>b>a
D.lg![]() =2时,若同时微热两种液体(不考虑挥发),则
=2时,若同时微热两种液体(不考虑挥发),则![]() 减小
减小
【答案】A
【解析】
根据题中图示可知,本题考查弱电解质在水溶液中的电离平衡,运用酸或碱抑制水电离,平衡常数只随温度变化分析。
A. 如图所示:a、b的pH值相同,a点电荷守恒式为:![]() ,b点电荷守恒式为:
,b点电荷守恒式为:![]() ,由于同温度下两溶液的
,由于同温度下两溶液的![]() 、
、![]() 相等,所以
相等,所以![]() ,故A正确;
,故A正确;
B. 酸的电离平衡常数只与温度有关,所以相同温度下,电离常数K(HX):a=d,故B错误;
C. 酸或碱抑制水电离,酸中氢离子浓度越小其抑制水电离程度越小,根据图知,b溶液中氢离子浓度等于a,则水电离程度a=b,溶液中氢离子浓度:a=b>c>d,所以溶液中水的电离程度:a=b<c<d,故C错误;
D. lg![]() =2,若同时微热两种溶液(不考虑挥发),n(X)增大,n(Y)不变,二者溶液体积相等,所以
=2,若同时微热两种溶液(不考虑挥发),n(X)增大,n(Y)不变,二者溶液体积相等,所以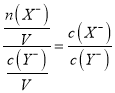 变大,故D错误;
变大,故D错误;
答案选A。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】锰酸锂(LiMn2O4)是新型锂离子电池常用的正极材料。工业上以软锰矿浆为原料可制备锰酸锂,同时制得副产品MnSO4·H2O晶体,其流程如图所示。
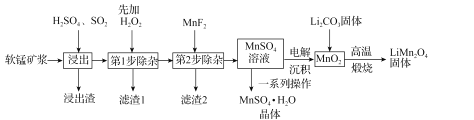
已知:(1)软锰矿浆的主要成分为MnO2,还含有Fe2O3,MgO、Al2O3,CaO,SiO2等杂质。
(2)温度高于27℃时,MnSO4晶体的溶解度随温度升高而逐渐降低。
(3)有关物质的溶度积常数如下表:
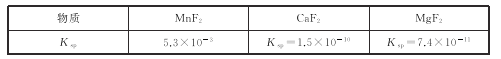
(1)“浸出”过程中MnO2转化为Mn2+的离子方程式为_____。该过程中,为提高软锰矿中MnO2的浸出率,下列措施可行的有_____(填字母)。
A.不断搅拌,使SO2和软锰矿浆充分接触
B.增大通入SO2的流速
C.适当升温
D.减少软锰矿浆的进入量
(2)第1步除杂中加入H2O2的目的是_____。
(3)第2步除杂,主要是将Ca2+,Mg2+转化为相应的氟化物沉淀除去,其中MnF2除去Mg2+反应的离子方程式为MnF2(s)+Mg2+(aq)=Mn2+(aq)+MgF2(s),该反应的平衡常数为_____。
(4)图中的一系列操作指的是_____。
(5)将MnO2和Li2CO3按4:1的物质的量之比配料,混合搅拌,然后高温煅烧600~750℃,制取产品LiMn2O4。写出该反应的化学方程式:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】压强变化不会使下列化学反应的平衡发生移动的是( )
A. C(s)+CO2(g)![]() 2CO(g)B. 3H2(g)+N2(g)
2CO(g)B. 3H2(g)+N2(g)![]() 2NH3(g)
2NH3(g)
C. 2SO2(g)+O2(g)![]() 2SO3(g)D. H2(g)+I2(g)
2SO3(g)D. H2(g)+I2(g)![]() 2HI(g)
2HI(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值.下列叙述错误的是
A.7.8gNa2O2与过量水反应转移电子数为0.1NA
B.1 mol OD-离子含有的质子、中子数均为9NA
C.46g NO2和N2O4混合气体中含有原子总数为3NA
D.已知N2(g)+3H2(g)![]() 2NH3(g)△H=﹣92.4kJ·mol﹣1,当有3NA个电子转移时,△H变为﹣46.2kJ·mol﹣1
2NH3(g)△H=﹣92.4kJ·mol﹣1,当有3NA个电子转移时,△H变为﹣46.2kJ·mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二茂铁![]() 的结构简式为
的结构简式为![]() ,与芳香族化合物性质相似,广泛应用于航天、化工等领域,可以环戊二烯与铁为原料制得。下列说法错误的是( )
,与芳香族化合物性质相似,广泛应用于航天、化工等领域,可以环戊二烯与铁为原料制得。下列说法错误的是( )
A.环戊二烯的化学式为![]() B.二茂铁的一氯取代物有2种
B.二茂铁的一氯取代物有2种
C.二茂铁能发生加成反应、氧化反应D.二茂铁中的铁为![]() 价
价
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】查尔酮类化合物![]() (
(![]() )的一种合成路线如下:
)的一种合成路线如下:

已知:![]()
回答下列问题:
(1)![]() 的名称为_______,
的名称为_______,![]() 的官能团名称为_____________。
的官能团名称为_____________。
(2)![]() 的分子式为_____________________。
的分子式为_____________________。
(3)![]() 的反应类型为____________________。
的反应类型为____________________。
(4)![]() 的反应方程式为_________________。
的反应方程式为_________________。
(5)M是E的同分异构体,满足下列条件,其中核磁共振氢谱有4组吸收峰,峰面积之比为![]() 的结构为__________________。
的结构为__________________。
①能发生水解反应 ②遇![]() 显色
显色
(6)参照上述合成路线,写出用苯乙烯与苯甲醛为原料制备查尔酮(![]() )的合成路线(其他试剂任选)。________________
)的合成路线(其他试剂任选)。________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂,而且与Cl2相比不会产生对人体有潜在危害的有机氯代物。已知: ClO2浓度过高或受热易分解,甚至会爆炸。现有下列制备ClO2的方法:
(1)方法一:氧化法
可用亚氯酸钠和稀盐酸为原料制备,反应原理为5NaClO2+4HCl=5NaCl+4ClO2↑+2H2O。
①该反应中氧化剂和还原剂的物质的量之比是_______________________。
②研究表明:若反应开始时盐酸浓度较大,则气体产物中有Cl2,用离子方程式解释产生Cl2的原因__________________________________________________。
(2)方法二:草酸还原法
在酸性溶液中用草酸(H2C2O4)还原氯酸钠的方法来制备ClO2
①写出制备ClO2的离子方程式:__________________________________________;
②与电解法相比,用草酸还原法制备ClO2的特点是____________________,提高了生产、储存及运输过程的安全性。
(3)已知: ClO2被I-还原为ClO2-、Cl-的转化率与溶液pH 的关系如图所示。当pH<2.0 时,ClO2-也能被I- 完全还原为Cl-。反应生成的I2与Na2S2O3 反应的方程式: 2Na2S2O3+ I2= Na2S4O6 + 2NaI。用ClO2消毒的饮用水中含有ClO2、ClO2-。测定饮用水中ClO2、ClO2-的含量,分两步进行:
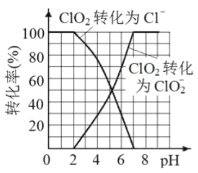
①用紫外分光光度法测得水样中ClO2的含量为a mol/L。
②用滴定法测量ClO2-的含量。请完成相应的实验步骤:
步骤1: 准确量取V mL 上述水样加入锥形瓶中。
步骤2: 调节水样的pH小于2。
步骤3: 加入足量的KI 晶体,充分反应。
步骤4: 加入少量淀粉溶液,用c mol/L Na2S2O3 溶液滴定至终点,消耗Na2S2O3 溶液V1 mL。
根据上述分析数据,测得该饮用水中ClO2-的浓度为___________mol/L( 用含字母的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年中国科学家成功合成NiO/TiO2电解水催化剂和新型高效的钙钛矿太阳能电池,为解决能源危机保护环境作出了重大贡献。请回答下列问题:
(1)TiO2与焦炭、Cl2在高温下反应的化学方程式为:TiO2+2C+2Cl2 ![]() TiCl4+2CO。
TiCl4+2CO。
①基态钛原子的价电子排布式为_________________。
②该反应中涉及到的非金属元素的电负性大小顺序为_______________________。
(2)已知NiO/TiO2催化化合物甲生成化合物乙的过程如图所示:

化合物甲的沸点小于化合物乙的沸点,主要原因是___________________。在化合物乙中,氧原子的杂化方式是______________。
(3)CH3NH3+、Ti4+、Pb2+、Cl-等离子是组成新型钙钛矿太阳能电池的主要离子。CH3NH3+离子中H—N—H键的键角比NH3分子中H—N—H键的键角 ______ (填“大”或“小”),原因是_____________ 。
(4)Sb(锑)和Ga(镓)的卤化物有很多用途。一定条件下将SbCl3与GaCl3以物质的量之比为l:l反应得到一种固态离子化合物,有人提出了以下两种结构。你认为下列关于结构和说法中合理的是 ____ 。
a. [SbCl2+][GaCl4-] b. [GaCl2+][SbCl4-] c. 没有相关资料,无法判断
(5)金属钛晶胞(如图1所示)中有若干个正四面体空隙,图1中a、b、c、d四个钛原子形成的正四面体其内部空隙中可以填充其他原子。
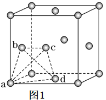
①请回答,金属钛晶胞的结构属于____________。
a. 简单立方 b. 体心立方 c. 面心立方 d. 金刚石型
②若晶胞中所有的正四面体空隙中都填充氢原子,那么形成的氢化钛的化学式为______________。
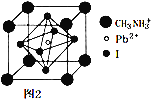
(6)某钙钛矿太阳能电池材料的晶胞如图2所示,其晶胞参数为d pm、密度为ρ g·cm-3。则该晶体的摩尔质量________ g·mol-1。(用含d、ρ等符号的式子表示,用NA表示阿伏加德罗常数的值)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法中正确的是()
A.Ksp(AB2)<Ksp(CD),说明AB2的溶解度小于CD的溶解度
B.在ZnS的沉淀溶解平衡体系中加入蒸馏水,ZnS的Ksp增大
C.AgCl分别在同浓度的CaCl2溶液和NaCl溶液中溶解度不同
D.在CaCO3的沉淀溶解平衡体系中加入稀盐酸,沉淀溶解平衡不移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com