
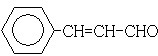 ;
; ;
; 、
、 、
、 、
、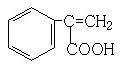 (其中任意两种).
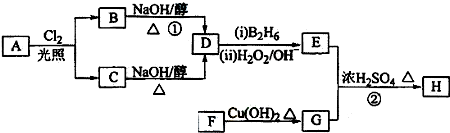
(其中任意两种). 分析 11.2L(标准状况)的烃A的物质的量=$\frac{11.2L}{22.4L/mol}$=0.5mol,11.2L(标准状况)的烃A,在氧气中充分燃烧可以生成88gCO2和45gH2O,n(CO2)=$\frac{88g}{44g/mol}$=2mol,n(H2O)=$\frac{45g}{18g/mol}$=2.5mol,烃、二氧化碳、水的物质的量之比=0.5mol:2mol:2.5mol=1:4:5,根据原子守恒知,A分子式为C4H10,且A分子结构中有3个甲基,则A的结构简式为(CH3)3CH,A发生取代反应生成氯代烃B、C,B和C均为一氯代烃,则B和C发生消去反应生成烯烃D,D的结构简式为CH2=C(CH3)2,D发生信息反应生成E,结合题给信息知,E结构简式为CH3CH(CH3)CH2OH,在催化剂存在下1molF与2molH2反应,生成3-苯基-1-丙醇,F的结构简式为 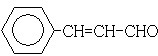 ,F中醛基氧化为羧基生成G为
,F中醛基氧化为羧基生成G为 ,D与E发生酯化反应生成H为
,D与E发生酯化反应生成H为 ,据此分析解答.
,据此分析解答.
解答 解:11.2L(标准状况)的烃A的物质的量=$\frac{11.2L}{22.4L/mol}$=0.5mol,11.2L(标准状况)的烃A,在氧气中充分燃烧可以生成88gCO2和45gH2O,n(CO2)=$\frac{88g}{44g/mol}$=2mol,n(H2O)=$\frac{45g}{18g/mol}$=2.5mol,烃、二氧化碳、水的物质的量之比=0.5mol:2mol:2.5mol=1:4:5,根据原子守恒知,A分子式为C4H10,且A分子结构中有3个甲基,则A的结构简式为(CH3)3CH,A发生取代反应生成氯代烃B、C,B和C均为一氯代烃,则B和C发生消去反应生成烯烃D,D的结构简式为CH2=C(CH3)2,D发生信息反应生成E,结合题给信息知,E结构简式为CH3CH(CH3)CH2OH,在催化剂存在下1molF与2molH2反应,生成3-苯基-1-丙醇,F的结构简式为 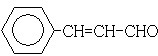 ,F中醛基氧化为羧基生成G为
,F中醛基氧化为羧基生成G为 ,D与E发生酯化反应生成H为
,D与E发生酯化反应生成H为
(1)通过以上分析知,A的结构简式为(CH3)3CH,
故答案为:(CH3)3CH;
(2)通过以上分析知,反应(1)的反应类型为消去反应,
故答案为:消去反应;
(3)通过以上分析知,F的结构简式是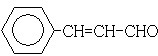 ,
,
故答案为: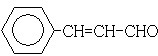 ;
;
(4)E结构简式为CH3CH(CH3)CH2OH,G为 ,二者发生酯化反应生成酯,所以反应②的化学方程式为
,二者发生酯化反应生成酯,所以反应②的化学方程式为 ,
,
故答案为: ;
;
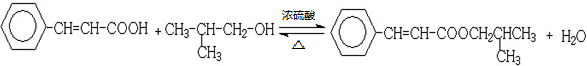
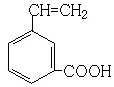
(6)G为 ,与G具有相同官能团的芳香类同分异构体,说明其同分异构体中含有碳碳双键、羧基和苯环,可以将官能团作相应的位置变换而得出其芳香类的同分异构体.所以其同分异构体有
,与G具有相同官能团的芳香类同分异构体,说明其同分异构体中含有碳碳双键、羧基和苯环,可以将官能团作相应的位置变换而得出其芳香类的同分异构体.所以其同分异构体有 、
、 、
、 、
、 ,其四种,
,其四种,
故答案为:4; 、
、 、
、 、
、 (其中任意两种).
(其中任意两种).
点评 本题考查有机物推断,侧重考查学生分析、推断、知识迁移能力,正确推断A的结构是解本题关键,根据物质官能团确定性质,注意结合题给信息分析,难点是同分异构体种类的判断,题目难度中等.


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 使用容量瓶前必须检查容量瓶是否漏水 | |
| B. | 容量瓶用蒸馏水洗净后,再用待配溶液润洗 | |
| C. | 称好的固体试样需用纸条小心地送入容量瓶中 | |
| D. | 摇匀后发现凹液面下降,再加水至刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑥ | B. | ①②④⑤⑥ | C. | ①④⑤⑥ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
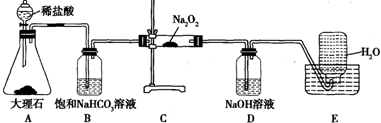
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O和Na2O2的混合物共1mol,阴离子数目在NA~2NA之间 | |
| B. | 1mol OH-和1mol-OH (羟基)中含有的质子数均为9NA | |
| C. | 铁做电极电解食盐水,若阴极得到NA个电子,则阳极产生11.2L气体(标准状况下) | |
| D. | 某密闭容器盛有0.1mol N2和0.3mol H2,在一定条件下充分反应,转移电子的数目为0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高温下,16.8g Fe与足量水蒸气完全反应失去电子数为0.8NA | |
| B. | 一定条件下Fe粉与足量的浓硫酸反应,转移电子数为3NA | |
| C. | 1.8g重水(D2O)中含有的质子数和电子数均为NA | |
| D. | 标准状况下,22.4L NO 和22.4L O2混合后所得气体中分子总数为1.5NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com