
【题目】铜有两种常见的氧化物CuO和Cu2O。某学习小组取0.98g(用精密天平测量)Cu(OH)2固体加热,有铜的氧化物生成,其质量随温度变化如图1所示:另外,某同学绘制了三条表示金属氧化物与其所含金属元素的质量的关系曲线,如图2所示。则下列分析正确的是
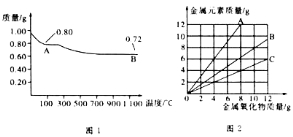
A.图1中A和B化学式分别为Cu2O和CuO
B.图1整个过程中共生成0.26g水
C.图2三条曲线中,表示CuO和其中所含Cu元素质量关系的曲线是A
D.图1中,A到B的过程中有0.01mol电子发生了转移
【答案】D
【解析】
试题分析:A、由0.98gCu(OH)2可知其物质的量为0.01mol,若全部生成CuO,则质量为0.01mol×80gmol-1=0.8g,所以A点是CuO;若全部生成Cu2O,则质量为0.005mol×144gmol-1=0.72g,所以B点是Cu2O,A错误;B、根据化学方程式Cu(OH)2![]() CuO+H2O、4CuO
CuO+H2O、4CuO![]() 2Cu2O+O2↑可知,水的物质的量为0.01mol,质量为0.01mol×18g/mol=0.18g,B错误;C、CuO和其中所含Cu元素的质量关系(以CuO的质量为10g计算)为:
2Cu2O+O2↑可知,水的物质的量为0.01mol,质量为0.01mol×18g/mol=0.18g,B错误;C、CuO和其中所含Cu元素的质量关系(以CuO的质量为10g计算)为:
CuO~ Cu
8064 10g8g
观察图2可知,B曲线符合上述质量关系,表示的是CuO,C错误;D、错误根据反应式4CuO![]() 2Cu2O+O2↑可知,A到B的过程中有0.01mol电子发生了转移,D正确;答案选D。
2Cu2O+O2↑可知,A到B的过程中有0.01mol电子发生了转移,D正确;答案选D。


科目:高中化学 来源: 题型:
【题目】某研究性学习小组为合成1 一丁醇,查阅资料得知一条合成路线:
CH3CH=CH2+CO+H2![]() CH3CH2CH2CHO
CH3CH2CH2CHO![]() CH3CH2CH2CH2OH
CH3CH2CH2CH2OH
CO的制备原理:HCOOH![]() CO+H2O,并设计出原料气的制备装置(如图)。
CO+H2O,并设计出原料气的制备装置(如图)。

请填写下列空白:
(1)实验室现有锌粒、稀硝酸、稀盐酸、浓硫酸、2-丙醇,从中选择合适的试剂制备丙烯。写出化学方程式:_______________________。
(2)若用以上装置制备H2,在虚线框内画出收集干燥H2的装置图。
(3)制丙烯时,还产生少量SO2、CO2及水蒸气,该小组用以下试剂检验这四种气体,混合气体通过试剂的顺序是_______________(填序号)
① 饱和Na2SO3溶液② 酸性KMnO4溶液③ 石灰水④ 无水CuSO4 ⑤ 品红溶液
(4)合成正丁醛的反应为正向放热的可逆反应,为增大反应速率和提高原料气的转化率,你认为应该采用的适宜反应条件是_____________。
a.低温、高压、催化剂 b.适当的温度、高压、催化剂
c.常温、常压、催化剂 d.适当的温度、常压、催化剂
(5)正丁醛经催化加氢得到含少量正丁醛的1-丁醇粗品,为纯化1-丁醇,该小组查阅文献得知:① RCHO+NaHSO3(饱和)→RCH(OH)SO3Na↓;②沸点:乙醚34℃,1-丁醇118℃,并设计出如下提纯路线:

试剂1为_________,操作1为__________,操作2为__________,操作3为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.氢氧化铁胶体的制备步骤如下:
(1)用烧杯取少量蒸馏水,放在酒精灯上加热至沸腾;
(2)向烧杯中逐滴加入饱和FeCl3溶液;
(3)继续煮沸至液体是透明的红褐色,即得Fe(OH)3胶体.
回答下列问题:
①写出制备Fe(OH)3胶体的化学方程式_____________________;
②如何确定你制备的胶体是否成功?__________________________;
③若向Fe(OH)3胶体中逐滴加入H2SO4溶液会出现的现象:__________________;
II.描述下列反应的现象并写出反应的离子方程式:
①向NaHCO3溶液中加入NaHSO4溶液,现象______________,离子方程式___________;
②向FeCl3溶液中加入NaOH溶液,现象_______,离子方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】

A. 操作①:使用稍浸入液面下的倒扣漏斗检验氢气的纯度
B. 操作②:使用CCl4萃取溴水中的溴时,振荡后需打开活塞使漏斗内气体放出
C. 操作③:吸收氨气或氯化氢气体并防止倒吸(氨气或氯化氢均极易溶于水)
D. 操作④:用食指顶住瓶塞,另一只手托住瓶底,把瓶倒立,检查容量瓶是否漏水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )

A.图1所示,从能量角度考虑,石墨比金刚石稳定
B.图2表示Al3+与OH-反应时含铝微粒浓度变化曲线,图中a点溶液中大量存在Al3+
C.图3所示,图中的阴影部分面积的含义是(v正-v逆)
D.图4表示0.001 mol·L-1盐酸滴定0.001 mol·L-1NaOH溶液的滴定曲线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某个容积为2 L的密闭容器内,在T℃时按下图1所示发生反应:

mA(g)+nB(g)![]() pD(g)+qE(s) H<0(m、n、p、q为最简比例的整数)。
pD(g)+qE(s) H<0(m、n、p、q为最简比例的整数)。
(1)根据图1所示,反应开始至达到平衡时,用D表示该反应速率为____________ mol/(L·min);方程式中m:n:p:q =________________
(2)该反应的化学平衡常数K为_________________(保留至一位小数);
(3)下列措施能增大B的转化率的是 ( )
A.升高温度 B.保持体积不变通入1molB
C.保持体积不变移出部分物质D(g) D.将容器的容积增大为原来的2倍
E. 保持体积不变通入1mol A
(4)能判断该反应已经达到化学平衡状态的是( )
A.恒容恒温时容器中气体压强保持不变
B.混合气体中D浓度不变
C.v(A)正 = v(A)逆
D.恒容时容器中气体密度不变
(5)反应达到平衡后,第7 min时,改变条件,在第9min达到新的平衡,在图2上作出第7 min至第15 min(作在答题纸上):下列情况下,D浓度变化图像
①若降低温度且平衡时D物质的量变化了0.4 mol (用虚线)
②若将容器的容积压缩为原来一半(用实线)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(双选)恒温、恒压下,1 mol A和1 mol B在一个容积可变的容器中发生如下反应:
A(g)+2B(g)![]() 2C(g),一段时间后达到平衡,生成a mol C,则下列说法中正确的是( )
2C(g),一段时间后达到平衡,生成a mol C,则下列说法中正确的是( )
A.物质A、B的转化率之比为1∶2
B.起始时刻和达平衡后容器中混合气体密度相等
C.当v正(A)=2v逆(C)时,可断定反应达到平衡状态
D.若起始时放入3 mol A和3 mol B,则达平衡时生成 3a mol C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写正确的是( )
A.稀硫酸滴在铜片上:Cu+2H+ = Cu2++H2↑
B.向CH3COOH溶液中加入CaCO3:2 CH3COOH+CaCO3 = 2 CH3COO-+Ca2++H2O+CO2↑
C.稀硫酸与Ba(OH)2溶液混合:H++ SO![]() +OH-+ Ba2+ = BaSO4↓+H2O
+OH-+ Ba2+ = BaSO4↓+H2O
D.NaOH溶液与KHCO3溶液混合:OH- + HCO3- = H2O +CO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com