
【题目】在标准状况下,称量一个充满氧气的容器,质量为66.4 g,若改充氮气,其质量为66 g,则容器的容积为( )
A.4.48 LB.11.2 LC.2.24 LD.5.6 L
 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:
【题目】分别取1mol葡萄糖进行下列实验: ①进行银镜反应时,需Ag(NH3)2OHmol,反应后葡萄糖变为(结构简式).
②与乙酸反应生成酯,从理论上讲完全酯化需要g 乙酸.
③若使之完全转化为CO2和H2O,所需氧气的体积在标准状况下为L,反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据问题填空:
(1)室温下: pH=13的CH3COONa溶液加水稀释100倍后,pH11(填“>”“=”或“<”);
(2)pH相等时,①NH4Cl②(NH4)2SO4③NH4HSO4三种溶液中c(NH4+)由大到小的顺;
(3)等体积、等浓度的氢氧化钠与醋酸混合后,溶液中c(Na+)c(CH3COO﹣)(填“>”“=”或“<”); pH=13的氢氧化钠与pH=1的醋酸等体积混合后溶液呈性;
(4)用0.1000mol/L NaOH溶液滴定20.00mL0.1000mol/L CH3COOH溶液所得滴定曲线如图. 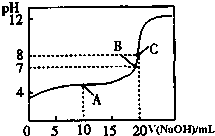
①为减小实验误差,由图可知滴定时指示剂应选用;(填“石蕊”、“酚酞”、“甲基橙”);
②A点的离子浓度大小关系是
③A,B,C三点所示溶液导电能力最强的是点对应的溶液;
④A,B,C三点水的电离程度大小关系是;
(5)相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水②0.1molL﹣1盐酸③0.1molL﹣1氯化镁溶液④0.1molL﹣1硝酸银溶液中,C(Ag+)大小顺序: . (用序号表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 2mL0.5mo/L硅酸钠溶液中滴入适量盐酸制备硅酸胶体,所得胶粒数目为0.001NA
B. 1molNa2O2中含有的离子总数是4NA
C. 常温常压下,7.8gNa2S和Na2O2的混合物中,阴离子所含电子数为1.8NA
D. 2.7gAl与足量氢氧化钠溶液反应,反应过程中转移的电子数目是0.15NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验设计中能达到预期目的的是( )
A. 用酒精萃取碘水中的碘,将碘的酒精溶液从分液漏斗的上口倒出
B. 在沸水中逐滴加入FeCl3溶液,继续煮沸至溶液呈红褐色即可得到Fe(OH)3胶体。
C. 将氢气和氧气的混合气体通过灼热的氧化铜除去氢气
D. 氯酸钾和二氧化锰的混合物充分加热后可用溶解、过滤、蒸发的方法分离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将10mL质量分数为50%(密度1.4g/mL)的硫酸稀释成100mL,下列说法正确的是( )
A.纯硫酸的摩尔质量为98
B.上述100mL稀硫酸中含溶质14g
C.上述稀释过程所需要的蒸馏水为90mL
D.质量分数为50%的硫酸物质的量浓度为7.14mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的化学用语表达正确的是( )
A.甲烷的球棍模型: ![]()
B.羟基的电子式: ![]()
C.乙醛的结构式:CH3CHO
D.(CH3)3COH的名称:2,2二甲基乙醇
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com