
(16分)活性氧化锌在橡胶、化工、涂料、陶瓷、医药、电子等行业有着广泛的应用。但随着锌资源的不断开发和利用,锌矿资源越来越少,因此研究利用锌二次资源对缓解锌资源枯竭进程具有重要意义。下图是以含锌铜烟尘(火法炼铜的副产品,主要成分是ZnO、CuO和FeO)制备活性氧化锌的工艺流程:
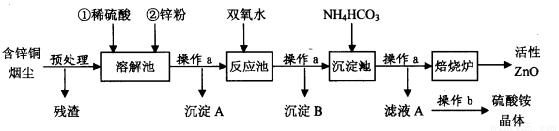
含锌铜烟尘经过预处理后的主要成分为ZnO,还含有少量的CuO和Fe2O3。
(1)操作a名称是____ ,在实验室中,该过程用到的主要玻璃仪器有 。
(2)溶解池中待固体全部溶解后,加入锌粉的作用有:
①将Fe3+还原为Fe2+;② :③调节溶液的pH(控制其在5,0-5.4之间)。
(3)检验溶解池中Fe3+已全部被还原为Fe2+的最佳试剂是 ;
(4)右表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为
1.0 mol-l计算)。反应池中的温度控制在90-95℃,请写出反应池中所发生反应的离子方
程式: 。
| 开始沉淀的pH | 沉淀完全的pH |
Fe3+ | 1.1 | 3.2 |
Fe2+ | 5.8 | 8.8 |
2n2+ | 5.9 | 8.9 |
(5)操作b的名称是________ ;
(6)沉淀池中得到的沉淀化学式可以表示为:aZnCO3·bZn(OH)2·cH2O(a、b、c均为整数)。某校化学兴趣小组的同学为了确定其组成,进行如下实验:称取3.59g沉淀进行焙烧,将焙烧过程中产生的气体依次通过足量的浓硫酸和碱石灰,它们分别增重0.72g和0.44g,则该沉淀的组成为 。
(1)过滤 烧杯、漏斗、玻璃棒; (2)除去杂质Cu2+ (3)KSCN溶液
(4)2Fe2++H2O2+4H2O=2Fe(OH)3↓+4H+;(5) 蒸发浓缩、冷却结晶;(6) ZnCO3?2Zn(OH)2?2H2O.
【解析】
试题分析:(1)操作a是将固体与溶液分离,应采取过滤的方法,过滤所用的主要玻璃仪器有:烧杯、漏斗、玻璃棒,答案为:过滤;烧杯、漏斗、玻璃棒;
(2)溶解池反应后溶液中还含有硫酸锌、硫酸铜、硫酸亚铁与硫酸铁,加入锌粉还有除去杂质Cu2+的作用,答案为:除去杂质Cu2+;
(3)Fe3+遇KSCN溶液呈红色,是Fe3+的特征反应,可以检验Fe3+的存在,答案为:KSCN溶液;
(4)反应池中加入H2O2的目的是将Fe2+氧化为Fe3+便于除去,同时不引入新的杂质,由工艺流程可知,生成氢氧化亚铁沉淀,反应方程式为2Fe2++H2O2+4H2O=2Fe(OH)3↓+4H+;
(5)操作b从溶液中获得硫酸铵晶体,应采取蒸发浓缩、冷却结晶等操作,答案为:蒸发浓缩、冷却结晶;
(6)分解最终生成氧化锌、二氧化碳与水,浓硫酸增重0.72g为生成的水的质量,物质的量为0.72/18=0.04mol,碱石灰增重0.44g为生成的二氧化碳的质量,物质的量为0.44/44=0.01mol,根据质量守恒可知氧化锌的质量=3.59g-0.72g-0.44g=2.43g,其物质的量为2.43/81=0.03mol,则n(ZnCO3)=0.01mol,n[Zn(OH)2]=0.03mol-0.01mol=0.02mol,n(H2O)=0.04mol-0.02mol=0.02mol,故n(ZnCO3):n[Zn(OH)2]:n(H2O)=0.01mol:0.02mol:0.02mol=1:2:2,该沉淀的组成为ZnCO3?2Zn(OH)2?2H2O.
考点:考查物质除杂的工艺流程的综合应用。


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源:2015届江苏省、常州一中、沭阳中学高三联合调研化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列叙述中正确的是
A.78g苯含有C=C双键的数目为3NA
B.室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA
C.0.1molMg在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为0.2NA
D.50mL18.4mol·L-1浓硫酸与足量铜微热反应,生成SO2分子的数目为0.46NA
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高三质量调研化学试卷(解析版) 题型:选择题
下列物质的使用不涉及化学变化的是
A.明矾用作净水剂 B.液氨用作致冷剂 C.氢氟酸刻蚀玻璃 D.生石灰作干燥剂
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高三上学期第一次阶段性检测化学试卷(解析版) 题型:选择题
下列对有关实验事实的解释正确的是
A.向某溶液中滴加氯水后,再加入KSCN溶液,溶液呈红色,说明原溶液中含有Fe2+
B.浓硫酸和浓盐酸长期暴露在空气中浓度均降低,原理不相同
C.向某溶液中加入氯化钡溶液,生成白色沉淀,再加入稀盐酸,沉淀不溶解,则原溶液一定含有SO42
D.常温下,浓硫酸可以用铁质容器储运,说明铁与冷的浓硫酸不反应
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高三上学期第一次阶段性检测化学试卷(解析版) 题型:选择题
通过溶解、过滤、蒸发等操作,可将下列各组混合物分离的是
A.硝酸钠 氢氧化钠 B.氧化铜 二氧化锰
C.氯化钾 碳酸钙 D.硫酸铜 氢氧化钠
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高三上学期期中考试化学试卷(解析版) 题型:选择题
25oC时,2amol·L-1氢氟酸水溶液中,用NaOH溶液调节溶液pH(忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系如下图所示。下列说法正确的是
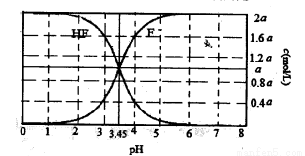
A.当c(F一)>c(HF)时,溶液呈碱性
B.当pH=3时,溶液中c(F一)<c(Na+)
C.当pH=3.45时,所加NaOH溶液恰好与HF完全反应
D.当pH=4时,溶液中:c(HF)+c(Na+)+c(H+)-c(OH-)=2amol·L-1
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高三上学期期中考试化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数的数值,下列说法中正确的是
A.常温常压下,在空气中燃烧0.l molH2,转移的电子总数为0.2 NA
B.常温常压下,2.24 L NO和NO2混合气体中含有的氮原子数目为0.lNA
C.1.0 L的0.1 mol·L-lNa2S溶液中含有的S2-离子数为0.1 NA
D.标准状况下,22.4 L的CCl4中含有的CCl4分子数为NA。
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高三上学期第一次质量检测化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值,下列叙述正确的是 ( )
A.含有NA个氦原子的氦气在标准状况下的体积约为22.4 L
B.25℃,1.01×105 Pa,64 g SO2中含有的原子数为3NA
C.在常温常压下,11.2 L Cl2含有的分子数为0.5 NA
D.标准状况下,11.2 L H2O含有的分子数为0.5 NA
查看答案和解析>>
科目:高中化学 来源:2015届广东省高三9月月考化学试卷(解析版) 题型:选择题
下列化学用语或模型表示正确的是( )
A.Cl-离子的结构示意图: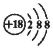 B.CCl4分子的球棍模型:
B.CCl4分子的球棍模型:
C.乙烯的结构简式 CH2CH2 D.H2O2的结构式:H—O—O—H
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com