
电池是人类生产和生活中重要的能量来源.各式各样电池的发明是化学对人类的一项重大贡献.下列有关电池的叙述正确的是()
A. 锌锰干电池工作一段时间后碳棒变细
B. 氢氧燃料电池可将热能直接转变为电能
C. 氢氧燃料电池工作时氢气在负极被氧化
D. 太阳能电池的主要材料是高纯度的二氧化硅
考点: 常见化学电源的种类及其工作原理.
专题: 电化学专题.
分析: A、根据锌锰干电池的正极是碳棒,该极上二氧化锰发生得电子的还原反应;
B、氢氧燃料电池是将化学能转化为电能的装置;
C、氢氧燃料电池中,燃料做负极发生失电子的氧化反应;
D、太阳能电池的主要材料是半导体硅.
解答: 解:A、在锌锰干电池中,正极是碳棒,该极上二氧化锰发生得电子的还原反应,该电极质量不会减少,故A错误;
B、氢氧燃料电池属于原电池的一种,是将化学能转化为电能的装置,不可将热能直接转变为电能,故B错误;
C、氢氧燃料电池中,燃料做负极,发生失电子的氧化反应,被氧化,故C正确;
D、太阳能电池的主要材料是半导体硅,不是二氧化硅,故D错误.
故选C.
点评: 本题考查锌锰干电池以及氢氧燃料电池的有关知识,属于基本知识的考查,难度不大.


科目:高中化学 来源: 题型:
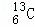 ﹣NMR(核磁共振)可用于含碳化合物的结构分析,
﹣NMR(核磁共振)可用于含碳化合物的结构分析,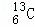 表示的是()
表示的是()
A. 核外有13个电子,其中6个能参与成键
B. 核内有6个质子,核外有7个电子
C. 质量数是13,原子序数是6,核内有7个质子
D. 质量数是13,原子序数是6,核内有7个中子
查看答案和解析>>
科目:高中化学 来源: 题型:
用10mL的0.1mol•L﹣1 BaCl2溶液恰好可使相同体积的硫酸铁(Fe2(SO4)3)、硫酸锌(ZnSO4)和硫酸钾(K2SO4)三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的物质的量浓度之比是()
A. 3:2:2 B. 1:2:3 C. 1:3:3 D. 3:1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
福岛核电站泄漏的放射性物质中含有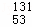 I,下列有关
I,下列有关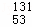 I的说法正确的是()
I的说法正确的是()
A. 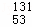 I是碘元素的一种同位素
I是碘元素的一种同位素
B. 由此可确定碘元素的相对原子质量为131
C. 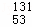 I核素中含中子数为53
I核素中含中子数为53
D. 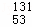 I2的摩尔质量为262 g
I2的摩尔质量为262 g
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学用语使用正确的是()
A. 氟化镁的电子式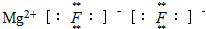
B. 用电子式表示硫化氢的形成过程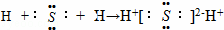
C. HClO的结构式 H﹣O﹣Cl
D. Cl﹣离子的结构示意图
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组性质比较中,正确的是()
①酸性:HClO4>HBrO4>HIO4
②离子还原性:S2﹣>Cl﹣>Br﹣>I﹣
③沸点:HF>HCl>HBr>HI
④金属性:K>Na>Mg>Al
⑤气态氢化物稳定性:HF>HCl>H2S
⑥半径:O2﹣>Na+>Na>Cl.
A. ①②③ B. ②③④ C. ①④⑤ D. ①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E、F为六种短周期元素,它们核电荷数依次递增.已知:B原子核外最外层电子数是次外层电子数的两倍,电子总数的2倍比E原子电子总数多1,F是同周期元素中原子半径最小的元素;D2﹣与E+的电子层结构相同.B与D可以形成三原子化合物甲.A是非金属元素,且A、C、F可形成离子化合物乙.请回答:
(1)C单质的电子式 ,F元素原子的电子排布式 [ B的电子排布图
(2)化合物乙中含有的化学键是 化合物乙为的阳离子的杂化类型 ,VSEPR构型是
(3)A、C形成化合物的VSEPR构型是 该物质是由 分子组成(填“极性”或“非极性”)
(4)ADE形成的化合物与F 单质反应的离子方程式
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com