
下列各单质及化合物之间的关系如下图,其中A为盐,C、M、N为日常生活中用途较广的金属单质,C是紫红色金属单质,常温下,可以用M或N制成的容器装运B的浓溶液,X具有磁性,B是工业上重要的化工原料。
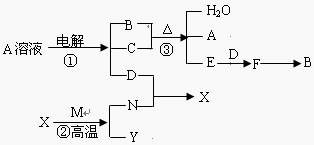
回答下列问题:
(1)N在周期表中的位置
(2)写出反应③的化学方程式
(3)写出反应①阳极的电极反应式 ,若阳极上析出的单质物质的量为0.01 mol,则阴极上析出的物质质量为 。
(4)工业生产中F→B反应是在 (填设备名称)中进行。
(5)写出反应②的化学方程式 ,若有16.8g的 N 生成,则转移的电子数为 。
科目:高中化学 来源: 题型:阅读理解
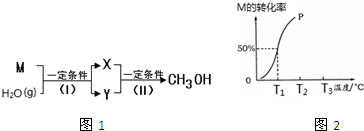
查看答案和解析>>
科目:高中化学 来源:2013-2014学年湖北省荆州市高三毕业班质量检查(二)理综化学试卷(解析版) 题型:填空题
如图表示各物质之间的转化关系。已知D、E、Z是中学化学常见的单质,其他都是化合物。Z、Y是氯碱工业的产品。D元素的原子最外层电子数与电子层数相等,且D的硫酸盐可作净水剂。E为日常生活中应用最广泛的金属。除反应①外,其他反应均在水溶液中进行。请回答下列问题。

(1)写出X的电子式:??????????? 。
(2)常温时pH =12的G溶液中,溶质的阳离子与溶质的阴离子浓度之差为?????????? (写出计算式)。
(3)在电镀工业中,若将E作为待镀金属,铜为镀层金属,则铜是____极,请写出在E电极上发生的电极反应式:????????????? 。
(4)写出反应③的离子方程式:??????????????????? 。
(5)现有无标签的Y和M的两种无色水溶液,不用其他任何试剂,请你设计一个简单的实验对这两种溶液加以鉴别???????????????? (回答实验操作、现象及结论)。
(6)A溶液与NaOH溶液混合可形成沉淀,某温度下此沉淀的Ksp =2.097×l0-39。将0.01 mol/L的A溶液与0.001 mol·L-1的NaOH溶液等体积混合,你认为能否形成沉淀____(填“能”或“不能”),请通过计算说明????????????????????????????? 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com