
【题目】2017年10月23日,十九大新闻中心在梅地亚举行以“践行绿色发展理念,建设美丽中国”为主题的记者招待会,聚焦环保话题。绿色化学是“预防污染”的根本手段,它的目标是研究和寻找能充分利用的无毒害原材料,最大限度地节约能源,在化工生产各个环节中都实现净化和无污染。
(1)在我国西部大开发中,某省为筹建一大型化工基地,征集到下列方案,其中你认为可行的是________。
A 建在西部干旱区可以脱贫致富
B 应建在水资源丰富和交通方便且远离城市的郊区
C 企业有权自主选择厂址
D 不宜建在人稠密的居民区
(2)某化工厂排放的污水中含有![]() 、
、![]() 、
、![]() 、
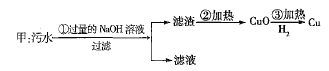
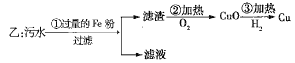
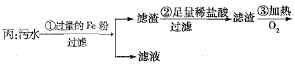
、![]() 四种离子。甲、乙、丙三位学生分别设计了从该污水中回收纯净的金属铜的方案。
四种离子。甲、乙、丙三位学生分别设计了从该污水中回收纯净的金属铜的方案。
![]()
在能制得纯铜的方案中,哪一步操作会导致环境污染?_______。应增加什么措施防止污染?_______。
【答案】BD 丙 方案的第③步增加冷凝回收装置
【解析】
(1)A.建在干旱山区缺乏水分不利于化工企业的运作,故A错误;
B.大型化工企业必须水源充足,交通方便,故B正确;
C.不能乱选择基地,必须保证水源充足,交通方便,不能污染居民,故C错误;
D.由于大型化工企业具有污染性,不能建在居民区附近,故D正确;
故选BD;
(2)方案甲:污水加入氢氧化钠后会生成多种难溶碱,主要有氢氧化铁、氢氧化镁和氢氧化铜等,因为这三种沉淀加热后均会分解生成氧化物和水,所以不能得到纯净的氧化铜,更不能得到纯净的铜;
方案乙:由于铁的活动性比铜和汞都强,所以污水中加入过量的铁粉时滤渣的成分除铜、汞外还含有剩余的铁,所以加热滤渣不会得到纯净的氧化铜,故也不能得到纯净的铜;
方案丙:由于铁的活动性比铜和汞都强,所以污水中加入过量的铁粉后得滤渣的成分主要是铜、汞和剩余的铁,滤渣中铜汞不能与与盐酸反应,而铁能反应,此时滤渣就变成了铜与汞的混合物,加热汞转化成汞蒸气挥发出来,铜与氧气反应生成了氧化铜,氧化铜采用氢气还原可得纯净的铜;
从方案丙的过程可以看出步骤③中是汞的污染环节,要想防止汞污染的产生就得需要对汞蒸气进行处理,以防止汞蒸气挥发到空气中导致污染,需要在第③步增加冷凝回收装置。


科目:高中化学 来源: 题型:
【题目】一定温度下,向氨水中通入![]() ,得到含有
,得到含有![]() 、
、![]() 等物质的溶液,溶液中部分微粒的物质的量分数与pH的关系如图所示。下列说法正确的是
等物质的溶液,溶液中部分微粒的物质的量分数与pH的关系如图所示。下列说法正确的是![]()

A.随着![]() 的通入,溶液中
的通入,溶液中 不断增大
不断增大
B.已知常温下,![]() 的
的![]() 溶液
溶液![]() ,则常温下
,则常温下![]()
C.![]() 溶液中存在关系:
溶液中存在关系:![]()
D.![]() 时,溶液中
时,溶液中![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国务院强调,“南水北调”工程必须坚持节水、治污和生态环境保护与工程建设相协调,以水资源合理配置为主线,把节水、治污和生态环境保护与调水作为一个完整的系统来分析的原则。在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大隐患。经检测,某工厂废液中含有大量的![]() 、
、![]() 、
、![]() 、
、![]() 。试分析并回答下列问题:
。试分析并回答下列问题:
(1)该废液中可能大量存在的阴离子是________(填序号)。
A ![]() B
B ![]() C
C ![]() D
D ![]()
(2)为了回收废液中的金属银,某同学设计了如图所示的实验方案。若按照该方案获得金属银108g,在保证不污染环境且![]() 循环利用的情况下,可得出理论上应提供标准状况下的
循环利用的情况下,可得出理论上应提供标准状况下的![]() ________L。
________L。
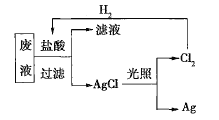
(3)为了实现(2)中氯气的循环利用,有人设想以氢气和氯气为原料利用原电池原理直接制盐酸,假设这种想法可行,下列说法肯定错误的是________(填序号)。
A 两极材料都用石墨,用稀盐酸作电解质溶液
B 通入氢气的电极为原电池的正极
C 电解质溶液中的阳离子向通入氯气的电极移动
D 通入氯气的电极的电极反应式为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种高效安全的杀菌消毒剂。用氯化钠电解法生成ClO2的工艺原理示意图如图,发生器内电解生成ClO2。下列说法正确的是( )
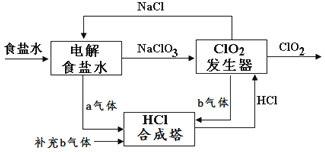
A.a气体是氯气,b气体是氢气
B.为使a、b气体恰好完全反应,理论上每生产1molClO2需要补充56L(标准状况)b气体
C.ClO2发生器中的还原反应为:2ClO3-+12H++10e-=Cl2↑+6H2O
D.氯化钠电解槽内每生成2mola气体,转移2mole-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于有机物的叙述正确的是( )
A.丙烷的二卤代物是4种,则其六卤代物是2种
B.某烃的同分异构体只能形成一种一氯代物,其分子式一定为C5H12
C.甲苯苯环上的一个氢原子被含3个碳原子的烷基取代,所得产物有6种
D.对二甲苯的核磁共振氢谱显示有3种不同化学环境的氢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳是地球上组成生命的最基本的元素之一。按要求回答:
(1)碳原子核外有________种不同空间运动状态的电子,第一电离能介于B和C之间的元素的名称为_________。
(2)碳元素能形成多种无机物。
①CO32-的立体构型是_______________。
②MgCO3分解温度比CaCO3低的原因是_________________________。
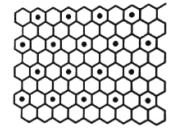
③石墨与钾可形成石墨夹层离子晶体C8K(如图),其结构为每隔一层碳原子插入一层钾原子,与钾原子层相邻的上下两层碳原子排列方式相同,则与钾最近等距的配位碳原子有_________个。
(3)碳也可形成多种有机化合物,下图所示是一种嘌呤和一种吡啶的结构,两种分子中所有原子都在一个平面上。
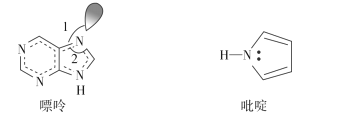
①1 mol 吡啶分子中含有σ键数目是__________。
②嘌呤结构中N原子的杂化方式为________。
③嘌呤中轨道之间的夹角∠1比∠2大,解释原因________________________________。
(4)将立方金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元取代可形成碳的一种新型三维立方晶体结构——T-碳。已知T-碳密度为ρ g/cm,阿伏加德罗常数为NA,则T-碳的晶胞参数a=________ pm (写出表达式即可)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一固体混合物,可能由![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 混合而成,为检验它的成分,做了如下实验:
混合而成,为检验它的成分,做了如下实验:![]() 已知
已知![]() 不能被稀
不能被稀![]() 氧化,
氧化,![]() 微溶于水
微溶于水![]()
![]() 将固体溶于足量水,搅拌后静置,得到无色透明溶液和白色沉淀;
将固体溶于足量水,搅拌后静置,得到无色透明溶液和白色沉淀;
![]() 取等量固体加入足量的稀硝酸中,有刺激性气味黄绿色气体产生,同时有白色沉淀生成。根据以上实验现象,你认为以下判断正确的是
取等量固体加入足量的稀硝酸中,有刺激性气味黄绿色气体产生,同时有白色沉淀生成。根据以上实验现象,你认为以下判断正确的是![]()
![]()
A.一定含有![]() 、
、![]() 、
、![]()
B.无法判断是否含有![]()
C.一定含有![]() 、
、![]() 、
、![]() ,不能肯定是否含有
,不能肯定是否含有![]()
D.是否含![]() ,只要把实验
,只要把实验![]() 产生的气体通入少量澄清石灰水中,若没有变浑浊,则一定不含
产生的气体通入少量澄清石灰水中,若没有变浑浊,则一定不含![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,CH3COOH的电离平衡常数Ka=1.75×10-5,NH3·H2O的电离平衡常数Kb=1.75×10-5,现在25 ℃时向10 mL浓度均为0.1 mol·L-1的HCl和CH3COOH的混合溶液中逐滴加入0.1 mol·L-1的氨水,溶液的pH变化曲线如图所示。下列有关说法不正确的是( )
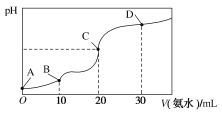
A.A点到B点,溶液的导电性逐渐减小
B.整个过程中,C点处水的电离程度最大
C.pH =7时对应的点应在C点和D点之间,此时溶液中存在:c(NH4+)=c(CH3COO-)+c(CH3COOH)
D.D点处:c(NH4+)>c(Cl-)>c(CH3COO-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机物结构,性质和应用的说法中,不正确的是![]()
![]()
A.环己烷与溴混合振荡后,在光照条件下可以发生取代反应
B.裂化汽油可以使溴水褪色和酸性![]() 褪色,且原理相同
褪色,且原理相同
C.苯的二氯代物、四氯代物的同分异构体数相等
D.燃烧等物质的量的乙烯、乙醇,消耗氧气的量相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com