
【题目】碳是地球上组成生命的最基本的元素之一。按要求回答:
(1)碳原子核外有________种不同空间运动状态的电子,第一电离能介于B和C之间的元素的名称为_________。
(2)碳元素能形成多种无机物。
①CO32-的立体构型是_______________。
②MgCO3分解温度比CaCO3低的原因是_________________________。
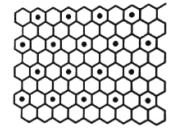
③石墨与钾可形成石墨夹层离子晶体C8K(如图),其结构为每隔一层碳原子插入一层钾原子,与钾原子层相邻的上下两层碳原子排列方式相同,则与钾最近等距的配位碳原子有_________个。
(3)碳也可形成多种有机化合物,下图所示是一种嘌呤和一种吡啶的结构,两种分子中所有原子都在一个平面上。
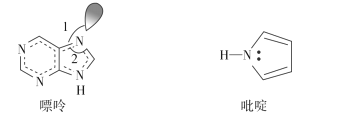
①1 mol 吡啶分子中含有σ键数目是__________。
②嘌呤结构中N原子的杂化方式为________。
③嘌呤中轨道之间的夹角∠1比∠2大,解释原因________________________________。
(4)将立方金刚石中的每个碳原子用一个由4个碳原子组成的正四面体结构单元取代可形成碳的一种新型三维立方晶体结构——T-碳。已知T-碳密度为ρ g/cm,阿伏加德罗常数为NA,则T-碳的晶胞参数a=________ pm (写出表达式即可)。

【答案】4 铍 平面三角形 氧化镁晶格能比氧化钙大,使得镁离子比钙离子更容易结合碳酸根中的氧离子 12 10NA sp2 孤电子对与键合电子对之间的斥力大于键合电子对之间的斥力,斥力大,键角大 ![]() ×1010
×1010
【解析】
(1)碳原子核外有6个电子,电子排布式为1s22s22p2,据此判断不同空间运动状态的电子数目;同周期主族元素随原子序数增大第一电离能呈增大趋势,ⅡA族、VA族第一电离能高于相邻元素,据此结合元素周期表分析解答;
(2)①CO32-中C的价层电子对数=3+![]() =3,据此分析判断;
=3,据此分析判断;
②根据金属阳离子结合氧离子的能力大小分析解答;
③根据石墨与钾可形成石墨夹层离子晶体C8K的结构图,2层碳原子中插入一层钾原子,与钾最近等距的碳原子有上下2层中对应的2个六边形,据此判断;
(3)①1个单键为1个σ键,1个双键为1个σ键和1个π键,根据吡啶(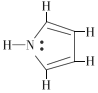 )的结构分析判断;
)的结构分析判断;
②嘌呤分子为平面结构,N形成3根共价键,根据杂化轨道理论分析判断;
③孤电子对与键合电子对之间的斥力>键合电子对与键合电子对之间的斥力,据此解答;
(4)根据图示计算一个T-碳晶胞中含有的碳原子数,从而计算1molT-碳晶胞的质量,结合T-碳的密度计算T-碳的晶胞参数a。
(1)碳原子核外有6个电子,电子排布式为1s22s22p2,其中2p上的3个原子轨道互相垂直,一共有4种不同空间运动状态的电子;同周期主族元素随原子序数增大第一电离能呈增大趋势,第ⅡA族、VA族满足全充满或半充满稳定状态,第一电离能高于同周期相邻元素的,第二周期中,第一电离能介于B元素和C元素间的元素是Be,名称为铍,故答案为:4;铍;
(2)①CO32-中C的价层电子对数=3+![]() =3,采用sp2杂化,立体构型为平面三角形,故答案为:平面三角形;
=3,采用sp2杂化,立体构型为平面三角形,故答案为:平面三角形;
②在离子晶体中,离子半径越小晶格能越大,所以在第ⅡA族金属碳酸盐中,阳离子半径越小对氧的吸引力越大,就越容易导致碳酸根的分解,所以在第ⅡA族中,随着原子序数的增加,原子半径增大,碳酸盐的分解温度也增大,所以MgCO3分解温度比CaCO3低,故答案为:氧化镁晶格能比氧化钙大,使得镁离子比钙离子更容易结合碳酸根中的氧离子;
③根据石墨与钾可形成石墨夹层离子晶体C8K的结构图,与钾最近等距的配位碳原子有上下2层中对应的2个六边形上的12个碳原子,故答案为:12;
(3)①1个单键为1个σ键,1个双键为1个σ键和1个π键,1 mol 吡啶( )分子中含有σ键数目是10NA,故答案为:10NA;
)分子中含有σ键数目是10NA,故答案为:10NA;
②嘌呤分子为平面结构,N形成3根共价键,根据杂化轨道理论,则N原子的杂化方式为sp2杂化,故答案为:sp2;
③根据VSEPR理论,孤电子对对键合电子对之间的斥力大于键合电子对对键合电子对之间的斥力,导致键合电子对与键合电子对之间的夹角减小,因此嘌呤中轨道之间的夹角∠1比∠2大,故答案为:孤电子对与键合电子对之间的斥力大于键合电子对之间的斥力,斥力大,键角大;
(4)一个金刚石晶胞中,含有C的数目为8×![]() +6×
+6×![]() +4=8,将每个C原子换成四面体结构的C,则T-碳晶胞中含有碳原子数目为8×4个,取1mol这样的晶胞,则有NA个这样的晶胞,则1molT-碳晶胞的质量为m=12×8×4g,T-碳密度为ρ g/ cm3,则1个晶胞的体积为
+4=8,将每个C原子换成四面体结构的C,则T-碳晶胞中含有碳原子数目为8×4个,取1mol这样的晶胞,则有NA个这样的晶胞,则1molT-碳晶胞的质量为m=12×8×4g,T-碳密度为ρ g/ cm3,则1个晶胞的体积为 =
=![]() cm3,则T-碳的晶胞参数a=
cm3,则T-碳的晶胞参数a=![]() cm =
cm =![]() ×1010pm,故答案为:
×1010pm,故答案为:![]() ×10span>10。
×10span>10。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某实验小组用下列装置进行乙醇催化氧化的实验。

(1)请写出装有铜网的试管中反应的化学方程式:___。
(2)不断鼓入空气,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化氧化反应是____反应(填“吸热”或“放热”)。
(3)甲和乙两个水浴作用不相同。甲的作用是___;乙的作用是___。
(4)反应进行一段时间后,集气瓶收集到的气体主要是___。
(5)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,要除去该物质,选择的试剂是__(填写字母):
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.金属钠
再通过___(填实验操作名称)即可得到乙醛。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.过量的100gNa2O2与CO2反应后,固体质量变成了105.6g,此反应转移电子为0.4mol
B.在Fe与含nmolHNO3的稀溶液反应中,被还原的HNO3不一定为![]() nmol
nmol
C.在Mg与Al做电极,其它溶液做电解质构成原电池中,Mg一定为负极
D.碱性氧化物一定为金属氧化物,酸性氧化物不一定是非金属氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲同学利用下图所示装置在实验室制备乙酸乙酯
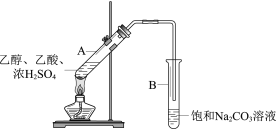
(1)实验中饱和Na2CO3溶液的作用是__________。
(2)分离出试管B中油状液体用到的主要仪器是_________________。
(3)乙醇和乙酸反应制乙酸乙酯是可逆反应。请根据化学平衡移动的相关知识写出一种增大乙酸乙酯产率的方法_________________。
(4)工业上用CH2=CH2和乙酸直接反应获得乙酸乙酯
①其反应类型是____。
②与实验室制法相比,工业制法的优点是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年10月23日,十九大新闻中心在梅地亚举行以“践行绿色发展理念,建设美丽中国”为主题的记者招待会,聚焦环保话题。绿色化学是“预防污染”的根本手段,它的目标是研究和寻找能充分利用的无毒害原材料,最大限度地节约能源,在化工生产各个环节中都实现净化和无污染。
(1)在我国西部大开发中,某省为筹建一大型化工基地,征集到下列方案,其中你认为可行的是________。
A 建在西部干旱区可以脱贫致富
B 应建在水资源丰富和交通方便且远离城市的郊区
C 企业有权自主选择厂址
D 不宜建在人稠密的居民区
(2)某化工厂排放的污水中含有![]() 、
、![]() 、
、![]() 、
、![]() 四种离子。甲、乙、丙三位学生分别设计了从该污水中回收纯净的金属铜的方案。
四种离子。甲、乙、丙三位学生分别设计了从该污水中回收纯净的金属铜的方案。
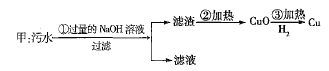
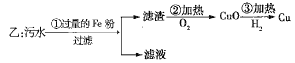
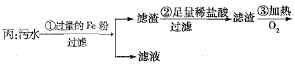
![]()
在能制得纯铜的方案中,哪一步操作会导致环境污染?_______。应增加什么措施防止污染?_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
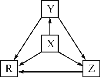
选项 | X | Y | Z | R |
A | Al | AlCl3 | Al(OH)3 | NaAlO2 |
B | Na | Na2O | Na2O2 | NaOH |
C | H2S | S | SO2 | SO3 |
D | N2 | NH3 | NO | NO2 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸亚铁(FeC2O4)可作为生产电池正极材料磷酸铁锂的原料,受热容易分解,为探究草酸亚铁的热分解产物,按下面所示装置进行实验。
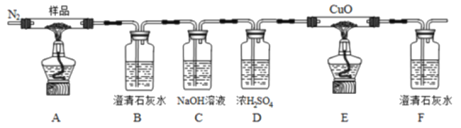
下列说法不正确的是
A.实验中观察到装置B、F中石灰水变浑浊,E中固体变为红色,则证明分解产物中有CO2和CO
B.反应结束后,取A中固体溶于稀硫酸,向其中滴加1~2滴KSCN溶液,溶液无颜色变化,证明分解产物中不含Fe2O3
C.装置C的作用是除去混合气中的CO2
D.反应结束后,应熄灭A,E处酒精灯后,持续通入N2直至温度恢复至室温
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1mol有机化合物A与标准状况下5.6L氧气混合,一定条件下两者完全反应,只有CO、CO2和H2O三种产物,将全部产物依次通入足量的浓硫酸和碱石灰中,浓硫酸增重5.4克,碱石灰增重4.4克,还有标准状况下2.24L气体的剩余,求:
(1)有机化合物A的分子式_______(要求写出推理过程);
(2)若有机化合物A能与钠反应放出氢气,请写出A的结构简式_________;
(3)写出所有比A多一个—CH2—原子团的同系物的结构简式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜的冶炼过程大致可分为:①富集,对硫化物矿进行浮选;②焙烧,主要反应为 (炉渣);③制粗铜,在1200℃下发生的主要反应为
(炉渣);③制粗铜,在1200℃下发生的主要反应为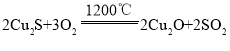 ,
, ;④电解精炼铜。下列说法不正确的是( )
;④电解精炼铜。下列说法不正确的是( )
A.上述焙烧过程的尾气回收后可用来制硫酸
B.上述过程中,由![]()
![]() 制取
制取![]()
![]() 共消耗
共消耗![]()
![]()
C.在反应 中,只有
中,只有![]() 作氧化剂
作氧化剂
D.电解精炼铜时,粗铜应与外接电源的正极相连
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com