
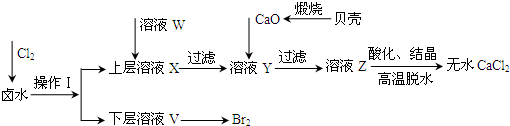
实验室以含有Mg2+、Cl—、Br—、SO42—等离子的卤水为主要原料制备Mg和Br2,流程如下:

(1)操作Ⅰ使用的试剂是 ;所用主要仪器的名称是 。
(2)为了使Mg2+转化为沉淀,试剂1可以选用 ;加入试剂1后,
能够分离得到Mg(OH)2沉淀的方法是 。
(3)试剂2可以选用 。
(4)请写出由无水MgCl2生成Mg的化学反应方程式 。
 应用题作业本系列答案
应用题作业本系列答案 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:阅读理解
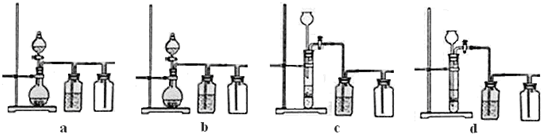
| 开始沉淀时的pH | 沉淀完全时的pH | |
| Mg2+ | 9.6 | 11.0 |
| Ca2+ | 12.2 | c(OH-)=1.8mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
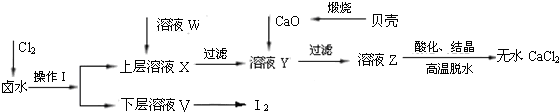

| 实验步骤 | 现象 | 结论 |
将SO2依次通过 NaHCO3或Na2CO3溶液、 酸性KMnO4溶液、 品红溶液、 澄清石灰水 将SO2依次通过 NaHCO3或Na2CO3溶液、 酸性KMnO4溶液、 品红溶液、 澄清石灰水 |
NaHCO3或Na2CO3溶液有气泡, 品红溶液不褪色, 澄清石灰水变浑浊 NaHCO3或Na2CO3溶液有气泡, 品红溶液不褪色, 澄清石灰水变浑浊 |
H2SO3酸性强于H2CO3 |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年河南省许昌市五校高一下学期第四次联考化学试卷(带解析) 题型:实验题
(8分)实验室以含有Mg2+、Cl—、Br—、SO42—等离子的卤水为主要原料制备Mg和Br2,流程如下: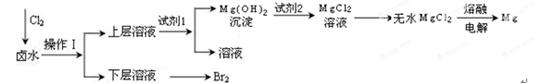
(1)操作Ⅰ使用的试剂是 ;所用主要仪器的名称是 。
(2)为了使Mg2+转化为沉淀,试剂1可以选用 ;加入试剂1后,能够分离得到Mg(OH)2沉淀的方法是 。
(3)试剂2可以选用 。
(4)请写出由无水MgCl2生成Mg的化学反应方程式 。
查看答案和解析>>
科目:高中化学 来源:2014届河南省许昌市五校高一下学期第四次联考化学试卷(解析版) 题型:实验题
(8分)实验室以含有Mg2+、Cl—、Br—、SO42—等离子的卤水为主要原料制备Mg和Br2,流程如下:
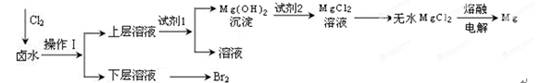
(1)操作Ⅰ使用的试剂是 ;所用主要仪器的名称是 。
(2)为了使Mg2+转化为沉淀,试剂1可以选用 ;加入试剂1后,能够分离得到Mg(OH)2沉淀的方法是 。
(3)试剂2可以选用 。
(4)请写出由无水MgCl2生成Mg的化学反应方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com