
某元素X的原子核外电子数等于核内中子数,取该元素的单质2.8g跟氧气充分作用,可得到6.0g化合物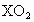 ,该元素在周期表中的位置是
,该元素在周期表中的位置是
[ ]
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:物理教研室 题型:021
某元素X的原子核外电子数等于核内中子数,取该元素的单质2.8g与氧气充分反应可得6g化合物 ,该元素在周期表中的位置
,该元素在周期表中的位置
[ ]
|
A.第二周期 |
B.第三周期 |
C.第ⅣA族 |
D.第ⅤA族 |
查看答案和解析>>
科目:高中化学 来源:高中化学同步单元练习册 全册 高二年级 题型:021
某元素X的原子核外电子数等于核内中子数,取2.8g此元素的单质与氧充分反应,可得6g 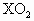 .有关元素X的说法正确的是
.有关元素X的说法正确的是
[ ]
A.X位于周期表中第二周期ⅤA族
B.X位于周期表中第三周期ⅣA族
C.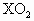 晶体熔点高,硬度大
晶体熔点高,硬度大
D.X的气态氢化物的水溶液呈强酸性
查看答案和解析>>
科目:高中化学 来源:教材完全解读:高中化学 2:(必修) (鲁科版课标版) 鲁科版课标版 题型:021
|
某元素X的原子核外电子数等于核内中子数,取该元素的单质2.8 g跟氧气充分作用,可得到6.0 g化合物XO2,该元素在周期表中的位置是 | |
A. |
第二周期,ⅣA族 |
B. |
第三周期,ⅣA族 |
C. |
第二周期,ⅥA族 |
D. |
第三周期,ⅥA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:021
某元素X的原子核外电子数等于核内中子数,取2.8g此元素的单质与氧充分反应,可得6g 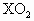 .有关元素X的说法正确的是
.有关元素X的说法正确的是
[ ]
A.X位于周期表中第二周期ⅤA族
B.X位于周期表中第三周期ⅣA族
C.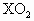 晶体熔点高,硬度大
晶体熔点高,硬度大
D.X的气态氢化物的水溶液呈强酸性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com