
已知一定温度和压强下,合成氨反应:N2(g)+3H2(g)===2NH3(g) ΔH=-92.0 kJ·mol-1,将1 mol N2和3 mol H2充入一密闭容器中,保持恒温恒压,在催化剂存在时进行反应,达到平衡时,测得N2的转化率为20%。若在相同条件下,起始时向该容器中充入2 mol NH3,反应达到平衡时的热量变化是( )
A.吸收18.4 kJ热量 B.吸收73.6 kJ热量
C.放出18.4 kJ热量 D.放出73.6 kJ热量
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
氯气是一种重要的化工原料。工业上常用反应:
3Cl2+8NH3===N2+6NH4Cl 检验氯气管道是否漏气。根据材料中的反应回答下列问题:
(1)氧化剂是 ,还原剂是 。
(2)氧化剂与被氧化的还原剂分子个数比为 。
(3)当有68 g NH3参加反应时,将会有 mol电子发生转移,被氧化的物质为________ g。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各项中,关于用途的说法不正确的是 ( )
A.75%(体积分数)的酒精溶液常用于医疗消毒
B.乙烯主要用于作燃料使用
C. 石油裂化的主要目的是为了得到轻质油
D.乙酸常用作调味剂
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中正确的是 ( )
A.1L水中溶解了58.5 g NaCl,该溶液的物质的量浓度为1mol/L
B.从1L2mol/L的H2SO4溶液中取出0.5L,该溶液的浓度为1mol/L
C.配制500mL0.2mol/L的CuSO4溶液,需25g胆矾
D.中和100mL1mol/L的H2SO4溶液,需NaOH4g
查看答案和解析>>
科目:高中化学 来源: 题型:
写出下列反应的离子方程式:
① 用稀硫酸清洗铁锈(Fe2O3)
② 将锌粒加入到稀硫酸中
③ NaHCO3溶液与盐酸混合
④ 向足量澄清石灰水中通入二氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
T ℃时在2 L的密闭容器中X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图(1)所示;若保持其他条件不变,反应温度分别为T1和T2时,Y的体积分数与时间的关系如图(2)所示。
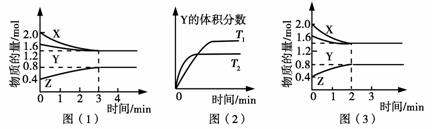
则下列结论正确的是( )
A.反应进行的前3 min内,用X表示的反应速率v(X)=0.3 mol·(L·min)-1
B.容器中发生的反应可表示为3X(g)+Y(g)2Z(g)
C.保持其他条件不变,升高温度,反应的化学平衡常数K减小
D.若改变反应条件,使反应进程如图(3)所示,则改变的条件是增大压强
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能用勒夏特列原理解释的是( )
A.由NO2和N2O4组成的平衡体系加压后颜色先变深后变浅
B.增大压强可加快SO2转化为SO3的速率
C.黄绿色的氯水光照后颜色变浅
D.在含有Fe(SCN)3的红色溶液中加铁粉,振荡静置,溶液颜色变浅或褪去
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法正确的是( )
A.CaCO3(s)===CaO(s)+CO2(g)室温下不能自发进行,说明该反应的ΔH<0
B.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈
C.N2(g)+3H(g)===2NH3(g) ΔH<0,其他条件不变时升高温度,反应速率v(H2)和H2的平衡转化率均增大
D.水的离子积常数Kw随着温度的升高而增大,说明水的电离是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
向四个体积相同的密闭容器(甲、乙、丙、丁)中分别充入一定量的SO2和O2,开始反应时,按反应速率由大到小排列顺序正确的是( )
甲:在500 ℃时,10 mol SO2和6 mol O2反应
乙:在500 ℃时,用V2O5作催化剂,10 mol SO2和5 mol O2反应
丙:在450 ℃时,8 mol SO2和5 mol O2反应
丁:在500 ℃时,8 mol SO2和5 mol O2反应
A.甲、乙、丙、丁 B.乙、甲、丙、丁
C.乙、甲、丁、丙 D.丁、丙、乙、甲
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com