
【题目】我国重晶石(含BaSO490%以上)资源丰富,其中贵州省重晶石储量占全国总储量的三分之一。我省某工厂以重晶石为原料,生产“电子陶瓷工业支柱”——钛酸钡(BaTiO3)的工艺流程如下:
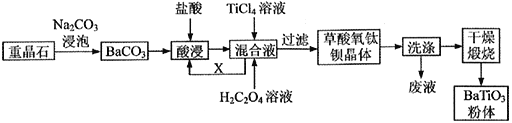
查阅资料可知:
①常温下: Ksp(BaSO4)=1.0×10-10,Ksp(BaCO3)=2.5×10-9
②TiC14在常温下是无色液体,遇水容易发生水解:TiCl4+2H2O=TiO2+4HCl。
③草酸氧钛钡的化学式为:BaTiO(C2O4)2·4H2O。
请回答下列问题:
(1)工业上用饱和Na2CO3溶液处理重晶石(假设杂质不与Na2CO3溶液作用),待达到平衡后,移走上层清液,重复多次操作,将BaSO4转化为易溶于酸的BaCO3,该过程用离子方程式可表示为___________,此反应的平衡常数K=____ (填写计算结果)。若不考虑CO32- 的水解,则至少需要使用_____mol/L 的Na2CO3溶液浸泡重晶石才能实现该转化过程。
(2)酸浸时所发生反应的离子方程式为___________________________________。
(3)配制TiCl4溶液时通常将TiCl4固体溶于浓盐酸再加水稀释,其目的是_____________________。
(4)可循环使用的物质X 是_________(填化学式),设计实验方案验证草酸氧钛钡晶体是否洗涤干净:_____________________________________________________________。
(5)煅烧草酸氧钛钡晶体得到BaTiO3的同时,高温下生成的气体产物有CO、__________和_________(填化学式)。
【答案】 BaSO4(s)+CO32-(aq)=BaCO3(s)+SO42-(aq) 0.04(或1/25) 2.5×10-4 BaCO3+2H+= Ba2++CO2↑+H2O 抑制TiCl4的水解 HCl 取最后一次洗涤液少许,滴入稀硝酸酸化的硝酸银,若无沉淀生成,则说明晶体已经洗涤干净 CO2 H2O(g)
【解析】(1)用饱和Na2CO3溶液将BaSO4转化为易溶于酸的BaCO3离子方程式为:BaSO4(s)+CO32-(aq)=BaCO3(s)+SO42-(aq),根据平衡常数的定义,结合方程式可知K=![]() =
=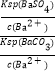 =0.04,饱和硫酸钡溶液中,SO42-浓度是1×10-5mol/L,所以此时CO32-浓度是1×10-5mol/L÷0.04=2.5×10-4mol/L;(2)酸浸时,碳酸钡与盐酸反应生成氯化钡、水、二氧化碳,离子反应为BaCO3+2H+=Ba2++CO2↑+H2O;(3)TiC14在常温下是无色液体,遇水容易发生水解可知,在配制为抑止其水解,需将TiCl4固体溶于浓盐酸再加水稀释;(4)向混合液中加入TiC14溶液和H2C2O4溶液反应得到草酸氧钛钡和HCl,故可循环使用的物质X 是HCl;草酸氧钛钡晶体表面附着氯离子,验证草酸氧钛钡晶体是否洗涤干净的方法为:取最后一次洗涤液少许,滴入稀硝酸酸化的硝酸银,若无沉淀生成,则说明晶体已经洗涤干净;(5)BaTiO(C2O4)24H2O煅烧,发生分解反应,由元素守恒可知,生成高温下的气体产物有CO、CO2、H2O(g)。
=0.04,饱和硫酸钡溶液中,SO42-浓度是1×10-5mol/L,所以此时CO32-浓度是1×10-5mol/L÷0.04=2.5×10-4mol/L;(2)酸浸时,碳酸钡与盐酸反应生成氯化钡、水、二氧化碳,离子反应为BaCO3+2H+=Ba2++CO2↑+H2O;(3)TiC14在常温下是无色液体,遇水容易发生水解可知,在配制为抑止其水解,需将TiCl4固体溶于浓盐酸再加水稀释;(4)向混合液中加入TiC14溶液和H2C2O4溶液反应得到草酸氧钛钡和HCl,故可循环使用的物质X 是HCl;草酸氧钛钡晶体表面附着氯离子,验证草酸氧钛钡晶体是否洗涤干净的方法为:取最后一次洗涤液少许,滴入稀硝酸酸化的硝酸银,若无沉淀生成,则说明晶体已经洗涤干净;(5)BaTiO(C2O4)24H2O煅烧,发生分解反应,由元素守恒可知,生成高温下的气体产物有CO、CO2、H2O(g)。


科目:高中化学 来源: 题型:
【题目】在Al2(SO4)3和MgSO4的混合溶液中,滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液的体积关系如右图所示,则原混合液中Al2(SO4)3与MgSO4的物质的量浓度之比为( )

A. 6:1 B. 3:1 C. 2:1 D. 1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列措施能加快Fe与0.1mol/L的稀H2SO4反应产生H2的反应速率的是( )
A.向溶液中再滴加1mol/L的HNO3B.将稀硫酸改为98%的浓硫酸
C.降低温度D.滴加少量的CuSO4 溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组设计了如图所示的电化学装置:下列说法不正确的是

A. 乙池工作时,CO32-不断移向负极
B. 乙池负极反应为CH30H-6e-+3CO32-=4CO2+2H2O
C. 甲池中Fe电极发生的反应为2Cl- -2e-=Cl2
D. 为了使电池持续供电,工作时必须有CO2参与循环
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酮洛芬是一种良好的抗炎镇痛药,可以通过以下方法合成:

(1)化合物D中所含官能团的名称为__________________和_____________________。
(2)化合物E的结构简式为__________________;由B→C的反应类型是____________。
(3)写出C→D的反应方程式____________________________________。
(4)B的同分异构体有多种,其中同时满足下列条件的有_____种。
I.属于芳香族化合物
II.能发生银镜反应
III.其核磁共振氢谱有5组波峰,且面积比为1:1:1:1:3
(5)请写出以甲苯为原料制备化合物![]() 的合成路线流程图____(无机试剂可任选)。合成路线流程图示例如图:
的合成路线流程图____(无机试剂可任选)。合成路线流程图示例如图:![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由乙烯的结构和性质推测丙烯(CH2=CH—CH3)的结构或性质正确的是
A. 不能使酸性高锰酸钾溶液褪色 B. 不能在空气中燃烧
C. 能使溴的四氯化碳溶液褪色 D. 易与Cl2在光照条件下发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列陈述Ⅰ、Ⅱ正确并且有因果关系的是( )
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | Fe3+有氧化性 | FeCl3溶液可用于回收废旧电路板中的铜 |
B | SiO2有导电性 | SiO2可用于制备光导纤维 |
C | SO2有漂白性 | SO2可使溴水褪色 |
D | 浓硫酸有强氧化性 | 浓硫酸可用于干燥H2和CO |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com