
【题目】已知烃A 的产量通常用来衡量一个国家的石油化工水平,现以A为主要原料合成一种具有果香味的物质E,其合成路线如下图所示。
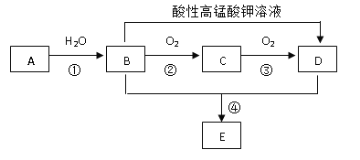
请回答下列问题:
(1)写出A的结构简式_________; A 、B 中官能团的名称和化学式__________;
(2)B→C的化学方程式为____________________,①,②反应类型为__________;
(3)B的结构式为____________________。若B中含有少量H2O,可加入_____________蒸馏除去。
(4)D与少量Na2CO3反应的离子方程式____________________。
(5)已知乙醇能发生如下脱水反应:CH3CH2OH+HOCH2CH3![]() CH3CH2OCH2CH3+ H2O,乙酸也能发生类似的脱水反应生成乙酸酐,写出该反应的化学方程式____________________。
CH3CH2OCH2CH3+ H2O,乙酸也能发生类似的脱水反应生成乙酸酐,写出该反应的化学方程式____________________。
【答案】CH2=CH2 碳碳双键![]() 、羟基 –OH 2 CH3CH2OH+O2
、羟基 –OH 2 CH3CH2OH+O2![]() 2 CH3CHO + 2H2O 加成反应,氧化反应
2 CH3CHO + 2H2O 加成反应,氧化反应 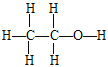 生石灰(或CaO) 2CH3COOH+CO32-→2CH3COO-+H2O+CO2↑ CH3COOH + CH3COOH →
生石灰(或CaO) 2CH3COOH+CO32-→2CH3COO-+H2O+CO2↑ CH3COOH + CH3COOH →![]() + H2O
+ H2O
【解析】
烃A的产量通常用来衡量一个国家石油化工水平,则A是乙烯,乙烯和水发生加成反应生成的B是乙醇,乙醇和氧气反应生成C,则C是乙醛,C进一步发生氧化反应生成的D为乙酸,乙醇与乙酸反应生成的E为乙酸乙酯。
(1)由上述分析可知A为乙烯,A的结构简式CH2=CH2,A中含有的官能团为碳碳双键![]() ,B为乙醇,B中官能团为羟基 –OH,因此本题正确答案是: CH2=CH2;碳碳双键
,B为乙醇,B中官能团为羟基 –OH,因此本题正确答案是: CH2=CH2;碳碳双键![]() 、羟基 -OH 。
、羟基 -OH 。
(2) B→C是乙醇发生氧化反应生成乙醛,反应方程式为: 2 CH3CH2OH+O2![]() 2 CH3CHO + 2H2O ;反应①是乙烯与水发生加成反应生成乙醇,反应②是乙醇发生氧化反应生成乙醛;答案:CH3CH2OH+O2
2 CH3CHO + 2H2O ;反应①是乙烯与水发生加成反应生成乙醇,反应②是乙醇发生氧化反应生成乙醛;答案:CH3CH2OH+O2![]() 2 CH3CHO + 2H2O ;加成反应;氧化反应。
2 CH3CHO + 2H2O ;加成反应;氧化反应。
(3)B为乙醇,B的结构式为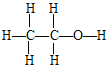 。若B中含有少量H2O,可加入生石灰CaO与水反应,CaO与乙醇不反应,进而蒸馏除去水。答案:
。若B中含有少量H2O,可加入生石灰CaO与水反应,CaO与乙醇不反应,进而蒸馏除去水。答案: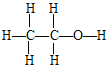 ;生石灰(或CaO)
;生石灰(或CaO)
(4)D为乙酸与少量Na2CO3反应的离子方程式:2CH3COOH+CO32-→2CH3COO-+H2O+CO2↑;答案:2CH3COOH+CO32-→2CH3COO-+H2O+CO2↑。
(5)已知乙醇能发生如下脱水反应:CH3CH2OH+HOCH2CH3![]() CH3CH2OCH2CH3+ H2O,乙酸也能发生类似的脱水反应生成乙酸酐,反应的化学方程式为:CH3COOH + CH3COOH →
CH3CH2OCH2CH3+ H2O,乙酸也能发生类似的脱水反应生成乙酸酐,反应的化学方程式为:CH3COOH + CH3COOH →![]() + H2O。
+ H2O。


 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案科目:高中化学 来源: 题型:
【题目】已知![]() 与足量的10mol/L硫酸液混合微热,产生下列现象:①有红色金属生成②产生刺激性气味的气体③溶液呈现蓝色。据此判断下列说法正确的是
与足量的10mol/L硫酸液混合微热,产生下列现象:①有红色金属生成②产生刺激性气味的气体③溶液呈现蓝色。据此判断下列说法正确的是
A. 反应中硫酸作氧化剂
B. ![]() 中硫元素被氧化
中硫元素被氧化
C. 刺激性气味的气体是氨气
D. 1mol![]() 完全反应转移0.5mol电子
完全反应转移0.5mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有五种化合物:①Mg(HCO3)2,②Al(OH)3,③Al,④(NH4)2CO3,⑤Al2O3。跟盐酸和NaOH溶液都能反应的物质有
A.二种B.三种C.四种D.五种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水开发利用的部分过程如图所示。下列说法错误的是

A. 向苦卤中通入Cl2是为了提取溴
B. 粗盐可采用除杂和重结晶等过程提纯
C. 工业生产中常选用NaOH作为沉淀剂
D. 富集溴一般先用空气和水蒸气吹出单质溴,再用SO2将其还原吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某可逆反应:2A(g)![]() B(g)+D(g)在密闭固定容积的容器中4种不同条件下进行,B和D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表:
B(g)+D(g)在密闭固定容积的容器中4种不同条件下进行,B和D的起始浓度均为0,反应物A的浓度随反应时间的变化情况如下表:
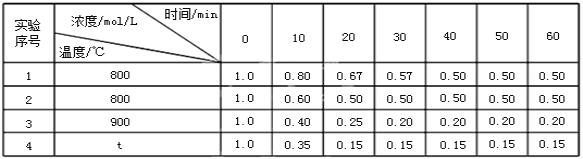
(1)实验1中,在10~20min内,以物质A表示的平均反应速率为_____。
(2)0~20min内,实验2比实验1的反应速率(“快”或“慢”)_____,其原因可能是_____。
(3)实验3比实验1的反应速率(填“快”或“慢”)_____,其原因可能是_____。
(4)从表中可以看出,t_____900(填“>”、“<”、“=”)。
(5)实验3中40分钟时υ(正)_____υ(逆)(填“>”、“<”、“=”)。
(6)实验4中50分钟时B的浓度为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 用湿润的pH试纸测定NaCl 溶液的pH时会影响测定结果
B. 检验某溶液含有NH4+:取试样少许于试管中,加入足量NaOH溶液加热,用湿润红色石蕊试纸检验变蓝
C. 液溴保存时液面覆盖一层水,装在带橡胶塞的细口试剂瓶中
D. 配制一定物质的量浓度的NaOH溶液时,NaOH固体溶解后未恢复到室温就定容,所配制的溶液浓度偏小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应C(s)+H2O(g)![]() CO(g)+H2(g)在一个体积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
CO(g)+H2(g)在一个体积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
①增加固体碳的量 ②保持压强不变,充入Ar使体系体积增大
②将容器压缩体积 ④保持体积不变,充入Ar使体系压强增大
A. ①③B. ①④C. ①②D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废气中氮氧化物(NO、NO2等,以通式NOx表示)是主要的大气污染物之一。
利用甲烷可消除NO2污染,CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g)。在1L密闭容器中,控制不同温度,分别加入0.50molCH4和0.80molNO2,测得n(CH4)随时间变化的有关实验数据见下表:
N2(g)+CO2(g)+2H2O(g)。在1L密闭容器中,控制不同温度,分别加入0.50molCH4和0.80molNO2,测得n(CH4)随时间变化的有关实验数据见下表:
组别 | 温度 | 时间/min | 0 | 10 | 20 | 40 | 50 | 60 |
① | T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 | 0.10 |
② | T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | …… | 0.15 | 0.15 |
回答下列问题:
(1)组别①中,0~10min内NO2的平均降解速率为v(NO2)= ________________。
(2)由实验数据可知实验控制的温度T2_____T1(填“>”或“<”),请简述理由__________。
(3)组别②中,T2温度下40min时n(CH4)=________mol。该反应正反应为_______反应(填“吸热”或“放热”),理由是_____________________________。
(4)温度T1时CO2物质的量随时间的变化如下图,在图中画出温度T2时CO2物质的量随时间的变化曲线________。

(5)汽车尾气中含有CO和NOx等多种有害气体,若在汽车的排气管上安装一种催化转化装置,可使CO与NOx反应,生成两种无毒气体,则该反应的化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关硅及其化合物的描述不正确的是( )
A.用二氧化硅和水反应可以制得H2SiO3
B.SiO2可用于制造光导纤维
C.普通玻璃是以纯碱、石灰石和石英为原料制成的
D.盛装NaOH溶液的试剂瓶不用玻璃塞的原因是因为玻璃塞与NaOH溶液反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com