
| A、直线形,三角锥形 |
| B、V形,三角锥形 |
| C、直线形,正四面体形 |
| D、V形,正四面体形 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、盐酸和氢氧化钾溶液的反应 |
| B、硝酸和氢氧化铜溶液的反应 |
| C、盐酸和澄清石灰水的反应 |
| D、硫酸和氢氧化钠溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,2.24L NH3和HF的混合物,所含电子总数为2NA |
| B、7gCnH2n中含氢原子数为nNA |
| C、0.1mol O22-所含的电子数为1.8NA |
| D、40g金刚砂中所含的共价键数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ca(OH)2═Ca2++2OH- |
| B、NaHCO3═Na++H++CO32- |
| C、KHSO4═K++H++SO42- |
| D、Al2(SO4)3═2Al3++3SO42- |
| E、Al2(SO4)3═2Al3++3SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
 |
 |
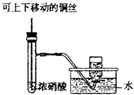 |
 |
| A、证明非金属性Cl>C>Si | B、吸收氨气,并防止倒吸 | C、制备并收集少量NO2气体 | D、制备少量氧气 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
| B、1-a% | ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向饱和硼酸溶液中滴加Na2CO3溶液,有CO2气体生成 |
| B、KClO3积SO3溶于水后能导电,故KClO3和SO3为电解质 |
| C、AgCl沉淀易转化为AgI沉淀且Ksp(AgX)=c(Ag+)?c(X-),故Ksp(AgI)<Ksp(AgCl) |
| D、沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com