
����Ŀ���״���һ�����͵���������ȼ�ϣ���ҵ�Ͽ�ͨ��CO��H2�������Ʊ��״���
��1����֪H2(g)��CO(g)��CH3OH(l)��ȼ���ȷֱ�Ϊ285.8kJ/mol��283.0kJ/mol��726.5kJ/mol����״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽΪ___��
��2��ij�о���ѧϰС�����ݻ��̶�Ϊ2L���ܱ������ڳ���1molCO��2molH2��������ʴ���(������Ժ��Բ���)����з�ӦCO(g)+2H2(g)=CH3OH(g) ��H<0��
�����д�ʩ������������÷�Ӧ�ķ�Ӧ���������ת���ʵ���__(����ĸ���)
A.��ʱ��CH3OH�뷴Ӧ�������� B.���ͷ�Ӧ�¶�
C.ʹ�ø�Ч���� D.������ϵѹǿ
��ʵ���������ѹ���Ƽ��������ѹǿ�ı仯���£�
��Ӧʱ��/min | 0 | 5 | 10 | 15 | 20 | 25 |
ѹǿ/MPa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
��ӷ�Ӧ��ʼ��20minʱ����H2��ʾ��ƽ����Ӧ����=__mol/(L��min)�����¶���ƽ�ⳣ��k=__��
�����ں��º�ѹ�����½���������Ӧ���ﵽƽ�������ϵ��ͨ��һ������ϡ�ͼ�(ˮ����)��CO��ת����__(��"����"��"��С"��"����")��
��3�������ݻ���Ϊ1L��a��b��c�����ܱ������зֱ����1molCO��2molH2�Ļ�����壬�����¶ȣ����з�Ӧ�����������ݵĹ�ϵ��ͼ��ʾ��b�м״������������a�е�ԭ����__���ﵽƽ��ʱ��a��b��c��CO��ת���ʴ�С��ϵΪ__��
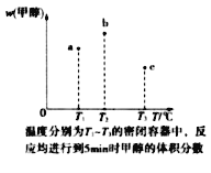
���𰸡�CH3OH(l)+O2(g)=CO(g)+2H2O(l) ��H=-443.5kJ/mol D 0.025 4 ��С b���¶ȸߣ���Ӧ���ʿ죬��Ӧ��ͬʱ�����ɵļ״��࣬��������� a>b>c
��������
��1������H2(g)��CO(g)��CH3OH(l)��ȼ���ȷֱ�Ϊ285.5kJ/mol��283.0kJ/mol��726.5kJ/mol��
д������ȼ���ȵ��Ȼ�ѧ����ʽ����д���״�����ȫȼ������һ����̼��Һ̬ˮ�Ļ�ѧ����ʽ�������ݸ�˹���ɼ����䷴Ӧ�ȣ�
��2��������ѧ��Ӧ���ʿ����£���ѹ��ʹ�ô���������Ӧ��Ũ�ȣ�����Ӧ���ȣ�ѹǿ��С����˽��£���ѹ�����ڷ�Ӧ������У���߷�Ӧ���ת���ʣ�
���г�����ʽ�����ݷ�Ӧʼĩ״̬��ѹǿ֮�ȵ������ʵ���֮�ȼ���ƽ��ʱH2��ת�������ٸ���![]() ���㷴Ӧ���ʣ��ݴ˼���ƽ��Ũ�ȣ��ٸ���ƽ��Ũ�ȼ��㻯ѧƽ�ⳣ����
���㷴Ӧ���ʣ��ݴ˼���ƽ��Ũ�ȣ��ٸ���ƽ��Ũ�ȼ��㻯ѧƽ�ⳣ����
�ۺ��º�ѹ�����£���Ӧ��ϵ��ͨ�������壬�൱�ڼ�Сѹǿ��
��3��δ�ﵽƽ��ǰ���¶ȸߵ����ʿ죬��ͬʱ���ڣ������ļ״����࣬��������Ӧ���ȣ�����ƽ����������¶ȣ�ƽ�����淴Ӧ�����ƶ����״��ĺ����ή�ͣ�����ͼ��5minʱ��a����һ��δƽ�⣬c����һ��ƽ�⣬b������һ��ƽ�⣬�ݴ˷������
��1����֪H2(g)��CO(g)��CH3OH(l)��ȼ���ȷֱ�Ϊ285.5kJ/mol��283.0kJ/mol��726.5kJ/mol��
������H2(g)+![]() O2(g)�TH2O(l) ��H1=285.5kJ/mol��
O2(g)�TH2O(l) ��H1=285.5kJ/mol��
��CO(g)+![]() O2(g)�TCO2(g) ��H2=283.0kJ/mol��
O2(g)�TCO2(g) ��H2=283.0kJ/mol��
��CH3OH(l)+![]() O2(g)�TCO2(g)+2H2O(l) ��H3=726.0kJ/mol��
O2(g)�TCO2(g)+2H2O(l) ��H3=726.0kJ/mol��
�״�����ȫȼ������һ����̼��Һ̬ˮ�Ļ�ѧ����ʽΪCH3OH(l)+O2(g)=CO(g)+2H2O(l)�����ݸ�˹���ɣ���֪�÷�Ӧ���ɢ��ڵõ����÷�Ӧ���ʱ���H=��H3��H2=443.5kJ/mol��
�ʴ�Ϊ��CH3OH(l)+O2(g)=CO(g)+2H2O(l) ��H=443.5kJ/mol��
��2����A. ��ʱ��CH3OH�뷴Ӧ�������룬ƽ�������ƶ�������߷�Ӧ���ת���ʣ�����ѧ��Ӧ���ʼ�С����A��ѡ��
B. ���ͷ�Ӧ���¶ȣ���ʹ��Ӧ������г̶�������߷�Ӧ��ת���ʣ�����ѧ��Ӧ���ʼ�С����B��ѡ��
C. ʹ�ø�Ч���������ѧ��Ӧ���ʣ������ı仯ѧƽ��״̬��������߷�Ӧ��ת���ʣ���C��ѡ��
D. ������ϵѹǿ��ƽ�������ƶ�������߷�Ӧ���ת���ʣ���������ѧ��Ӧ���ʣ���Dѡ��
�ʴ�Ϊ��D��
���ɱ��������ݿ�֪��20min��ѹǿ���ֲ��䣬��Ӧ�ﵽƽ��״̬���跴Ӧת��xmolCO����ɵ�����ʽ��
 ����ѹǿ֮�ȵ������ʵ���֮�ȣ�������
����ѹǿ֮�ȵ������ʵ���֮�ȣ�������![]() �����x=0.5����ӷ�Ӧ��ʼ��20minʱ����H2��ʾ��ƽ����Ӧ����=
�����x=0.5����ӷ�Ӧ��ʼ��20minʱ����H2��ʾ��ƽ����Ӧ����=![]() ������ֵ�ƽ��Ũ��Ϊc(CO)=0.25mol/L��c(H2)=0.5mol/L��c(CH3OH)=0.25mol/L�����Է�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ
������ֵ�ƽ��Ũ��Ϊc(CO)=0.25mol/L��c(H2)=0.5mol/L��c(CH3OH)=0.25mol/L�����Է�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ ��
��
�ʴ�Ϊ��0.025��4��
�����ں��º�ѹ�����½���������Ӧ���ﵽƽ�������ϵ��ͨ��һ������ϡ�ͼ�(ˮ����)�����ڷ�Ӧ��������Ũ�Ⱦ�ͬ�ȳ̶ȵļ�С���൱�ڼ�Сѹǿ��ƽ�������ƶ�����CO��ת���ʼ�С��
�ʴ�Ϊ����С��
��3��δ�ﵽƽ��ǰ���¶ȸߵ����ʿ죬��ͬʱ���ڣ������ļ״����࣬��������Ӧ���ȣ�����ƽ����������¶ȣ�ƽ�����淴Ӧ�����ƶ����״��ĺ����ή�ͣ�����ͼ��5minʱ��a����һ��δƽ�⣬c����һ��ƽ�⣬b������һ��ƽ�⣻�ﵽƽ��ʱ��a��b��c���������ķ�Ӧ�¶Ȳ�ͬ����������ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�������ƶ����ʴﵽƽ��ʱ��ת���ʵĹ�ϵΪ��a>b>c��
�ʴ�Ϊ��b���¶ȸߣ���Ӧ���ʿ죬��Ӧ��ͬʱ�����ɵļ״��࣬���������a>b>c��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£��ֱ�ȡŨ�Ȳ�ͬ�������Ϊ20.00mL��3��HCl��Һ���ֱ����Ũ��Ϊ1.000mol��L-1��0.1000mol��L-1��0.01000mol��L-1��NaOH��Һ�����3����Ӧ��ϵ��pH��V(NaOH)�ı仯��������ͼ����V(NaOH)=20.00mLǰ�����ͻԾ������˵������ȷ����
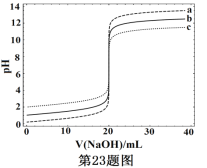
A. 3��HCl��Һ��c(HCl)����������С��100��
B. ����a��b��c��Ӧ��c(NaOH)��a>b>c
C. ��V(NaOH)=20.00mLʱ��3����ϵ�о����㣺c(Na+)=c(Cl-)
D. ��V(NaOH)��ͬʱ��pHͻԾ������ϵ�е�c(H+)���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͼ�е����ִ�������ԭ��������ͼ����������ʾ��Ԫ����������Ԫ�����ڱ��е�ʵ��λ���������(����)
A.  B.
B. 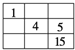 C.
C. 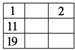 D.
D. 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijʵ��С��ѧ����50mL0.50mol/L��������50mL0.55mol/L��NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų������������к��ȡ�����˵����ȷ���ǣ� ��

A.��ͼ������ʵ�������û��������ʧ
B.ͼ��ʵ��װ��ȱ�ٻ��β��������
C.�ձ���������ֽ���������ǹ̶�С�ձ�
D.������60mL0.50mol/L������50mL0.55mol/L��NaOH��Һ���з�Ӧ����������˵���ⷴӦ����ֵ����ȵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���25 ��ʱijЩ�ε��ܶȻ�����������ĵ���ƽ�ⳣ��������˵����ȷ����
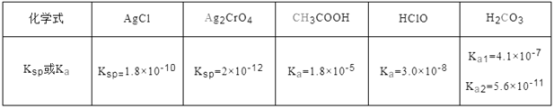
A. ��ͬŨ��CH3COONa��NaClO�Ļ��Һ�У�������Ũ�ȵĴ�С��ϵ��c(Na+)��c(ClO-)��c(CH3COO-)��c(OH-)��c(H+)
B. ̼������Һ�еμ�������ˮ�����ӷ���ʽH2O+2CO32-+Cl2===2HCO3-+Cl-+ClO-
C. ��0.1 mol��L-1CH3COOH��Һ�еμ�NaOH��Һ��c(CH3COOH):c(CH3COO-)=9:5����ʱ��ҺpH=5
D. ��Ũ�Ⱦ�Ϊ1��10-3mol��L-1��KCl��K2CrO4���Һ�еμ�1��10-3mol�� L-1��AgNO3��Һ��CrO42-���γɳ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ������У���һ����A��B�����Ϻ�����Ӧ��xA(g)+yB(g)![]() zC(g)+mD(s)��ƽ��ʱ��A��Ũ��Ϊ0.5mol/L�������¶Ȳ��䣬���������ݻ�����ԭ�����������ٴ�ƽ��ʱ�����A��Ũ��Ϊ0.3mol/L���������й��ж���ȷ���ǣ� ��
zC(g)+mD(s)��ƽ��ʱ��A��Ũ��Ϊ0.5mol/L�������¶Ȳ��䣬���������ݻ�����ԭ�����������ٴ�ƽ��ʱ�����A��Ũ��Ϊ0.3mol/L���������й��ж���ȷ���ǣ� ��
A. x+y>z+m B. B��ת����һ����С C. ƽ��������Ӧ�����ƶ� D. ���������ܶ�һ����С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������װ�����ϵ��ʵ�飬����˵����ȷ���ǣ� ��

A. ͭ��Ũ����ķ�Ӧ��ͭ��Ũ����ķ�Ӧһ����Ҫ���������²��ܽ���
B. BaCl2��Һ�л���ְ�ɫ����BaSO3
C. H2S��Һ�л���ֻ�ɫ������������SO2�Ļ�ԭ��
D. Ϊ��֤̼����ǽ����Ե����ǿ����A�Թ��е��Լ�������KMnO4��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij̽����ѧϰС������H2C2O4��Һ������KMnO4��Һ֮��ķ�Ӧ��̽����������ı�Ի�ѧ��Ӧ���ʵ�Ӱ�졣ʵ�������ʾ�������й�˵������ȷ���ǣ� ��
ʵ�� ��� | ʵ���¶�/K | ����KMnO4��Һ | H2C2O4��Һ | H2O | ��Һ������ɫʱ����ʱ��/s | ||
V/mL | c/mol��L-1 | V/mL | c/mol��L-1 | V/mL | |||
A | 293 | 2 | 0.02 | 5 | 0.1 | 3 | t1 |
B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
C | 313 | 2 | 0.02 | V2 | 0.1 | 5 | t1 |
A.����KMnO4��Һʱ����ϡ�����ữ
B.��t1<8�����ͨ�����Ʊ�������ʵ��A��B̽��H2C2O4Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�첢�ó����ۣ�����Ӧ��Ũ�ȣ���ѧ��Ӧ���ʼӿ�
C.��span>T1=293K��V1 =V2=3mL�����ͨ��ʵ��B��C̽���¶ȶԻ�ѧ��Ӧ���ʵ�Ӱ��
D.����ʵ��B�����ݼ��㣬��KMnO4��Ũ�ȱ仯��ʾ�Ļ�ѧ��Ӧ����v��KMnO4��=5��10-4mol��L-1��s-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ʽ��NaHY��ˮ��Һ�Լ��ԣ�����������ȷ���ǣ� ��
A.H2Y�ĵ��뷽��ʽΪ��H2Y![]() 2H����Y2��
2H����Y2��
B.HY����ˮ�ⷽ��ʽΪ��HY����H2O![]() H3O����Y2��
H3O����Y2��
C.����ʽ����Һ������Ũ�ȹ�ϵΪ��c(Na��)��c(HY��)��c(OH��)��c(H��)��c(Y2��)
D.����ʽ����Һ������Ũ�ȹ�ϵΪ��c(Na��)��c(Y2��)��c(HY��)��c(OH��)��c(H��)
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com