
��֪��P4(s)��6Cl2(g)��4PCl3(g) ��H��akJ��mol��1
P4(s)��10Cl2(g)��4PCl5(g) ��H�� bkJ��mol��1
P4������������ṹ��PCl5��P��Cl���ļ���ΪckJ��mol��1,PCl3��P��Cl���ļ���Ϊ1.2ckJ��mol��1 ����������ȷ����( )
A��P��P���ļ��ܴ���P��Cl���ļ���
B������Cl2(g)��PCl3(g)��PCl5(s)�ķ�Ӧ�Ȧ�H
C��Cl��Cl���ļ���(b-a+5.6c)/4kJ��mol��1
D��P��P���ļ���Ϊ(5a-3b+12c)/8kJ��mol��1
 �����������һ��һ��ϵ�д�
�����������һ��һ��ϵ�д� Ӧ������ҵ��ϵ�д�
Ӧ������ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016�������ʡ������12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����ȷ��ʾ���з�Ӧ�����ӷ���ʽ��
A�����⻯�Ƶ�ˮ�ⷴӦ HS�� + H2O  S2��+H3O+
S2��+H3O+
B��̼������������ NaOH ��Һ��Ӧ Ca2++2HCO3��+2OH�� = CaCO3��+2H2O+CO32��
C��Na2O2��H2O��Ӧ�Ʊ�O2 Na2O2 + H2O �� 2Na+ + 2OH�� + O2��
D����̼������Һ�м��������� CO32��+2H+ = H2O+CO2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʦ���С��ٴ�һ�и����ϵ�һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
���и������ӻ�����ܴ������棬��������Ӧ�Լ���ᷢ����ѧ�仯���ҷ�����Ӧ�����ӷ���ʽ��д��ȷ����
ѡ�� | ������ | �����Լ� | �����Լ�������Ӧ�����ӷ���ʽ |
A | NH4+��Fe2����SO42- | ����Ba(OH)2��Һ | 2NH4+��SO42-��Ba2����2OH��===BaSO4����2NH3��H2O |
B | Mg2����HCO3-��Cl�� | ����NaOH��Һ | Mg2����2HCO3-��4OH��=== 2H2O��Mg(OH)2����2CO32- |
C | K����NH3��H2O��CO32- | ͨ������CO2 | 2OH����CO2===CO32-��H2O |
D | Fe2����NO3-��SO32- | NaHSO4��Һ | SO32-��2H��===SO2����H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�������һ�и�һ��ѧ�ڵڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵������ȷ����
A��H2SO4 ��Ħ�������� 98 g B��1 mol H2O �������� 18 g/mol
C��Cl-��Ħ�������� 35.5 g/mol D��1 mol N2 ������� 22.4 L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ��һ��ѧ��12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���ΪV(mL)���ܶ�Ϊ��(g��cm��3)����Һ������Ħ������ΪM����������Ϊm(g)�����ʵ���Ũ��Ϊc����������Ϊw�����б���ʽ�в���ȷ����
A��c��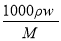 B��m��V���ѡ�
B��m��V���ѡ� C��w��
C��w��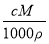 D��c��
D��c��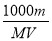
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ�߶���ѧ��12���¿���ѧ�Ծ�����ʦ�棩 ���ͣ�ѡ����
ij�ɳ�������ӵ����LiMn2O4Ϊ������Ƕ��﮵�̼����Ϊ��������Li+�������Ϊ����ʡ��ŵ�ʱ�ĵ�ط�ӦΪ��Li+LiMn2O4==Li2Mn2O4������˵����ȷ����
A���ŵ�ʱ��LiMn2O4����������Ӧ
B���ŵ�ʱ������ӦΪ��Li++LiMn2O4+e-==Li2Mn2O4
C�����ʱ��LiMn2O4����������Ӧ
D�����ʱ������ӦΪ��Li++e-==Li
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�꽭��ʡ������ѧ�ڵ����ο������ۻ�ѧ�Ծ��������棩 ���ͣ������
�Թ�ҵ��ˮ��������ˮ���д����Ƿ�ֹˮ����Ⱦ������ˮ�ʵ���Ҫ��ʩ��
��1�������ˮ�е�CN���о綾��
��CN����CԪ����+2�ۣ� NԪ����-3�ۣ���ԭ�ӽṹ����NԪ���Ը��۵�ԭ����
��������������£�CN���ܹ�������������HCO3-��ͬʱ����NH3���÷�Ӧ�����ӷ���ʽΪ ��
��2���������ƺͶ��ȷ�( ���ķ�ˮ�������������س�ȥ����ԭ������ͼ��ʾ��
���ķ�ˮ�������������س�ȥ����ԭ������ͼ��ʾ��
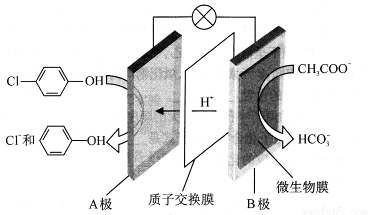
��B�ǵ�ص� �����������������
��A���ĵ缫��ӦʽΪ ��
��3��������������������������Һ��ͬʱ�õ������ԭ������ͼ��ʾ��ͼ�С�HA����ʾ������ӣ�A- ��ʾ��������ӣ���
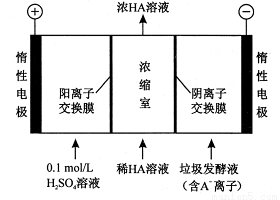
�������ĵ缫��ӦʽΪ
�ڼ���Ũ�����еõ�Ũ�����ԭ����
�۵������У���ȡһ����ʩ�ɿ���������pHԼΪ6-8����ʱ����Ũ���ҵ�OH-�ɺ��Բ��ơ�
400mL 10 g•L-1������Һͨ��һ��ʱ���Ũ������Ϊ145 g•L-1����Һ����仯���Բ��ƣ��������ϲ�����H2�ڱ�״���µ����ԼΪ L���������Ħ������Ϊ90 g• mol-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡ�����и�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ұ���ʾ������Ԫ���У�W��X��Y��ZΪ������Ԫ�أ�WԪ�صĺ˵����ΪXԪ�ص�2��������˵���������
X | Y | ||
W | Z | ||
T |
A����̬�⻯���ȶ��ԣ�Z > W
B�������Ӱ뾶��X < Y
C��Һ̬WZ4������˷����Ӽ�������
D������Ԫ�������ɣ������Ʋ�TԪ�صĵ��ʾ��а뵼������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���Ĵ�ʡ��һ����ĩģ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
���и��������У�����ͬһ��Һ�д������棬����һС���ƺ����ܴ����������
A��Na+��K+��Cl-��CO32- B��Cu2+��Na+��SO42-��CO32-
C��Ba2+��K+��Cl-��SO42- D��K+��Na+��HCO3-��NO3-
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com