
����Ŀ�����з����п���˵��2HI(g)![]() H2(g)+I2(g)�Ѵﵽƽ����ǣ��ٵ�λʱ��������n mol H2��ͬʱ����n mol HI����һ��H�CH�����ѵ�ͬʱ������H�CI�����ѣ��۰ٷ������(HI)=��(I2)���ܷ�Ӧ������(H2)=��(I2)=1/2��(HI)ʱ���� c(HI):c(H2):c(I2)=2:1:1ʱ�����¶Ⱥ����һ��ʱ��������ѹǿ���ٱ仯�����¶Ⱥ����һ��ʱ��ijһ������Ũ�Ȳ��ٱ仯��������һ������������ƽ����Է����������ٱ仯�����¶Ⱥ����һ��ʱ������������ɫ���ٱ仯�����¶Ⱥ�ѹǿһ��ʱ�����������ܶȲ��ٱ仯���� ��
H2(g)+I2(g)�Ѵﵽƽ����ǣ��ٵ�λʱ��������n mol H2��ͬʱ����n mol HI����һ��H�CH�����ѵ�ͬʱ������H�CI�����ѣ��۰ٷ������(HI)=��(I2)���ܷ�Ӧ������(H2)=��(I2)=1/2��(HI)ʱ���� c(HI):c(H2):c(I2)=2:1:1ʱ�����¶Ⱥ����һ��ʱ��������ѹǿ���ٱ仯�����¶Ⱥ����һ��ʱ��ijһ������Ũ�Ȳ��ٱ仯��������һ������������ƽ����Է����������ٱ仯�����¶Ⱥ����һ��ʱ������������ɫ���ٱ仯�����¶Ⱥ�ѹǿһ��ʱ�����������ܶȲ��ٱ仯���� ��
A. �ڢۢ� B. �٢ܢ� C. �ڢߢ� D. ����

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ǿ�����ڡ�2018�����Ժ�����������桷��ǿ����������������������ŷ���Ҫ�½�3%�����о�����������(��NOx)������(��SO2)���Ż����Ļ������塣
��. �����������ϰ�װ����ת���������䷴Ӧ���Ȼ�ѧ����ʽΪ��2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) ��H=-746.50kJ��mol-1��T��ʱ���������ʵ�����NO��CO�����ݻ�Ϊ2L���ܱ������У����¶Ⱥ�������䣬��Ӧ������(0~15min) NO�����ʵ�����ʱ��仯��ͼ��
2CO2(g)+N2(g) ��H=-746.50kJ��mol-1��T��ʱ���������ʵ�����NO��CO�����ݻ�Ϊ2L���ܱ������У����¶Ⱥ�������䣬��Ӧ������(0~15min) NO�����ʵ�����ʱ��仯��ͼ��
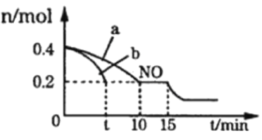
��1��ͼ��a��b�ֱ��ʾ����ͬ�¶��£�ʹ��������ͬ���������ͬ�Ĵ���ʱ���ﵽƽ�������n (NO)�ı仯���ߣ����б�ʾ����������ϴ��������______������a������b����
��2����a������ʾ��Ӧ�У�0~10min�ڣ�CO��ƽ����Ӧ����v(CO)=___________��T��ʱ���÷�Ӧ�Ļ�ѧƽ�ⳣ��K=_____________��ƽ��ʱ�������¶Ȳ��䣬���������г���CO��CO2��0.2 mol����ƽ�⽫_________�ƶ�(����������������������������)
��3��15minʱ, n (NO)����ͼ����ʾ�仯����ı������������_______������ţ�
A����������CO B.��N2Һ���Ƴ���ϵ C.�����¶� D.�������
��. ��֪�����з�Ӧ��
��5O2(g)+ 4NH3(g)![]() 6H2O(g)+ 4NO(g) ��H1
6H2O(g)+ 4NO(g) ��H1
��N2(g)+O2(g)![]() 2NO(g) ��H2
2NO(g) ��H2
��2NO(g)+ O2(g)![]() 2NO2(g) ��H3
2NO2(g) ��H3
��1�����ڸ�Ч���������¿ɷ���8NH3(g)+ 6NO2(g)![]() 7N2(g)+ 12H2O(g)�ķ�Ӧ����NO2���д�����÷�Ӧ�ġ�H=__________���á�H1����H2����H3��ʾ������S______0
7N2(g)+ 12H2O(g)�ķ�Ӧ����NO2���д�����÷�Ӧ�ġ�H=__________���á�H1����H2����H3��ʾ������S______0
��2��ij�¶��£���ij�����ܱ������г���һ������NH3��NO2�����գ�1����ԭ��ģ����Ⱦ��Ĵ������������й۲쵽________________������ţ������жϸ÷�Ӧ�ﵽƽ��״̬
A�����������ɫ���ٸı� B. ���������ܶȲ��ٸı�
C���������Ħ���������ٸı� D. NH3��NO2�����ʵ���֮�Ȳ��ٸı�
��3����һ��������O2��NH3��NO2�Ļ�����壬����ͨ��ͼ(a)��ʾװ�д���M�ķ�Ӧ���г�ֽ��з�Ӧ��
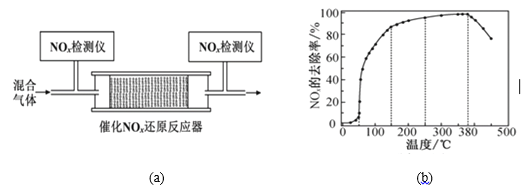
��Ӧ��ͬʱ��NOx��ȥ�����淴Ӧ�¶ȵı仯������ͼ(b)��ʾ����֪�ô�����100��150��ʱ������ߣ���ô��50��250 ����Χ�������¶ȵ����ߣ�NOx��ȥ������Ѹ����������������������ȥ����Ѹ�������ε���Ҫԭ����____________________________������Ӧ�¶ȸ���380 ��ʱ��NOx��ȥ����Ѹ���½���ԭ�������___________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2SO2(g)+O2(g) =2SO3(g)��Ӧ���̵������仯��ͼ��ʾ����֪1mol SO2(g)����Ϊ1mol SO3�� ��H=��99kJ��mol-1.��ش��������⣺
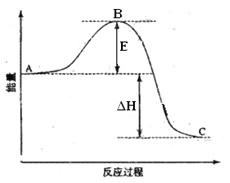
��1��ͼ��A��C�ֱ��ʾ �� ��
E�Ĵ�С�Ը÷�Ӧ�ķ�Ӧ������Ӱ�죿 ���÷�Ӧͨ����V2O5����������V2O5��ʹͼ��B�������ǽ��ͣ� ��������
��2��ͼ����H= KJ��mol-1��
��3��V2O5�Ĵ�ѭ����������Ϊ��V2O5����SO2ʱ����������ԭΪ�ļ۷�������ļ۷��������ٱ�����������д���ô�ѭ�������Ļ�ѧ����ʽ��
��
��
��4�������Ӧ��������SO2��Ϊ0.05 mol��L-1��min-1
,������O2��= mol��L-1��min-1��
��(SO3)= mol��L-1��min-1��
��5����֪�������ȼ����Ϊ296 KJ��mol-1������S(s)����3 molSO3(g)����H= ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E�������ʻ������֮����ת����ϵ����ͼ��ʾ��AΪ�ؿ��к������������ķǽ���Ԫ�صĵ��ʡ�
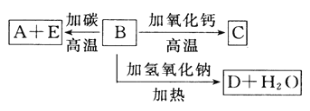
����գ�
(1)�γɵ���A��ԭ�ӵĽṹʾ��ͼΪ______����������ϼ�Ϊ______��
(2)B�Ļ�ѧʽ(����ʽ)Ϊ______��B��̼��Ӧ����A��E�Ļ�ѧ����ʽ��____________��
(3)C�Ļ�ѧʽ(����ʽ)Ϊ___________��D�Ļ�ѧʽ(����ʽ)Ϊ_____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ʯī�ͽ��ʯȼ�ջ�ѧ����ʽ���£�
C��ʯī��s��+O2��g��==CO2��g��
C�����ʯ��s��+O2��g��==CO2��g��
�����ֱ�Ϊ12 g��ʯī�ͽ��ʯ��ijһ��ͬ������ȼ��ʱ�ų��������ֱ�Ϊ393.8 kJ��395.2 kJ���ʣ����ڵ�����˵���ȶ��ĵ�����ʯī���ǽ��ʯ���������ɡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������һ�ֳ�����ǿ�����������������������ƽ���������������Ϣ�ش�����:
��֪:�ٸ���������ȷֽ�ΪN2��Cl2��O2��H2O;��Mg3N2��ˮ��;��Cu��N2�ھƾ��Ƽ��������²���Ӧ��
��1��д������������ȷֽ�Ļ�ѧ��Ӧ����ʽ: _____________��Mg3N2�ĵ���ʽΪ________��
��2������23.5g NH4ClO4�ֽ⣬������װ�����ʵ�飬��֤��ֽ���ﲢ����ֽ��ʡ�(ע:��װ���п����ѳ���;��װ�ÿ��ظ�ʹ��;��B~Fװ���е��Լ���������������Ӧ���ʷ�Ӧ��ȫ��)
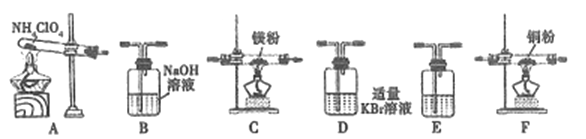
����Eװ����������������֤���ɵ��������֮һ����E��ʢ�ŵ��Լ���:_______��
���밴�����������ҵķ�������װ��:A ��E��D ��B��______��_____��_______��E (ѡ��B~Fװ�ã�����B~F��ĸ���)��
��֤����������Cl2��ʵ������:________��
�ܷ�Ӧ��������Cװ������������2.38g����NH4ClO4�ķֽ�����:________%��
��3����Ʒ��NH4ClO4�ĺ���(�����в���NH4+)���������ⶨ(��ͼ��ʾ�����Ⱥͼг�װ������ȥ)��ʵ�鲽������:

����1:��װ���������������;ȷ��ȡ��Ʒa g(������0.5g)��������ƿ�У�����Լ150mLˮ�ܽ⡣
����2:ȷ��ȡ40.00mL Լ0.1mol/L H2SO4����ƿ�С�
����3:��������ƿ�м���20mL 3mol/L NaOH��Һ;��������ʹNH3ȫ���ӷ���
����4:������й���ˮ��ϴ����װ��2~3�Σ�ϴ��Һ������ƿ�С�
����5:����ƿ�м�2~3�μ��ȣ���c mol/L NaOH����Һ�ζ����յ㣬����NaOH����ҺV1 mL��
����6:�ظ�ʵ��2~3�Ρ�
�ش���������:
�ٲ���2�У�ȷ��ȡ40.00ml H2SO4 ��Һ�IJ���������: __________��
��Ϊ�����Ʒ��NH4ClO4�ĺ��������貹���ʵ����:______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���ݻ�Ϊ3L���ܱ������ڽ������·�Ӧ��A2������+3B2������===aX����������Ӧ��ʼʱ��n(A2)=1.5mol��n(B2)= 4.0mol��2min��n(B2)=0.4mol�� n(X)=2.4mol�����㣺
��1��aֵ______________
��2��X�ı�ʾʽ����A��B��ʾ��________________
��3����(B2)Ϊ_____________
��4��2minĩ��A2��Ũ��_______________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A. ��ͭ��̼�ظֺ�ʯӢ���ǺϽ�
B. �մɡ�������ˮ������ǽ�������
C. �Ҵ�����ȩ��Ϊͬ���칹�壬���ܷ���������Ӧ
D. ��֬�����͵�����ˮ�ⶼ���ɸ߷�������С���ӵĹ���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com