
【题目】化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力,提升科学素养。I.在具支试管中加入碎瓷片和无水硫酸铝,用注射器吸取一定量石蜡油,重新连接好装置;点燃酒精灯,加热具支试管中的碎瓷片和无水硫酸铝的混合物约两分钟;将注射器中的石蜡油缓慢、逐次推入具支试管中,石蜡油与灼热的碎瓷片和无水硫酸铝接触,将所得气体依次通入酸性高锰酸钾溶液和溴水中,发现酸性高锰酸钾溶液和溴水均褪色.,将导气管迅速替换成燃烧尖嘴,点燃气体,火焰明亮,有黑烟。

(1)碎瓷片和无水硫酸铝的作用是___________。
(2)通过本实验说明____________________。
II.实验室可用氯气与金属铁反应制备无水三氯化铁,三氯化铁呈棕红色、易潮解,100![]() 左右时升华。某化学兴趣小组利用下列实验装置制备并收集无水三氯化铁。
左右时升华。某化学兴趣小组利用下列实验装置制备并收集无水三氯化铁。

(3)A装置中发生反应的离子方程式为 ;
(4)实验时,先点燃A处的酒精灯,当D管处颜色变黄绿色时,再点燃D处的酒精灯,这样操作是为了 。
(5)B装置中应盛放的试剂名称为 ;
(6)F装置所起的作用是阻止空气中的水进入反应器,防止无水三氯化铁潮解和
【答案】I.(1)催化作用; (2)所得气体含乙烯;II.(3) MnO2 + 4H+ + 2Cl-![]() Mn2+ +Cl2↑+ 2H2O;(4)排除装置中的空气;(5)饱和食盐水;(6)吸收氯气,防止污染空气。
Mn2+ +Cl2↑+ 2H2O;(4)排除装置中的空气;(5)饱和食盐水;(6)吸收氯气,防止污染空气。
【解析】
试题分析:I.(1)碎瓷片和无水硫酸铝的作用是作催化剂,催化石蜡油转变成乙烯;(2)根据实验现象,酸性高锰酸钾溶液和溴水均褪色,说明有乙烯气体存在,即石蜡油中得到的气体中含有乙烯;II.(3)反应装置A制备氯气,其离子反应方程式为MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O;(4)装置中有空气,空气中的氧气在加热条件下和铁粉发生反应,所以先通一段时间的氯气,其目的是排除装置的空气;(5)制备的氯气中含有HCl,可能干扰实验,用饱和食盐水吸收氯气中的HCl,因此B装置盛放的是饱和食盐水;(6)根据信息FeCl3易潮解,因此要防止空气中水蒸气的进入,同时氯气有毒,防止氯气污染空气。
Mn2++Cl2↑+2H2O;(4)装置中有空气,空气中的氧气在加热条件下和铁粉发生反应,所以先通一段时间的氯气,其目的是排除装置的空气;(5)制备的氯气中含有HCl,可能干扰实验,用饱和食盐水吸收氯气中的HCl,因此B装置盛放的是饱和食盐水;(6)根据信息FeCl3易潮解,因此要防止空气中水蒸气的进入,同时氯气有毒,防止氯气污染空气。


科目:高中化学 来源: 题型:
【题目】某化学学习小组设计如图实验装置(夹持装置略去)制备氯气并探究氯气的相关性质。D装置为分液漏斗形状,低进高出。
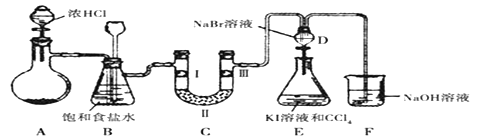
(1)若A装置中固体药品为MnO2,写出其离子反应方程式_________;若A装置中固体药品为KC1O3,则反应中每生成1 mol Cl2时转移电子数目为_______________。
(2)装置B的作用是______和________,若C处发生了堵塞,则B中的现象__________。
(3)装置C的作用是验证氯气是否具有漂白性,I处是湿润的有色布条,则II、III处应加入的物质分别是__________和__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用甲烷和氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组通过在实验室中模拟上述过程,其设计的模拟装置如下图所示:
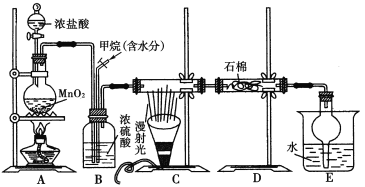
根据要求填空:
(1)B装置有三种功能:①控制气流速度;②干燥混合气体;③________________。
(2)设V(Cl2)/V(CH4)=x,若理论上欲获得最多的氯化氢,则x值应____________。
(3)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出置换出黑色小颗粒的化学方程式:____________________________________。
(4)E装置除生成盐酸外,还含有有机物,从E中分离出盐酸的最佳方法为___________。该装置的主要缺陷是 。
(5)已知丁烷与氯气的取代反应的产物之一为C4H8Cl2,其有 种同分异构体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,向A中充入1mol X和1mol Y,向B中充入2mol X和2mol Y,起始时,V(A)=V(B)=a L.在相同温度和有催化剂存在的条件下,两容器中各自发生下述反应:X(g)+Y(g)2Z(g)+W(g)△H<0
达到平衡时,V(A)=1.2aL.试回答:
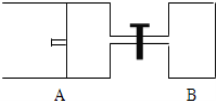
(1)A中X的转化率α(X)= 。
(2)A、B中X转化率的关系:α(A) α(B)(填“>”“=”或“<”)。
(3)平衡时的压强:P(B) 2P(A)(填“>”“=”或“<”)。
(4)打开K,一段时间又达平衡时,A的体积为 L(连通管中气体体积不计)。
(5)在(3)达平衡后,同时等幅升高A、B的温度,达新平衡后A的体积 (填“变大”“不变”或“变小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】低碳经济是以低能耗、低污染、低排放为基础的经济模式,低碳循环正成为科学家研究 的主要课题。最近有科学家提出构想:把空气吹 入饱和碳酸钾溶液,然后再把CO2从溶液中提取 出来,经化学反应后使之变为可再生燃料甲醇。 该构想技术流程如下:
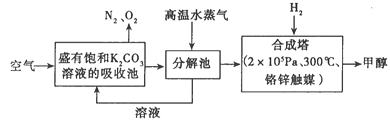
(1)向分解池中通入高温水蒸气的作用是________________。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) △H=-1275.6 kJ·mol-1
②2CO(g)+O2(g)=2CO2(g) △H=-566.0 kJ·mol-1
③H2O(g)=H2O(l) △H=-44.0 kJ·mol-1
则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为______________。
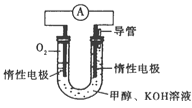
(3)依据甲醇燃烧的反应原理。设计如右图所示的电池装置。该装置负极的电极反应式为____________。
(4)已知Ksp(CaCO3)=2.8×10-9mol2·L-2.现将CaCl2溶液与0.02 mol·L-1Na2CO3溶液等体积混合,生成CaCO3沉淀时,所需CaCl2溶液的最小物质的量浓度为_____________。
(5)CO(g)和H2O(g)在一定条件下反应可得到清洁燃料H2。将不同量的CO(g)和H2O(g)分别通入到体积为2 L的恒容密闭容器中发生反应:CO(g)+H2O(g)=CO2(g)+H2(g),不同温度下得到三组数据:
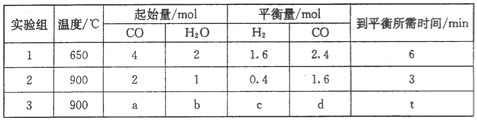
①实验1前6 min的反应速率v(CO2)=___________(保留小数点后两位,下同)。
②实验2条件下平衡常数K=_____________。
③该反应的△H____________0 (填“<”或“>”=。)
④实验3中,若平衡时的转化率α(CO)>α(H2O),则a/b的取值范围是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国古代有“银针验毒”的记载。“银针验毒”的反应原理之一是4Ag+2H2S+O2=2X+2H2O。下列有关该反应的说法正确的是( )
A. Ag得到电子 B. X为AgS
C. O2被还原 D. 每生成1 mo1X转移电子数4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.饮水安全在人们生活中占有极为重要的地位,某研究小组提取三处被污染的水源进行了分析,给出了如下实验信息:其中一处被污染的水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质。A、B、C、D、E五种常见化合物都是由下表中的离子形成:
阳离子 | K+ Na+ Cu2+ Al3+ |
阴离子 | SO42- HCO3- NO3- OH- |
为了鉴别上述化合物,分别进行以下实验,其结果如下所示:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃片);④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)将含1 mol A的溶液与含1 mol E的溶液反应后蒸干,仅得到一种化合物,该化合物为____________。
(2)写出实验②发生反应的离子方程式: 。
(3)C常用作净水剂,用离子方程式表示其净水原理: 。
Ⅱ.某强酸性溶液X可能含有A13+、NH4+、Fe2+、Fe3+、CO32-、SO32-、SO42-、C1-中的若干种,取该溶液进行连续实验,实验过程及产物如下:
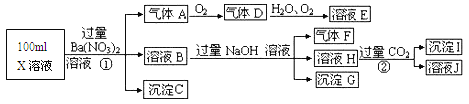
根据以上信息,回答下列问题:
(1)上述离子中,溶液X中除H+外还肯定含有的离子有_____________肯定不存在的离子是_________________
(2)请设计简单的实验检验不能确定是否含有的离子(若不止一种,可任选一种)的存在:____________________。
(3)写出反应①的离子方程式:________________。
(4)假设测定A、F、I均为0.1mol,100mL X溶液中n(H+)=0.4mol,当沉淀C的物质的量大于0.7mol时,溶液X中还一定含有____________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com