
【题目】在一支试管中放入一块很小的铜片,再加入少量浓硫酸,然后把试管固定在铁架台上。把一小条蘸有品红溶液的滤纸放入带有单孔橡皮塞的玻璃管中。塞紧试管口,在玻璃导管口处缠放一团蘸有![]() 溶液的棉花。给试管加热,观察现象。当试管中的液体逐渐透明时,停止加热。
溶液的棉花。给试管加热,观察现象。当试管中的液体逐渐透明时,停止加热。
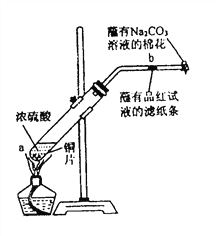
回答下列问题:
(1)写出a处反应的化学方程式____________________________________________。
(2)试管中的液体反应一段时间后,![]() 处滤纸条的变化为_____________。待试管中反应停止后,给玻璃管放有蘸过品红溶液的滤纸处微微加热,滤纸条的变化为_______。
处滤纸条的变化为_____________。待试管中反应停止后,给玻璃管放有蘸过品红溶液的滤纸处微微加热,滤纸条的变化为_______。
(3)待试管中液体冷却后,将试管上层液体倒去,再慢慢加入少量水,可观察溶液呈______色。
(4)玻璃导管口处缠放一团蘸有Na2CO3溶液的棉花所起的作用是____________
(5)如果浓硫酸的浓度为![]() ,铜片是过量的,加热使之反应,当被还原的硫酸为
,铜片是过量的,加热使之反应,当被还原的硫酸为![]() 。则浓硫酸的实际体积_____________(填写“大于”、“等于”或“小于”)
。则浓硫酸的实际体积_____________(填写“大于”、“等于”或“小于”)![]() 。
。
【答案】Cu+2H2SO4(浓)= Cu SO4 + SO2+ H2O滤纸颜色褪去滤纸颜色恢复蓝 色吸收产生的SO2防止大气污染大于
【解析】
(1)浓硫酸具有强氧化性,能和铜反应,被铜还原为二氧化硫,所以产物有生成的硫酸铜、二氧化硫和水;书写化学方程式为:Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O;
CuSO4+SO2↑+2H2O;
(2)二氧化硫能和有色物质生成无色物质,二氧化硫能使品红溶液褪色,所以二氧化硫具有漂白性;但生成的无色物质不稳定,加热时会恢复原来的颜色;
(3)铜和浓硫酸在加热条件下能发生反应,生成硫酸铜,上层是硫酸,下层是生成的硫酸铜,溶于水显蓝色;
(4)SO2是大气污染物,并能随意排放,则玻璃导管口处缠放一团蘸有Na2CO3溶液的棉花所起的作用是吸收二氧化硫,防止污染,有关的方程式是:Na2CO3+SO2=Na2SO3+CO2;
(5)由于在反应过程中,硫酸的浓度是逐渐降低的,而稀硫酸和铜不反应,如果浓硫酸的浓度为18mol/L,当被还原的硫酸为0.9mol,参加反应的硫酸的物质的量为1.8mol,此时浓硫酸的体积为1.8mol÷18mol/L=0.1L,则浓硫酸的实际体积大于100mL。


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
【题目】镍及其化合物用途广泛。某矿渣的主要成分是NiFe2O4(铁酸镍)、NiO、FeO、CaO、SiO2等,以下是从该矿渣中回收NiSO4的工艺路线:
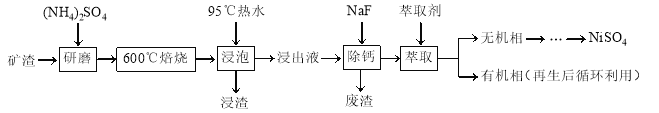
已知:(NH4)2SO4在350℃以上会分解生成NH3和H2SO4。NiFe2O4在焙烧过程中生成NiSO4、Fe2(SO4)3。锡(Sn)位于第五周期第ⅣA族。
(1)焙烧前将矿渣与(NH4)2SO4混合研磨,混合研磨的目的是______________。
(2)“浸泡”过程中Fe2(SO4)3生成FeO(OH)的离子方程式为______________,“浸渣”的成分除Fe2O3、FeO(OH)外还含有______________(填化学式)。
(3)为保证产品纯度,要检测“浸出液”的总铁量:取一定体积的浸出液,用盐酸酸化后,加入SnCl2将Fe3+还原为Fe2+,所需SnCl2的物质的量不少于Fe3+物质的量的________倍;除去过量的SnCl2后,再用酸性K2Cr2O7标准溶液滴定溶液中的Fe2+,还原产物为Cr3+,滴定时反应的离子方程式为______________。
(4)“浸出液”中c(Ca2+) = 1.0×10-3mol·L-1,当除钙率达到99%时,溶液中c(F-) = ________ mol·L-1。[已知Ksp (CaF2)=4.0×10-11]
(5)本工艺中,萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+的萃取率影响如图所示,V0/VA的最佳取值是________。
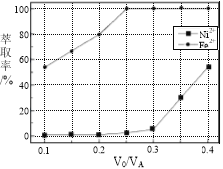
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】当配制一定物质的量浓度的溶液时,错误的操作会导致溶液的浓度发生改变. 不小心将溶液溅到烧杯外(填偏大、偏小或无影响)定容时俯视摇匀后,发现溶液低于刻度线,加水至刻度线 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】宇宙飞船以N2H4(联氨)和N2O4为推力源,反应温度达2700℃,反应式为2N2H4+N2O4=3N2+4H2O。关于该反应的说法中正确的是
A. 属于置换反应 B. 联氨是氧化剂
C. 联氨是还原剂 D. 氮气是氧化产物,不是还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.1 mol O2的质量是32g/mol
B.阿伏加德罗常数的准确值就是6.02×1023
C.CO2的摩尔质量是44g/mol
D.常温常压下22.4L氦气含有1 mol原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化钙(CaH2)固体是一种储氢材料,是登山运动员常用的能源提供剂,某化学小组的同学在老师的指导下制备氢化钙.
[查阅资料]
氢化钙通常用氢气与钙加热制得.
氢化钙要密封保存,遇水反应生成氢氧化钙和氢气.
钙遇水立即发生剧烈反应生成氢氧化钙和氢气,并放出大量的热.
标准状况下氢气的密度为0.09g/L.
[进行实验]小组同学设计的制取装置如图所示(固定装置略).

回答下列问题:
(1)写出A中发生反应的化学方程式______________________________.
(2)B、D中所盛试剂相同,该试剂为_____________,其作用分别是____________________、___________________________.
(3)实验时先打开A中活塞,一段时间后,再点燃C中酒精灯,其目的是__________________.
(4)装置C中制取氢化钙的化学方程式是______________________.
[实验反思]小组同学通过反思提出问题:上述制得的氢化钙是否纯净?
他们再次设计实验进行检验,实验步骤如下:
步骤1:检查装置气密性,装入足量的水和已称好质量的氢化钙样品,按图所示连接仪器(固定装置略).

步骤2:将Y形管倾斜,使A中的水全部进入B中,完全反应后,冷却至室温,读取量筒读数.
(5)通过上述实验可分析出制得的氢化钙是否纯净,其依据是______________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能用H++OH-=H2O来表示的化学反应是
A.氢氧化镁和稀盐酸反应
B.Ba(OH)2溶液滴入稀硫酸中
C.澄清石灰水和稀硝酸反应
D.二氧化碳通入澄清石灰水中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com