
ЎҫМвДҝЎҝЙиNAОӘ°ў·ьЩӨөВВЮіЈКэөДЦөЈ®ПВБРЛө·ЁХэИ·өДКЗЈЁ Ј©
A.0.2molAlУлЧгБҝNaOHИЬТә·ҙУҰЈ¬ЙъіЙөДH2·ЦЧУКэОӘ0.3NA
B.іЈОВПВЈ¬1LpH=1өДСОЛбИЬТәЈ¬УЙЛ®өзАлөДH+АлЧУКэДҝОӘ0.1NA
C.ұкЧјЧҙҝцПВЈ¬0.1molВИ·ВөДМе»эОӘ2.24L
D.11P4+60CuSO4+96H2O=20Cu3P+24H3SO4+60H2SO4·ҙУҰЦРЈ¬6molCuSO4ДЬСх»Ҝ°ЧБЧөД·ЦЧУКэОӘ1.1NA
Ўҫҙр°ёЎҝA
ЎҫҪвОцЎҝҪвЈәAЎў1molВБ·ҙУҰЙъіЙ1.5molЗвЖшЈ¬№К0.2molВБ·ҙУҰЙъіЙ0.3molЗвЖшЈ¬јҙ0.3NAёцЗвЖш·ЦЧУЈ¬№КAХэИ·Ј»BЎўіЈОВПВЈ¬1LpH=1өДСОЛбИЬТәЦРә¬УРЗвАлЧУөДОпЦКөДБҝЕЁ¶ИОӘЈә0.1mol/LЈ¬СОЛбТЦЦЖБЛЛ®өДөзАлЈ¬ФтИЬТәЦРөДЗвСхёщАлЧУКЗЛ®өзАлөДЈ¬Л®өзАлөДЗвАлЧУЕЁ¶ИОӘЈә1ЎБ10©Ғ13mol/LЈ¬1LёГИЬТәЦРУЙЛ®өзАлөДЗвАлЧУөДОпЦКөДБҝОӘЈә1ЎБ10©Ғ13molЈ¬№КBҙнОуЈ»
CЎўұкҝцПВЈ¬ВИ·ВОӘТәМ¬Ј¬І»ДЬёщҫЭЖшМеДҰ¶ыМе»эАҙјЖЛгЈ¬№КCҙнОуЈ»
DЎўCuФӘЛШөД»ҜәПјЫУЙ+2јЫҪөөНөҪ+1јЫЈ¬CuSO4КЗСх»ҜјБЈ¬P4Іҝ·ЦБЧФӘЛШУЙ0јЫҪөөНөҪ©Ғ3јЫЈ¬Іҝ·ЦБЧФӘЛШУЙ0јЫЙэёЯөҪ+5јЫЈ¬БЧФӘЛШөД»ҜәПјЫјИЙэёЯУЦҪөөНЈ¬ЛщТФP4јИКЗСх»ҜјБУЦКЗ»№ФӯјБЈ¬ИфУР11molP4ІОјУ·ҙУҰЈ¬ЖдЦР5molөДP4ЧцСх»ҜјБЈ¬60molБтЛбНӯЧцСх»ҜјБЈ¬Ц»УР6molөДP4Чц»№ФӯјБЈ¬
ФтУЙөзЧУКШәгҝЙЦӘЈ¬УР6 molөДCuSO4ІОјУ·ҙУҰЈ¬Фтұ»БтЛбНӯСх»ҜөД°ЧБЧ·ЦЧУөДОпЦКөДБҝОӘ ![]() =
= ![]() molЈ¬№КDҙнОуЈ®
molЈ¬№КDҙнОуЈ®
№КСЎAЈ®



| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝИзНјКЗТ»ЦЦЧЫәПҙҰАнSO2·ПЖшөД№ӨТХБчіМЎЈПВБРЛө·ЁХэИ·өДКЗ(ЎЎЎЎ)

A. ПтИЬТәBЦРөОјУKSCNИЬТәЈ¬ИЬТәТ»¶ЁІ»»бұдәмЙ«
B. ИЬТәAЧӘ»ҜОӘИЬТәB·ўЙъ·ҙУҰөДАлЧУ·ҪіМКҪОӘЈә2Fe3Ј«Ј«2H2OЈ«SO2===2Fe2Ј«Ј«SO![]() Ј«4HЈ«
Ј«4HЈ«
C. ИЬТәЛбРФЈәB>C>A
D. јУСх»ҜСЗМъҝЙТФК№ИЬТәCЧӘ»ҜОӘИЬТәA
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРЛө·ЁХэИ·өДКЗЈЁ Ј©
A. ¶Ўҙп¶ыР§УҰІ»КЗҪәМеМШУРөДПЦПуЈ¬ИЬТәУлЧЗТәТІУР
B. ҪәМеУлЖдЛы·ЦЙўПөөДұҫЦКЗшұрКЗУР¶Ўҙп¶ыР§УҰЈ¬¶шЖдЛы·ЦЙўПөГ»УР
C. ҪәМеБЈЧУөДЦұҫ¶РЎУЪ10Јӯ9m
D. ¶Ўҙп¶ыР§УҰҝЙУГУЪјшұрҪәМеәНИЬТә
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРОпЦКЦРЈ¬ДЬ·ўЙъИЎҙъ·ҙУҰөДКЗЈЁ Ј©
A.ТТП©
B.јЧНй
C.ТТИІ
D.ТТИ©
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝДіС§ЙъУГ0.1000 molL©Ғ1KOHТәөО¶ЁОҙЦӘЕЁ¶ИөДҙЧЛбЈ¬ЖдІЩЧч·ЦҪвОӘИзПВјёІҪЈә AЈ®ТЖИЎ20mLҙэІвҙЧЛбЧўИлҪаҫ»өДЧ¶РОЖҝЈ¬ІўјУИл2Ў«3өОЦёКҫјБ
BЈ®УГұкЧјИЬТәИуПҙөО¶Ё№Ь2Ў«3ҙО
CЈ®°СКўУРұкЧјИЬТәөДјоКҪөО¶Ё№Ь№М¶ЁәГЈ¬өчҪЪөО¶Ё№ЬјвЧмК№Ц®ідВъИЬТә
DЈ®ИЎұкЧјKOHИлјоКҪөО¶Ё№ЬЦБЎ°0ЎұҝМ¶ИТФЙП1Ў«2cm
EЈ®өчҪЪТәГжЦБЎ°0Ўұ»тЎ°0ЎұТФПВДіТ»ҝМ¶ИЈ¬јЗПВ¶БКэ
FЈ®°СЧ¶РОЖҝ·ЕФЪөО¶Ё№ЬөДПВГжЈ¬УГұкЧјKOHИЬТәөО¶ЁЦБЦХөгІўјЗПВөО¶Ё№ЬТәГжөДҝМ¶ИЈ®
ҫНҙЛКөСйНкіЙМоҝХЈә
ЈЁ1Ј©ХэИ·ІЩЧчІҪЦиөДЛіРтКЗЈЁУГРтәЕЧЦДёМоРҙЈ©Ј»
ЈЁ2Ј©ЙПКцBІҪЦиІЩЧчөДДҝөДКЗЈ»
ЈЁ3Ј©ЙПКцAІҪЦиІЩЧчЦ®З°Ј¬ПИУГҙэІвТәИуПҙЧ¶РОЖҝЈ¬Фт¶ФЧоЦХөО¶ЁҪб№ыөДУ°ПмКЗ Ј® ЈЁМоЎ°ФцҙуЎұЎўЎ°јхРЎЎұЎў»тЎ°І»ұдЎұЈ©
ЈЁ4Ј©AІҪЦиЦРЈ¬К№УГөДЦёКҫјБОӘ Ј¬ ЕР¶ПөҪҙпөО¶ЁЦХөгөДКөСйПЦПуКЗЈәЈ»
ЈЁ5Ј©ИзНј1ОӘДіТ»ҙОјоКҪөО¶Ё№ЬөО¶ЁЗ°ТәГжЈ¬Жд¶БКэЦөОӘmLЈ¬Нј2ОӘөО¶ЁҪбКшТәГжЈ¬ФтұҫҙОөО¶Ё№эіМ№ІК№УГБЛmLKOHұкЧјИЬТә 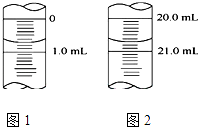
ЈЁ6Ј©ОӘұк¶ЁДіҙЧЛбИЬТәөДЧјИ·ЕЁ¶ИЈ¬УГ0.1000molL©Ғ1өДNaOHИЬТә¶Ф20.00mLҙЧЛбИЬТәҪшРРөО¶ЁЈ¬јёҙОөО¶ЁПыәДNaOHИЬТәөДМе»эИзПВЈә
КөСйРтәЕ | 1 | 2 | 3 | 4 |
ПыәДNaOHИЬТәөДМе»эЈЁmLЈ© | 20.05 | 20.00 | 18.80 | 19.95 |
ФтёГҙЧЛбИЬТәөДЧјИ·ЕЁ¶ИОӘ Ј® ЈЁұЈБфРЎКэөгәуЛДО»Ј©
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВұн¶ФДіР©·ҙУҰ·ҪіМКҪөДЖАјЫәПАнөДКЗЈЁ Ј©
ұаәЕ | АлЧУ·ҪіМКҪ»төзј«·ҙУҰКҪ | ЖАјЫ | |
A | ҙОВИЛбёЖИЬТәЦРНЁИлЧгБҝSO2 | Ca2++ClO©Ғ+SO2+H2O=CaSO4+Cl©Ғ+2H+ | ХэИ· |
B | БтЛбМъИЬТәУлЗвСх»ҜұөИЬТә»мәП | Fe3++SO | ХэИ· |
C | ҙЧЛбп§ИЬУЪЛ® | CH3COO©Ғ+NH | ҙнОуЈ¬ТхАлЧУЛ®ҪвПа»ҘҙЩҪшЈ¬УҰёГУГЎ°=ЎұәЕ |
D | УГ¶иРФөзј«өзҪвВИ»ҜНӯәНВИ»ҜДЖөД»мәПИЬТәТ»¶ОКұјд | Тхј«Јә2Cu2++4e©Ғ=2Cu | ҙнОуЈ¬ёГТхСфБҪј«·ҙУҰІ»ҝЙДЬН¬Кұ·ўЙъ |
A.A
B.B
C.C
D.D
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝScience ФУЦҫФЪ2017ДкҙәҪЪ·ўұнБЛДПҫ©Ан№ӨҙуС§өДВЫОДЈ¬ұЁөАБЛКАҪзЙПКЧёціЙ№ҰәПіЙөДОеөӘТхАлЧУСО (N5)6(H3O)3(NH4)4ClЈЁ°ЧЙ«№ММеЈ©Ј¬ХвКЗИ«өӘә¬ДЬІДБПЦРАпіМұ®КҪөДН»ЖЖЎЈёГСОҝЙјтВФұнКҫИзПВЈ¬ПВБР·ЦОцІ»әПАнөДКЗЈЁ Ј©
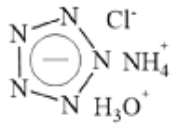
A. ОеөӘТхАлЧУөД»ҜС§КҪОӘ ![]() B. ёГСОЦРөӘФӘЛШөД»ҜәПјЫҫщОӘ-3јЫ
B. ёГСОЦРөӘФӘЛШөД»ҜәПјЫҫщОӘ-3јЫ
C. ёГСОУцЗҝјоДЬКН·ЕіцNH3 D. ёГСОЦРОеөӘТхАлЧУҫЯУР»№ФӯРФ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝОТ№ъГчҙъЎ¶ұҫІЭёЩДҝЎ·ЦРКХФШТ©Оп1892ЦЦЈ¬ЖдЦРЎ°ЙХҫЖЎұМхДҝПВРҙөАЈәЎ°ЧФФӘКұКјҙҙЖд·ЁЈ¬УГЕЁҫЖәНФгИлкөЈ¬ХфБоЖшЙПЎӯЎӯЖдЗеИзЛ®Ј¬О¶ј«ЕЁБТЈ¬ёЗҫЖВ¶ТІЎЈЎұХвАпЛщУГөДЎ°·ЁЎұКЗЦёЈЁ Ј©
A. ЭНИЎ B. ЙшОц C. ХфБу D. ·ЦТә
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝўЩЎ«ўв10ЦЦФӘЛШФЪФӘЛШЦЬЖЪұнЦРөДО»ЦГИзНјЈ¬Зл»ШҙрПВБРОКМвЈЁУГҫЯМеФӘЛШ·ыәЕ»т»ҜС§КҪөИ»ҜС§УГУпМоҝХЈ©Ј®
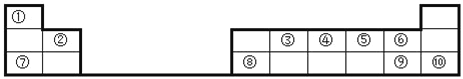
ЈЁ1Ј©10ЦЦФӘЛШЦР»ҜС§РФЦКЧоОИ¶ЁөДКЗ_____Ј¬·ЗҪрКфРФЧоЗҝөДКЗ______Ј®
ЈЁ2Ј©ЙПКцФӘЛШөДЧоёЯјЫСх»ҜОп¶ФУҰЛ®»ҜОпЦРЛбРФЧоЗҝөДКЗ___________ЈЁМо»ҜС§КҪЈ©Ј®
ЈЁ3Ј©ўЭўЮўЯўа¶ФУҰөДјтөҘАлЧУЦР°лҫ¶ЧоРЎөДКЗ________ЈЁУГАлЧУ·ыәЕұнКҫЈ©Ј®
ЈЁ4Ј©ФӘЛШўЬөДФӯЧУҪб№№КҫТвНјКЗ____________Ј¬№ӨТөЙПТФўЬөДЗв»ҜОпОӘФӯБПәПіЙўЬөДЧоёЯјЫСх»ҜОп¶ФУҰЛ®»ҜОпөД»ҜС§·ҪіМКҪОӘ___________________________ЎЈ
ЈЁ5Ј©ФӘЛШўЯЧоёЯјЫСх»ҜОп¶ФУҰЛ®»ҜОпУлФӘЛШўаөДЧоёЯјЫСх»ҜОп¶ФУҰЛ®»ҜОп·ҙУҰөДАлЧУ·ҪіМКҪЈә______________________
Ійҝҙҙр°ёәНҪвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com