
对于化学反应方向的确定,下列说法正确的
A.反应的焓变是决定反应能否自发进行的唯一因素
B.温度、压强一定时,放热反应能自发进行
C.在温度、压强一定的条件下,焓因素和熵因素共同决定一个化学反应的方向
D.固体的溶解过程与焓变无关
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.水是人体的重要组成成分, 是人体中含量最多的一种物质
B.淀粉在体内必须转换为葡萄糖才能被机体利用, 而这种转换不需水参加
C.水约占人体体重的三分之一, 由于水分不断代谢, 故人体内的水分需不断补充
D.喝纯净水比喝矿泉水更有利于人体健康
查看答案和解析>>
科目:高中化学 来源: 题型:
随着社会的发展,人们日益重视环境问题,下列做法或说法不正确的是( )
A.对垃圾进行无害化、资源化处理
B.将煤气化或液化,获得清洁燃料
C.PM2.5是指大气中直径接近于2.5×10﹣6m的颗粒物,也称细颗粒物,这些细颗粒物分散在空气中形成的分散系是胶体
D.推广使用无磷洗衣粉和无氟冰箱
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室里需要纯净的氯化钠溶液,但手边只有混有硫酸钠、碳酸氢铵的氯化钠.某学生设计了如图所示方案:(注:碳酸氢铵受热可完全分解成气态物质)
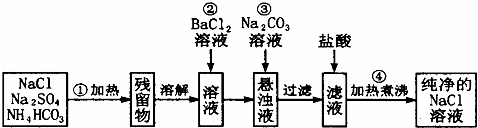
如果此方案正确,那么:
(1)操作①可选择的仪器是 坩埚 .
(2)操作②是否可改为加硝酸钡溶液?为什么? 不能 ;理由 改用Ba(NO3)2会使溶液中引入新的杂质离子NO3﹣,以后操作中无法除去 .
(3)进行操作②后,如何判断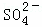 已除尽,方法是 取少量上层澄清溶液,再滴加BaCl2溶液,如无沉淀出现则说明SO42﹣已除尽 .
已除尽,方法是 取少量上层澄清溶液,再滴加BaCl2溶液,如无沉淀出现则说明SO42﹣已除尽 .
(4)操作③的目的是 除去过量的Ba2+ .
(5)操作④的目的是 除去滤液中溶解的CO2和多余的盐酸 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.金属腐蚀就是金属失去电子被还原的过程
B.将水库中的水闸(钢板)与外加直流电源的负极相连,正极连接到一块废铁上可防止水闸被腐蚀
C.合金的熔点都高于它的成分金属,合金的耐腐蚀性也都比其成分金属强
D.铜板上的铁铆钉处在潮湿的空气中直接发生反应:Fe-3e- = Fe3+,继而形成铁锈
查看答案和解析>>
科目:高中化学 来源: 题型:
t℃时,水的离子积为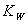 ,该温度下将a mol•L-1一元酸HA与b mol•L-1一元碱BOH等体积混合,要使混合液呈中性,必要的条件是
,该温度下将a mol•L-1一元酸HA与b mol•L-1一元碱BOH等体积混合,要使混合液呈中性,必要的条件是
A.混合液的pH=7 B.混合液中c(H+)=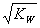
C.a=b D.混合液中c(B+)=c(A-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知0.1 mol·L-1的二元酸H2A溶液的pH=4,则下列说法中正确的是
A.在Na2A、NaHA两溶液中,离子种类不相同
B.在溶质物质的量相等的Na2A、NaHA两溶液中,阴离子总数相等
C.在NaHA溶液中一定有c(Na+)+c(H+)=c(HA-)+c(OH-)+2c(A2-)
D.在Na2A溶液中一定有c(Na+)>c(A2-)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
与100mL 0.5mol·L—1NaCl溶液中的Cl-的物质的量浓度相同的是
A.100mL 0.5 mol·L—1MgCl2溶液 B.100 mL 0.5mol·L—1KClO3溶液
mL 0.5mol·L—1KClO3溶液
C.200mL 0.25 mo l·L—1 KCl溶液 D.100mL 0.5mol·L—1 HCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液仅含Fe2+、Na+、Al3+、Ba2+、SO42-、NO3-、Cl-中的4种离子,所含离子的物质的量均为1mol。若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解)。下列说法不正确的是
A.若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液显血红色
B.若向该溶液中加入过量的稀硫酸,产生的气体遇空气能变成红棕色
C.该溶液中所含的离子是:Fe2+、Na+、SO42-、NO3-
D.若向该溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为72g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com