
【题目】下列有关热化学方程式的叙述正确的是( )
A.已知2H2(g)+O2(g)=2H2O(g);△H=﹣483.6kJ/mol,则氢气的燃烧热为241.8kJ
B.已知4P(红磷,s)=P4(白磷,s);△H>0,则白磷比红磷稳定
C.含20.0g NaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(aq)+ ![]() H2SO4(aq)=
H2SO4(aq)= ![]() Na2SO4(aq)+H2O(l);△H=﹣57.4kJ/mol
Na2SO4(aq)+H2O(l);△H=﹣57.4kJ/mol
D.己知C(s)+O2 (g)=CO2(g);△H1? 2C(s)+O2(g)=2CO(g);△H2????? 则△H1>△H2
【答案】C
【解析】解:A.已知2H2(g)+O2(g)=2H2O(g);△H=﹣483.6kJ/mol,热化学方程式中水是气体不是稳定氧化物,则氢气的燃烧热大于241.8kJ/mol,故A错误;B.已知4P(红磷,s)=P4(白磷,s);△H>0,则白磷比红磷能量高,所以红磷稳定,故B错误;
C.含20.0g NaOH的稀溶液与稀硫酸完全中和,放出28.7kJ的热量,则表示该反应中和热的热化学方程式为:NaOH(aq)+ ![]() H2SO4(aq)=
H2SO4(aq)= ![]() Na2SO4(aq)+H2O(l);△H=﹣57.4kJ/mol,故C正确;
Na2SO4(aq)+H2O(l);△H=﹣57.4kJ/mol,故C正确;
D.已知①C(s)+O2 (g)=CO2(g);△H1
②2C(s)+O2(g)=2CO(g);△H2
根据盖斯定律②﹣①得到C(s)+CO2(g)=2CO(g);△H2﹣△H1 , 因为C(s)+CO2(g)=2CO(g)为吸热反应△H>0,则△H1<△H2 , 故D错误;
故选C.


科目:高中化学 来源: 题型:
【题目】如图示个各物质间的转化关系中,X、Y、Z包含相同的元素 
(1)气体Z是色,具有气味的气体.
(2)固体X溶于水(填“能”或“不”)
(3)请写出Z与O2生成Y的化学方程式 .
(4)请写出X与浓硫酸反应生成Y的化学方程式 .
(5)请写出Z与Y反应生成X的化学方程式 .
(6)将Y通入到溴水当中发现溴水褪色,请写出其离子方程式 , 这体现了Y具有性.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】TiO2在工业生产和日常生活中有重要用途.
(1)工业上用钛铁矿石(FeTiO3 , 含FeO、Al2O3、SiO2等杂质)经过下述反应制得: 
其中,步骤③发生的反应为:2H2SO4+FeTiO3=TiOSO4+FeSO4+2H2O.
(i)净化钛矿石时,需用浓氢氧化钠溶液来处理,写出该过程中两性氧化物发生反应的离子反应方程式: .
(ii)④中加入的X可能是
A.H2O2 B.KMnO4 C.KOH D.SO2
(iii)④⑤两步的目的是 .
(iv)写出⑥的化学反应方程式 .
(2)TiO2可通过下述两种方法制备金属钛:方法一是先将TiO2与Cl2、C反应得到TiCl4 , 再用镁还原得到Ti.
(i)写出生成TiCl4的化学反应方程式
方法二是电解TiO2来获得Ti(同时产生O2):
将处理过的TiO2作阴极,石墨为阳极,熔融CaO为电解液,用碳块作电解槽池.
(ii)阴极反应的电极反应式为 .
(iii)电解过程中需定期向电解槽池中加入碳块的原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:A是石油裂解气的主要成分,现以A为主要原料合成乙酸乙酯,其合成路线如图所示.请回答下列问题: 
(1)B物质中官能团的名称;
(2)写出反应②的化学方程式(及反应类型): .
(3)写出C与银氨溶液反应的化学方程式: .
(4)写出乙酸乙酯在碱性条件下水解的化学方程式(及反应类型): .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示在某溶液中滴加Ba(OH)2溶液时,沉淀的物质的量随Ba(OH)2的物质的量的变化关系.该溶液的成分可能是( ) 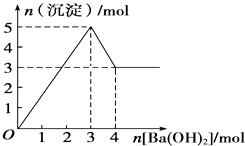
A.MgSO4
B.KAl(SO4)2
C.Al2(SO4)3
D.NaAlO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】写出有关反应的化学方程式:
(1)钠投入水中 .
(2)过氧化钠作为潜水艇和呼吸面具中氧气的来源; .
(3)实验室制取氯气时,多余的尾气用碱液来吸收: .
(4)漂白粉露置在空气中为什么会失效? .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为检验碳和浓硫酸反应生成的产物,设计如图装置,请回答: 
(1)指出仪器名称:甲; 乙;
(2)乙仪器中发生反应的化学方程式为;
(3)证明有二氧化碳产生的实验现象是;
(4)若把B玻璃管移到F试管后连接,是否可行(填“可行”或“不可行”),理由是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cl2、ClO2等气体可作为水处理等方面有广泛应用的高效安全消毒剂.我国从2 000年起逐步用ClO2代替氯气对饮用水进行消毒.
(1)工业制漂白粉的化学方程式为 .
(2)消毒水时,ClO2还可将水中的Fe2+、Mn2+等转化成Fe(OH)3和MnO2等难溶物除去,说明ClO2具有性.
(3)工业上在80℃时电解氯化钠溶液得到 NaClO3 , 然后与盐酸反应得到ClO2 . 电解时生成ClO3﹣的电极反应式为 .
(4)自来水厂用ClO2处理后的水中,要求ClO2的浓度在0.1~0.8mg/L之间.碘量法可以检测水中ClO2的浓度,步骤如下:
Ⅰ.取一定体积的水样,加入一定量的碘化钾,再用氢氧化钠溶液调至中性,并加入淀粉溶液,溶液变蓝.
Ⅱ.加入一定量的Na2S2O3溶液.(已知:2S2O32﹣+I2═S4O62﹣+2I﹣)
Ⅲ.加硫酸调节水样pH至1~3.
操作时,不同pH环境中粒子种类如图所示: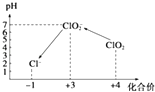
请回答:
①操作Ⅰ中反应的离子方程式是 .
②确定操作Ⅱ完全反应的现象是 .
③在操作Ⅲ过程中,溶液又呈蓝色,反应的离子方程式是 .
④若水样的体积为1.0L,在操作Ⅱ时消耗了1.0×10﹣3 mol/L的Na2S2O3溶液10mL,则水样中ClO2的浓度是mg/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】描述下列反应的现象并写出反应的离子方程式。
(1)向FeCl3溶液中滴加NaOH溶液,现象: , 离子方程式:
(2)向NaHCO3溶液中滴加稀H2SO4 , 现象: , 离子方程式:
(3)稀HNO3和Ba(OH)2溶液混合,现象: , 离子方程式:
(4)比较:上述三个离子反应发生的条件的不同点是;相同点是
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com