
【题目】A、B、C、D、E、F、G元素原子序数依次增大.已知B原子最外层有3个未成对电子,C原子最外层电子数与核外电子总数之比为3:4,E与C同主族,F﹣、D+、A+离子的半径逐渐减小,化合物AF常温下为气体,G的基态原子核外M能层填满电子,N能层只有1个电子.据此回答下列问题:
(1)写出D元素基态原子的核外电子排布式;B、C、E三种元素的第一电离能由大到小的顺序是 (用元素符号表示) .
(2)A与C可形成18电子分子,其水溶液中滴入少量氯化铁溶液时有大量气泡逸出,写出该反应的化学方程式 .
(3)某化合物由上述七种元素中的三种元素组成,为常见家用消毒剂的主要成分,其中化学键类型为;该化合物水溶液不呈中性的原因是(用离子方程式表示) .
(4)0.3mol G的低价氧化物能与mol B的最高价氧化物对应水化物的溶液恰好完全反应(设还原产物只有BO).
(5)卫星发射时可用B2A4为燃料,1 mol气态B2A4在适量C2中燃烧,生成B2和气态A2C,放出534 kJ的热量,1 mol液态A2C完全气化需吸收44 kJ热量.请写出气态B2A4在C2中燃烧生成B2和液态A2C时的热化学方程式 .
【答案】
(1)1s22s22p63s1;N>O>S
(2)2H2O2 ![]() 2H2O+O2↑
2H2O+O2↑
(3)离子键、共价键;ClO﹣+H2O?HClO+OH﹣
(4)1.4
(5)N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=﹣622kJ/mol
【解析】解:A、B、C、D、E、F、G元素原子序数依次增大.C原子最外层电子数与核外电子总数之比为3:4,最外层电子数不能超过8,原子只能有2个电子层,最外层电子数为6,故C为O元素;E与C同主族,则E为S元素;B原子最外层有3个未成对电子,原子核外电子排布为1s22s22p3 , 故B为N元素;F﹣、D+、A+离子的半径逐渐减小,化合物AF常温下为气体,则A为H元素、D为Na、F为Cl,G的基态原子核外M能层填满电子,N能层只有1个电子,则G为Cu元素.(1)D是Na元素,钠原子核外有11个电子,根据构造原理知D元素基态原子的核外电子排布式1s22s22p63s1;B是N元素,C是O元素,E是S元素,N元素2p能级为半满稳定状态,能量较低,第一电离能高于氧元素的,同主族张而行第一电离能减小,所以B、C、E三种元素的第一电离能由大到小的顺序是N>O>S,所以答案是:1s22s22p63s1;N>O>S;(2)A是H元素,C是O元素,A与C可形成18电子分子,则该物质是H2O2 , 双氧水在氯化铁作催化剂条件下分解生成水和氧气,反应方程式为:2H2O2 ![]() 2H2O+O2↑,所以答案是:2H2O2
2H2O+O2↑,所以答案是:2H2O2 ![]() 2H2O+O2↑;(3)由三种元素组成的常见家用消毒剂的主要成分是NaClO,次氯酸钠中钠离子和次氯酸根离子之间存在离子键,氧原子和氯原子之间存在共价键,次氯酸钠是强碱弱酸盐,次氯酸根离子易水解ClO﹣+H2OHClO+OH﹣ , 使其溶液呈碱性,所以答案是:离子键、共价键;ClO﹣+H2OHClO+OH﹣;(4)G的低价氧化物是Cu2O,B的最高价氧化物的水化物是HNO3 , 该反应方程式为:3Cu2O+14HNO3=6Cu(NO3)2+2NO+7H2O,根据方程式知,0.3molCu2O和1.4mol硝酸恰好完全反应,所以答案是:1.4;(5)1mol气态N2H4在适量O2中燃烧,生成N2和气态H2O,放出534kJ的热量,可得: N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=﹣534kJ/mol ①,
2H2O+O2↑;(3)由三种元素组成的常见家用消毒剂的主要成分是NaClO,次氯酸钠中钠离子和次氯酸根离子之间存在离子键,氧原子和氯原子之间存在共价键,次氯酸钠是强碱弱酸盐,次氯酸根离子易水解ClO﹣+H2OHClO+OH﹣ , 使其溶液呈碱性,所以答案是:离子键、共价键;ClO﹣+H2OHClO+OH﹣;(4)G的低价氧化物是Cu2O,B的最高价氧化物的水化物是HNO3 , 该反应方程式为:3Cu2O+14HNO3=6Cu(NO3)2+2NO+7H2O,根据方程式知,0.3molCu2O和1.4mol硝酸恰好完全反应,所以答案是:1.4;(5)1mol气态N2H4在适量O2中燃烧,生成N2和气态H2O,放出534kJ的热量,可得: N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=﹣534kJ/mol ①,
由1 mol液态H2O完全气化需吸收44 kJ热量,可得:
H2O(l)=H2O(g)△H=+44kJ/mol②,
根据盖斯定律,①﹣②×2得N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=﹣534kJ/mol﹣2(+44kJ/mol)=﹣622kJ/mol,
所以答案是:N2H4(g)+O2(g)=N2(g)+2H2O(l)△H=﹣622kJ/mol.


 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案科目:高中化学 来源: 题型:
【题目】下列是某校实验小组设计的一套原电池装置,下列有关描述不正确的是( ) 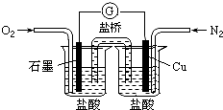
A.此装置能将化学能转变为电能
B.石墨电极的反应式:O2+2H2O+4e﹣=4OH﹣
C.电子由Cu电极经导线流向石墨电极
D.电池总的反应是:2Cu+O2+4HCl=2CuCl2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.2mol某烃A在氧气中完全燃烧后,生成CO2和H2O各1.0mol.试回答:
(1)烃A的分子式为 .
(2)若取一定量的该烃A完全燃烧后,生成CO2和H2O各3mol,则有g烃A参加了反应,燃烧时消耗标准状况下的氧气L;
(3)若烃A不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯取代物只有一种,则烃A的结构简式为;
(4)若烃A能使溴水褪色,在催化剂作用下,与H2加成,其加成产物经测定分子中含有3个甲基,烃A可能有的结构简式为;
(5)比烃A少一个碳原子A的同系物有种同分异构体.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数。下列有关NA的叙述中,正确的是( )
A. 1 mol 任何物质所含的微粒数均为NA
B. 14 g氮气所含的N原子数为NA
C. 标准状况下,22.4 L水所含的H2O分子数为NA
D. 在钠与氧气的反应中,1 mol钠失去电子的数目为2 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了检验某卤代烃(R﹣X)中的X元素,在下列实验操作中:①加热②加入硝酸银溶液③取少量卤代烃④加入稀硝酸溶液酸化⑤加入氢氧化钠溶液⑥冷却,所选择的正确的操作顺序是( )
A.③⑤④②
B.③⑤①④②
C.③⑤①⑥②
D.③⑤①⑥④②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA代表阿伏加德罗常数,下列说法正确的是( )
A. 0.2NA个CO分子在标准状况下的体积约是4.48 L
B. 0.1mol/L BaCl2溶液中Cl﹣数目是0.2 NA
C. 标准状况时,22.4 L水中含有的电子数目为10NA个
D. 将0.1mol FeCl3加到沸水中制得的胶体中,含胶粒0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,下列说法不正确的是( )
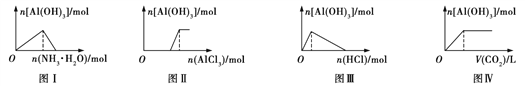
A. 图Ⅱ表示向NaOH溶液中滴加AlCl3溶液至过量且边滴边振荡
B. 图Ⅰ表示向AlCl3溶液中滴加氨水至过量
C. 图Ⅲ表示向NaAlO2溶液中滴加稀盐酸至过量且边滴边振荡
D. 图Ⅳ表示向NaAlO2溶液中缓慢通入二氧化碳至过量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业中采用适当的催化剂利用反应CO(g)+2H2(g)═CH3OH(g)来制取甲醇.
维持体系的压强一定,温度为T时,在体积为2.0L的封闭容器内充入0.6mol CO和0,.4mol H2 , 达到平衡时含有0.15mol CH3OH(g),则该反应平衡常数K=(保留两位小数),此时向容器中再通入0.7mol CO气体,则此平衡将(填“正向”、“不”或“逆向”)移动.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com