
| A. | ①④ | B. | ②③ | C. | ③④ | D. | ①⑤ |
分析 分子晶体熔化时需要克服分子间作用力,原子晶体熔化时需要克服共价键,金属晶体熔化时需要克服金属键,离子晶体熔化时需要克服离子键,这几种物质熔化时克服的相互作用力相同说明晶体类型相同,据此分析解答.
解答 解:分子晶体熔化时需要克服分子间作用力,原子晶体熔化时需要克服共价键,金属晶体熔化时需要克服金属键,离子晶体熔化时需要克服离子键,这几种物质熔化时克服的相互作用力相同说明晶体类型相同,
金刚石和水晶属于原子晶体,熔化时需要克服共价键;
食盐属于离子晶体,熔化时需要克服离子键;
干冰属于分子晶体,熔化时需要克服分子间作用力;
铝属于金属晶体,熔化时需要克服金属键,
通过以上分析知,克服相互作用力相同的是金刚石和水晶,
故选A.
点评 本题以晶体熔化为载体考查晶体中存在的作用力,明确物质的构成微粒是解本题关键,注意化学键与分子间作用力的区别,题目难度不大.


 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ①②⑤ | C. | 只有③④ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
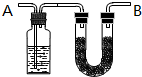 将含有C、H、O的有机物3.24g装入元素分析装置,通入足量的O2使之完全燃烧,将生成的气体依次通过管A和管B,测得A管质量增加了2.16g,B管增加了9.24g,已知该有机物的相对分子质量为108.
将含有C、H、O的有机物3.24g装入元素分析装置,通入足量的O2使之完全燃烧,将生成的气体依次通过管A和管B,测得A管质量增加了2.16g,B管增加了9.24g,已知该有机物的相对分子质量为108. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用氢氧化钠溶液吸收二氧化氮:2OH-+2NO2=NO${\;}_{3}^{-}$+NO↑+H2O | |
| B. | 向Na2S2O3溶液中通入足量氯气:S2O32-+2Cl2+3H2O=2SO32-+4Cl-+6H+ | |
| C. | 氧化亚铁溶于稀硝酸:FeO+2H+=Fe2++H2O | |
| D. | NH4HSO4溶液中加入等物质的量的Ba(OH)2溶液:NH4++H++SO42一+Ba2++2OH?=NH3•H2O+BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含共价键的共价化合物一定是分子晶体,分子晶体一定含共价键 | |
| B. | 固态可以导电的是离子晶体和金属晶体 | |
| C. | 由原子构成的晶体一定是原子晶体,由分子构成的晶体一定是分子晶体 | |
| D. | 判定晶体为离子晶体还是分子晶体的方法是看其熔融态是否能导电 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
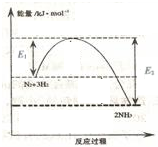 氨气在农业和国防工业都有很重要的作用,历史上诺贝尔奖曾经有三次颁给研究合成氨的科学家.
氨气在农业和国防工业都有很重要的作用,历史上诺贝尔奖曾经有三次颁给研究合成氨的科学家.| 时间/min | 20 | 60 | 40 | 80 |
| n(N2)/mol | 0.016 | 0.032 | 0.040 | 0.040 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的浊液中逐滴加入1mol•L-1 HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如图所示,试回答:
把NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后有1.16g白色沉淀,在所得的浊液中逐滴加入1mol•L-1 HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如图所示,试回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com