
| A. | 含共价键的共价化合物一定是分子晶体,分子晶体一定含共价键 | |
| B. | 固态可以导电的是离子晶体和金属晶体 | |
| C. | 由原子构成的晶体一定是原子晶体,由分子构成的晶体一定是分子晶体 | |
| D. | 判定晶体为离子晶体还是分子晶体的方法是看其熔融态是否能导电 |
分析 A.含有共价键的共价化合物不一定是分子晶体,可能是原子晶体,分子晶体中不一定含有共价键;
B.固态可以导电的是金属晶体或石墨;
C.原子晶体的构成微粒是原子,分子晶体的构成微粒是分子;
D.分子晶体在熔融态以分子存在,离子晶体在熔融态以离子存在.
解答 解:A.含有共价键的共价化合物不一定是分子晶体,可能是原子晶体,如金刚石等,分子晶体中不一定含有共价键,如稀有气体,故A错误;
B.固态可以导电的是金属晶体或石墨,离子晶体固态没有自由移动的离子,所以不导电,故B错误;
C.原子晶体的构成微粒是原子,分子晶体的构成微粒是分子,分子都是由原子构成的,所以由原子构成的晶体不一定是原子晶体,故C错误;
D.分子晶体在熔融态以分子存在,离子晶体在熔融态以离子存在,所以熔融状态下,分子晶体不导电、离子晶体导电,故D正确;
故选D.
点评 本题考查晶体的构成微粒、晶体的性质,根据物质的构成微粒确定晶体类型,易错选项是A,稀有气体中不含化学键,为易错点.


 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案科目:高中化学 来源: 题型:填空题
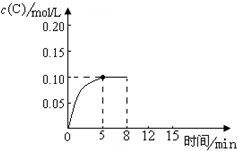 在500℃时,将足量的A固体投入2.0L真空密闭容器中,发生A(s)═2B(g)+C(g)反应,测得气体C随时间的浓度变化如图所示
在500℃时,将足量的A固体投入2.0L真空密闭容器中,发生A(s)═2B(g)+C(g)反应,测得气体C随时间的浓度变化如图所示查看答案和解析>>
科目:高中化学 来源: 题型:选择题
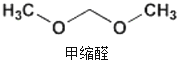 2015年央视3.15晚会曝光了山东省东营市、滨州市许多不法厂商,把一部分90号的汽油配上大量的石脑油、芳烃、甲缩醛等调和成“93号汽油”.查资料知,甲缩醛是一种无色易挥发可燃液体,主要用于生产杀虫剂、皮革和汽车上光剂等,是现行的车用汽油国家标准中不得添加的有害物质,它易造成汽车线路漏油,对动物有麻醉作用,也有一定毒性.下列对其说法中正确的是( )
2015年央视3.15晚会曝光了山东省东营市、滨州市许多不法厂商,把一部分90号的汽油配上大量的石脑油、芳烃、甲缩醛等调和成“93号汽油”.查资料知,甲缩醛是一种无色易挥发可燃液体,主要用于生产杀虫剂、皮革和汽车上光剂等,是现行的车用汽油国家标准中不得添加的有害物质,它易造成汽车线路漏油,对动物有麻醉作用,也有一定毒性.下列对其说法中正确的是( )| A. | 甲缩醛和乙醛互为同系物 | |
| B. | 用甲醇和甲醛生产甲缩醛的反应为加成反应 | |
| C. | 等物质的量的甲缩醛和丙炔完全燃烧的耗氧量相同 | |
| D. | 用甲缩醛生产杀虫剂、皮革和汽车上光剂等,均是利用了它的毒性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③ | C. | ③④ | D. | ①⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 的分子式为C12H16O.
的分子式为C12H16O. 分子中,处于同一平面上的原子数最多可能有16个.
分子中,处于同一平面上的原子数最多可能有16个. 系统命名为4,4-二甲基-2-戊醇.
系统命名为4,4-二甲基-2-戊醇.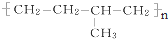 的单体为CH2=CH2、CH3-CH=CH2.
的单体为CH2=CH2、CH3-CH=CH2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
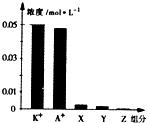 常温下,0.1mol•L-1一元酸HA与等浓度KOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )
常温下,0.1mol•L-1一元酸HA与等浓度KOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )| A. | 该混合溶液pH=7.0 | B. | 原HA溶液中:c(HA)>c(H+)>c(A-) | ||
| C. | 图中X表示HA,Y表示OH-,Z表示H+ | D. | 混合溶液中:c(X)+x(A-)=c(K+) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
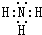 ,A在周期表中的位置第一周期第ⅠA族.
,A在周期表中的位置第一周期第ⅠA族.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
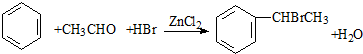 (卤烷基化反应)
(卤烷基化反应)
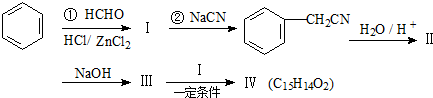
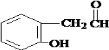 ,
,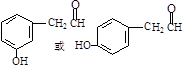 .
.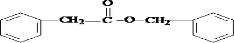 .
.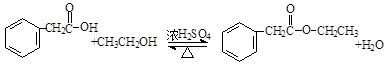 .
.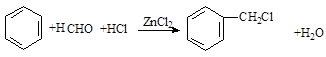 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com