
A.[物质结构与性质]
元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p轨道上有4个电子。元素Z的原子最外层电子数是其内层的3倍。
(1)X与Y所形成化合物晶体的晶胞如右图所示。
 ①在1个晶胞中,X离子的数目为 。
①在1个晶胞中,X离子的数目为 。
②该化合物的化学式为 。
(2)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是
。
(3)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是
。
(4)Y与Z可形成YZ42-
①YZ42-的空间构型为 (用文字描述)。
②写出一种与YZ42-互为等电子体的分子的化学式: 。
(5)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为 。
【参考答案】
(1)①4 ②ZnS
(2)sp3
(3)水分子与乙醇分子之间形成氢键
(4)①正四面体 ②CCl4或SiCl4
(5)16mol或16×6.02×1023个
【解析】本题考查学生对原子核外电子排布、晶体结构与计算、原子轨道 杂化类型、分子空间构型、氢键、配合物等《选修三》中基础知识的掌握和应用能力。本题基础性较强,重点特出。
杂化类型、分子空间构型、氢键、配合物等《选修三》中基础知识的掌握和应用能力。本题基础性较强,重点特出。
元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2,显然是锌。元素Y基态原子的3p轨道上有4个电子,即硫。元素Z的原子最外层电子数是其内层的3倍,为氧。
(1)①在1个晶胞中,Zn离子的数目为8×1/8+6×1/2=4。
②S离子的数目也为4,化合物的化学式为ZnS。
(4)①SO42-的空间构型根据VSEPR模型与杂化类型可知无孤对电子为正四面体。
②SO42-互为等电子体的分子的化学式CCl4或SiCl4
(5)锌的氯化物与氨水反应可形成配合物[Zn(NH3)4]Cl2,1mol该配合物中含有σ键的数目既要考虑到配体中,还要考虑配 体与中心原子之间的配位键,因此1mol该配合物中含有σ键的数目为16mol或16×6.02×1023个。
体与中心原子之间的配位键,因此1mol该配合物中含有σ键的数目为16mol或16×6.02×1023个。


科目:高中化学 来源: 题型:
1mol/L硫酸溶液的含义是
A.1L水中含有1molH2SO4 B.溶液中含有1molH2SO4
C.将98g浓硫酸溶于水配成1L溶液 D.指1L硫酸溶液中含有98gH2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
石墨烯[如图(a)所示]是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯[如图(b)所示]。
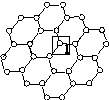
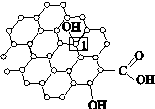
(a)石墨烯结构 (b)氧化石墨烯结构
(1)图(a)中,1号C与相邻C形成σ键的个数为________。
(2)图(b)中,1号C的杂化方式是________,该C与相邻C形成的键角________(填“>”“<”或“=”)图(a)中1号C与相邻C形成的键角。
(3)若将图(b)所示的氧化石墨烯分散在H2O中,则氧化石墨烯中可与H2O形成氢键的原子有________(填元素符号)。
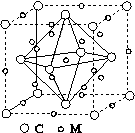
(4)石墨烯可转化为富勒烯(C60),某金属M与C60可制备一种低温超导材料,晶胞如图所示,M原子位于晶胞的棱上与内部。该晶胞中M原子的个数为________,该材料的化学式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
[选修3——物质结构与性质] Ⅰ.对于钠的卤化物(NaX)和硅的卤化物(SiX4),下列叙述正确的是( )
A.SiX4难水解
B.SiX4是共价化合物
C.NaX易水解
D.NaX的熔点一般高于SiX4
Ⅱ.碳元素的单质有多种形式,下图依次是C60、石墨和金刚石的结构图:
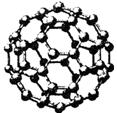
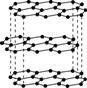
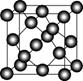
C60 石墨 金刚石晶胞
回答下列问题:
(1)金刚石、石墨、C60、碳纳米管等都是碳元素的单质形式,它们互为________________。
(2)金刚石、石墨烯(指单层石墨)中碳原子的杂化形式分别为________、________。
(3)C60属于________晶体,石墨属于________晶体。
(4)石墨晶体中,层内C—C键的键长为142 pm,而金刚石中C—C键的键长为154 pm。其原因是金刚石中只存在C—C间的________共价键,而石墨层内的C—C间不仅存在________共价键,还有________键。
(5)金刚石晶胞含有________个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r=____________a,列式表示碳原子在晶胞中的空间占有率____________________(不要求计算结果)。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、R为前四周期元素且原子序数依次增大。X的单质与氢气可以化合生成气体G,其水溶液pH>7;Y单质是一种黄色晶体;R基态原子3d轨道的电子数是4s轨道电子数的3倍。Y、Z分别与钠元素可以形成化合物Q和J,J的水溶液与AgNO3溶液反应可生成不溶于稀硝酸的白色沉淀L;Z与氢元素形成 的化合物与G反应生成M。
的化合物与G反应生成M。
请回答下列问题:
⑴M固体的晶体类型是 。
⑵Y基态原子的核外电子排布式是 ① ;G分子中X原子的杂化轨道的类型是 ② 。
⑶L的悬浊液加入Q的溶液,白色沉淀转化为黑色沉淀,其原因是 。
⑷R的一种含氧酸根RO42-具有强氧化性,在其钠盐中加入稀硫酸,溶液变为黄色,并有无色气体产生,该反应的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)可正确表示原子轨道的是________。
A.2s B.2d
C.3px D.3f
(2)写出基态镓(Ga)原子的电子排布式:________。
(3)下列物质变化,只与范德华力有关的是________ 。
A.干冰熔化 B.乙酸汽化
C.乙醇与丙酮混溶 D.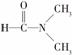 溶于水
溶于水
E.碘溶于四氯化碳 F.石英熔融
(4)下列物质中,只含有极性键的分子是________,既含离子键又含共价键的化合物是________;只存在σ键的分子是________,同时存在σ键和π键的分子是________。
A. N2 B.CO2 C.CH2Cl2 D.C2H4
E.C2H6 F.CaCl2 G.NH4Cl
(5)用“>”、“<”或“=”填空:
第一电离能的大小:Mg________Al;熔点的高低:KCl________ MgO。
查看答案和解析>>
科目:高中化学 来源: 题型:
元素的原子结构决定其性质和在周期表中的位置。下列说法正确的是
A.元素原子的最外层电子数等于元素的最高化合价
B.多电子原子中,在离核较近的区域内运动的电子能量较高
C.P、S、Cl得电子能力和最高价氧化物对应的水化物的酸性均依次增强
D.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.原子最外层电子数为2的元素一定处于周期表IIA族
B.主族元素X、Y能形成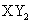 型化合物,则X与Y 的原子序数之差可能为2或5
型化合物,则X与Y 的原子序数之差可能为2或5
C.氯化氢的沸点比氟化氢的沸点高
D.同主族元素形成的氧化物的晶体类型均相同
查看答案和解析>>
科目:高中化学 来源: 题型:
铋(Bi)在医药方面有重要应用。下列关于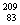 Bi和
Bi和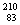 Bi的说法正确的是
Bi的说法正确的是
A 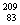 Bi和
Bi和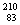 Bi都含有83个中子
Bi都含有83个中子
B 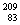 Bi和
Bi和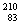 Bi互为同位素
Bi互为同位素
C 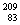 Bi和
Bi和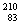 Bi的核外电子数不同
Bi的核外电子数不同
D 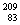 Bi和
Bi和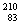 Bi分别含有126和127个质子
Bi分别含有126和127个质子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com