

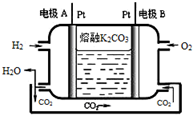
���� ��1����������������Ư���Լ����������Ư���ԣ�������⻯�ط�Ӧ���ɵ⣬�����������Ȼ�̼���ֲ��Һ����÷�Һ�ķ������룻
��2��������ͷ�������ж�ѹǿ�Ĵ�С�������ѹǿ�����ڷ�Һ©���ڵ�Һ��˳�����£�
��3������������Ũ�����ڼ��������·�Ӧ�����Ȼ��̡�������ˮ��
��� �⣺��1��Cl2��ɺ첼������Ӧ�����У���û�д��������ɣ�������ɫ��������ɫ��Cl2��H2O��Ӧ���ɵ�HClO��Ư�����ã����Ա��к�ɫ������ɫ��Cl2��KI��Һ��Ӧ����I2���ʣ�CCl4��ȡ�ⵥ�ʣ���Һ�ֲ㣬���÷�Һ�ķ������룻
�ʴ�Ϊ�������Ա仯���첼����ɫ���÷�Һ©����Һ��
��2��������ͷ����Ƥ�����Ӻ�Һ©������ƿ����ѹ��ȣ�������Һ�����£�
�ʴ�Ϊ�����ڣ���֤��Һ©��Һ���ϡ�������ѹǿ��ȣ����ڷ�Һ©����Һ��˳�����£�
��3������������Ũ�����ڼ��������·�Ӧ�����Ȼ��̡�������ˮ����ѧ����ʽΪ��4HCl��Ũ��+Mn02 $\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+C12��+2H20��
�ʴ�Ϊ��4HCl��Ũ��+Mn02 $\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+C12��+2H20��
���� ���⿼������������ȡ�����ʼ��������̽����ʵ�����ƣ���ȷ�����ʹ�����������ǽ���ؼ���ע��������ʷ���ѡ���ԭ����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������Ԫ��X��Y��Z��W��Ԫ�����ڱ������λ����ͼ��ʾ������Y������������������������ȣ���Ҫ��ش��������⣺
������Ԫ��X��Y��Z��W��Ԫ�����ڱ������λ����ͼ��ʾ������Y������������������������ȣ���Ҫ��ش��������⣺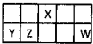
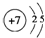 ��
��| �¶�/�� | 400 | 500 | 800 |
| ƽ�ⳣ��K | 9.94 | 9 | 1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ҵ�ƽ����ƣ���ⱥ��ʳ��ˮ | |
| B�� | ��ҵ���壺ijЩֲ���и�������������Ӻ���Ʒ����ȡ���ǹ�ҵ�ϻ�ȡ�����Ҫ;�� | |
| C�� | ұ���������Al2O3��ͬʱ�������ʯ��Na3AlF6����Ŀ����Ϊ�˽���Al2O3�����¶� | |
| D�� | ���Ṥҵ�����������������£��ӽӴ��ҽ����������������в����ܺ���SO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
NaHCO3��Һ BaCl2Ũ�� | 0.2mol•L-1 | 0.1mol•L-1 | 0.02mol•L-1 |
| 0.2mol•L-1 | ���� | ���� | �������� |
| 0.1mol•L-1 | ���� | �������� | ������ |
| 0.02mol•L-1 | �������� | ������ | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 6.72L CO | B�� | 6.6g CO2 | C�� | 8 g SO2 | D�� | 9.6g H2SO4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ�£�0.1mol D216O�к�������������������������ΪNA | |
| B�� | �Ȼƽ��18O2����ͨ��16O2�����ֲ�ͬ�ĺ��� | |
| C�� | ��״���£�2.24LCl2����ˮ��ת�Ƶĵ�����ĿΪ0.1NA | |
| D�� | 1L2mol•L-1��Al��NO3��3��Һ�к�Al3+����Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
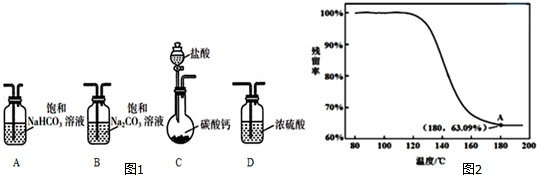
| A�� | 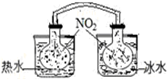 ������������������ɫ�仯���жϷ�Ӧ2NO2��g��?N2O4��g��ƽ���ƶ��ķ��� | |
| B�� | 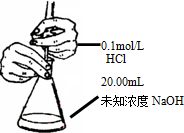 �ⶨ��ƿ�ڵ�NaOH��Ũ�� | |
| C�� | 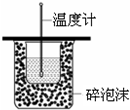 �ⶨ�к��� | |
| D�� | 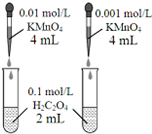 ������ɫ�����Ƚ�Ũ�ȶԷ�Ӧ���ʵ�Ӱ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C1��C2 | B�� | C1=C2 | C�� | C1��C2 | D�� | ��ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����C��D�γɵĻ�����ĵ���ʽ
����C��D�γɵĻ�����ĵ���ʽ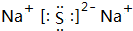 ��
���鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com